Clear Sky Science · de
Beschleunigte und lokalisierte Synukleinopathie in einem hybridem Mausmodell: Auswirkungen auf Positronen-Emissions-Tomographie-Studien
Warum diese Forschung wichtig ist
Morbus Parkinson ist vor allem durch Zittern und Bewegungsstörungen bekannt, beginnt im Gehirn jedoch mit winzigen Veränderungen, die schwer zu erkennen sind. Ärztinnen und Ärzte benötigen dringend Methoden, um diese frühen Veränderungen zu entdecken und neue Medikamente rasch zu testen. Diese Studie beschreibt ein verfeinertes Mausmodell, das zentrale Merkmale der Parkinson-ähnlichen Hirnschädigung in nur wenigen Wochen und in einer sehr spezifischen Hirnregion reproduziert – zugeschnitten für den Einsatz mit fortgeschrittenen Hirnscans wie der PET-Bildgebung. 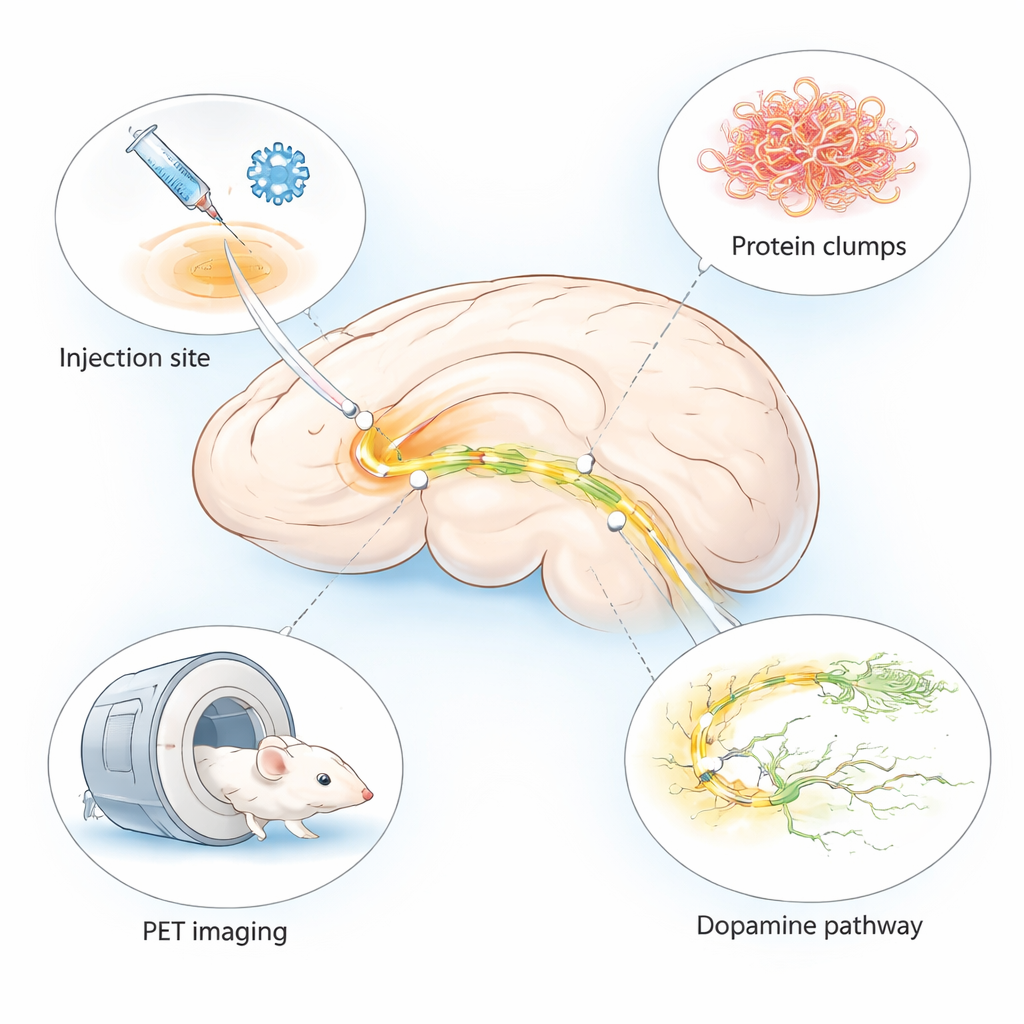
Aufbau eines schnelleren, fokussierteren Krankheitsmodells
Viele bestehende Tiermodelle für Morbus Parkinson brauchen Monate, bis Symptome auftreten, oder zeigen nicht das volle Spektrum der im Menschen beobachteten Hirnveränderungen. Die Autoren kombinierten zwei etablierte Ansätze zu einem einzigen „hybriden“ Modell. Sie injizierten ein harmloses Virus, das Gehirnzellen zur Produktion von menschlichem Alpha‑Synuklein anregt – einem Protein, das sich bei Parkinson verklumpt – zusammen mit vorgeformten Fibrillen, die als Samen wirken und weiteres Verklumpen auslösen. Beides wurde in eine kleine, bewegungsrelevante Region namens Substantia nigra auf einer Seite des Mausgehirns verabreicht. Dieses Design erzeugt lokale, aber intensive krankheitsähnliche Veränderungen auf der injizierten Seite, während die andere Seite relativ gesund bleibt und als Vergleich dient.
Nachverfolgung von Proteinablagerungen und sterbenden Nervenzellen
Bereits zwei Wochen nach der Injektion zeigten die Mäuse hohe Werte von humanem Alpha‑Synuklein und seiner abnormal phosphorylierten Form in der Zielregion. Unter dem Mikroskop beobachteten die Forschenden Strukturen, die Lewy-Körpern und Lewy-Neuriten ähnelten – Kennzeichen der Parkinson-Krankheit. Im Verlauf mehrerer Wochen nahmen diese abnormalen Ablagerungen zu. Gleichzeitig begannen Zellen, die den Botenstoff Dopamin produzieren – entscheidend für flüssige Bewegungen – zu schwinden. Marker für diese Zellen fielen bis zur fünften Woche auf etwa 60 Prozent des Niveaus der unbehandelten Seite und bestätigen damit einen klaren, progressiven Verlust des Dopaminsystems.
Entzündung, schwindende Synapsen und müde Kraftwerke
Die Immunzellen des Gehirns, sogenannte Mikroglia, schalteten in der Region um die Schädigung herum ebenfalls in einen hochaktiven, entzündlichen Zustand. Färbungen für mehrere entzündungsassoziierte Proteine waren in der Nähe von Alpha‑Synuklein-Ablagerungen deutlich stärker als auf der gegenüberliegenden Gehirnseite. Später im Prozess entdeckte das Team einen Verlust von Synapsen – den winzigen Kontaktpunkten, an denen Nervenzellen kommunizieren – sowie Hinweise darauf, dass Mitochondrien, die Energiefabriken der Zellen, nicht richtig funktionieren. Zusammengenommen zeigen diese Befunde, dass das Modell nicht nur Proteinablagerungen erzeugt, sondern auch die Kaskade aus Entzündung, versagenden Verbindungen und Energieproblemen abbildet, die zum Zelluntergang bei Morbus Parkinson beiträgt. 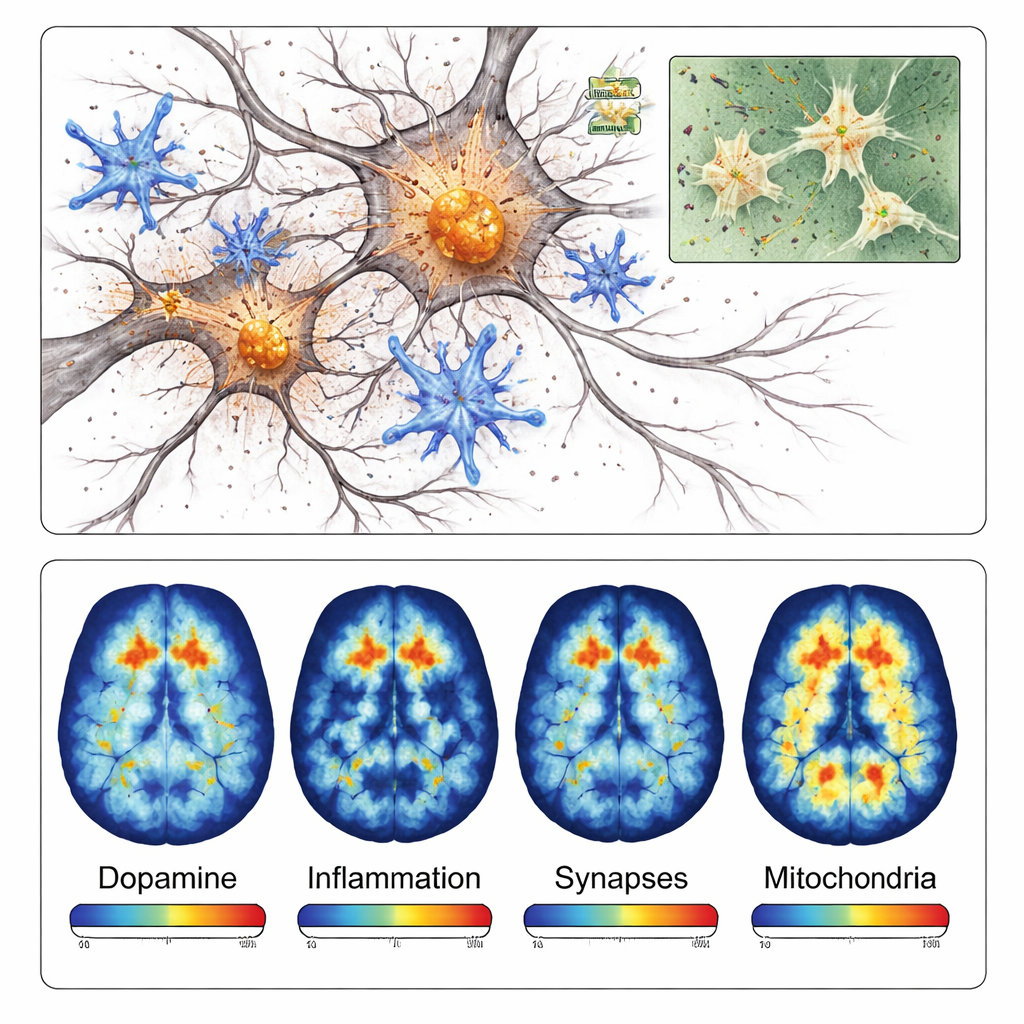
PET-Scanner in der Anwendung
Da dieses Modell lokal begrenzt ist und sich schnell entwickelt, eignet es sich besonders gut für die Positronen-Emissions-Tomographie (PET), eine Scan-Technik, die spezifische Moleküle im lebenden Gehirn messen kann. Die Forschenden testeten vier verschiedene PET-Tracer, die an dopaminerge Nervenendigungen, entzündliche Mikroglia, synaptische Proteine und mitochondriale Enzyme binden. In jedem Fall zeigten PET-Aufnahmen auf der injizierten Seite niedrigere oder höhere Signale in einer Weise, die mit den mikroskopischen Befunden übereinstimmte. Beispielsweise zeigte der Tracer für dopaminerge Bahnen etwa 40 Prozent weniger Signal auf der geschädigten Seite, während der Entzündungs-Tracer über 40 Prozent höhere Signale in der betroffenen Region zeigte.
Was das für Patientinnen, Patienten und zukünftige Behandlungen bedeutet
Dieses neue Mausmodell vereint in kurzer Zeit viele der zentralen Veränderungen, die sich beim Menschen mit Morbus Parkinson über Jahre entwickeln. Da die Schädigung auf einen kleinen, genau definierbaren Bereich beschränkt ist und mit PET-Scans verfolgt werden kann, können Forschende neue Bildgebungstracer und potenzielle Therapien effizienter testen. Obwohl keine Maus die menschliche Erkrankung vollständig reproduzieren kann, bietet dieser Ansatz ein leistungsfähiges, praktisches Werkzeug, um die Lücke zwischen Grundlagenforschung und Humanstudien zu überbrücken, letztlich die Diagnostik zu verfeinern und die Suche nach besseren Behandlungen zu beschleunigen.
Zitation: Xia, C.A., Tsai, HM., Diaz Garcia, S. et al. Accelerated and localized synucleinopathy in a hybrid mouse model: implications for positron emission tomography studies. npj Imaging 4, 7 (2026). https://doi.org/10.1038/s44303-026-00138-x
Schlüsselwörter: Morbus Parkinson, Alpha-Synuklein, Synukleinopathie, PET-Bildgebung, Mausmodell