Clear Sky Science · de
Modelle gewöhnlicher Differentialgleichungen der SARS-CoV-2-Replikationsdynamik und Wirkstärken antiviraler Medikamente
Warum Zahlen für ein neues Virus wichtig sind
Als COVID-19 auftauchte, konnten Ärztinnen und Ärzte sehen, was das Virus bei Patientinnen und Patienten anrichtet, aber sie konnten nicht leicht vorhersagen, wer schwer erkranken würde oder wann ein Medikament am wirksamsten verabreicht werden sollte. Dieser Übersichtsartikel beschreibt, wie Forschende Virusmessungen aus Patienten, Tieren und Zellkulturen in mathematische „Filme“ der Infektion im Körper verwandelt haben. Diese Modelle nutzen Gleichungen, um zu verfolgen, wie das Virus wächst, wie unsere Zellen und das Immunsystem reagieren und wie antivirale Medikamente und Impfstoffe das Kräfteverhältnis zu unseren Gunsten verschieben können.
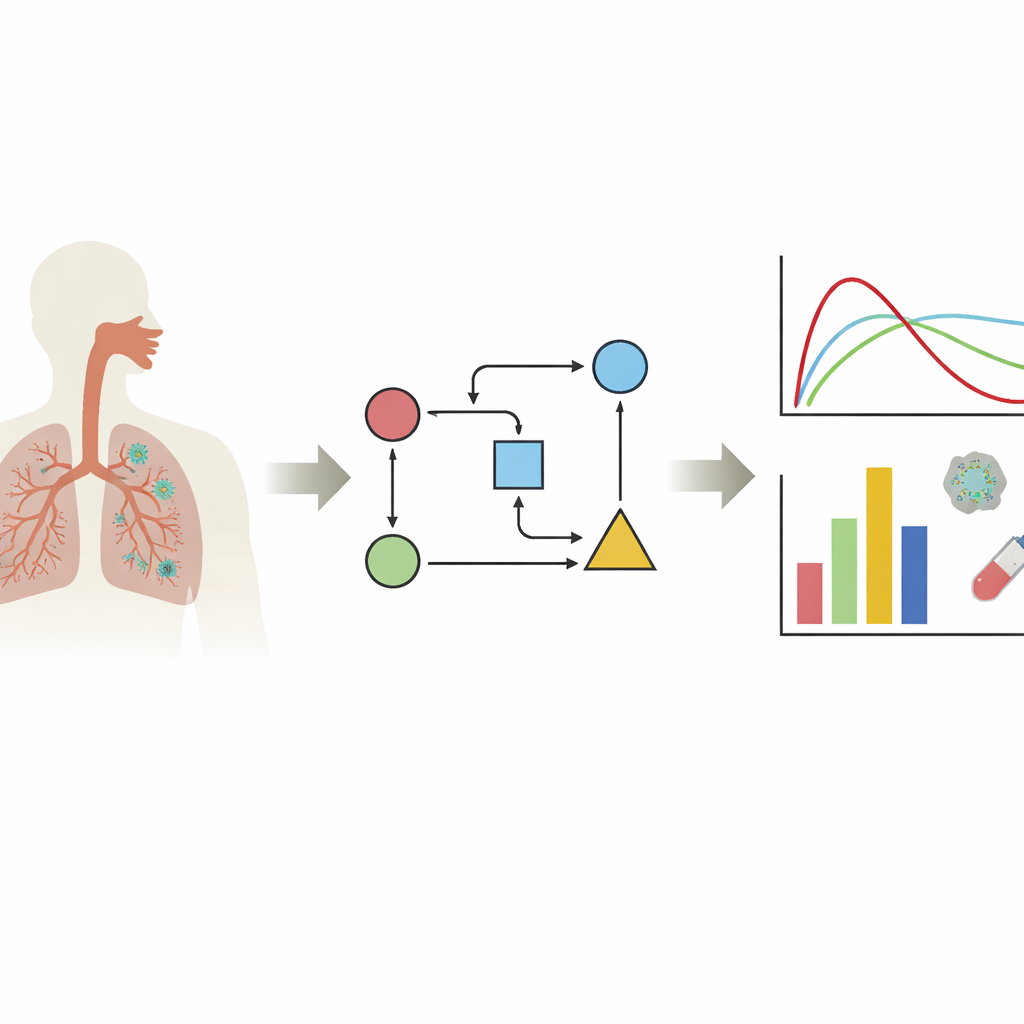
Dem Virus im Körper folgen
Die Autorinnen und Autoren konzentrieren sich auf eine Modellfamilie, die als zielzellenlimitierte Modelle bezeichnet wird. Einfach gesagt verfolgen diese Modelle drei Hauptakteure: gesunde Zellen, die infiziert werden können, bereits infizierte Zellen und freie Viruspartikel. Indem reale Daten zu Viruskonzentrationen in diese Gleichungen eingespeist werden, können Forschende verborgene Merkmale der Infektion abschätzen: wie schnell das Virus Zellen infiziert, wie lange eine infizierte Zelle Virus produziert und wie schnell das Virus eliminiert wird. Die Übersicht zeigt, dass sich die meisten Arbeiten auf die für COVID-19 wichtigsten Gewebe konzentrieren — die Nase sowie die oberen und unteren Atemwege — während nur wenige Modelle andere Organe untersuchen. Eine zentrale Botschaft ist, dass sich das Verhalten des Virus je nach Gewebe, Virusvariante und verwendeter Zelllinie sehr unterschiedlich darstellen kann, sodass es keine einzige „typische“ Infektionskurve gibt.
Was wir über das Immunsystem lernen
Viele Modelle fügen Schichten hinzu, die die frühen Abwehrmechanismen des Immunsystems und seine langsamere, gezieltere Reaktion darstellen. Studien, die sich auf die erste Verteidigungslinie konzentrieren, legen nahe, dass ein schnelles, gut getimtes Eingreifen durch angeborene Immunzellen und Signalmoleküle die Infektion abschwächen kann, sie aber selten allein vollständig beseitigt. Andere Arbeiten heben die entscheidende Rolle von T-Zellen und Antikörpern hervor, die das Virus schließlich unter Kontrolle bringen. Die Modelle erfassen auch eine dunkle Seite: Wenn die gezielte Immunantwort spät oder fehlgeleitet einsetzt, können dieselben Mechanismen, die eigentlich schützen sollen, schädliche „Zytokinstürme“ antreiben, bei denen überschüssige Entzündungssignale gesundes Gewebe schädigen. In diesen Simulationen entscheidet oft das fragile Gleichgewicht zwischen nützlicher und schädlicher Immunaktivität darüber, ob die Erkrankung mild bleibt oder lebensbedrohlich wird.
Wann Medikamente und Impfstoffe am besten wirken
Weil Gleichungen immer wieder unter unterschiedlichen Annahmen durchgespielt werden können, sind sie mächtige Werkzeuge, um Behandlungsstrategien am Computer zu testen, bevor sie an Menschen erprobt werden. In vielen Studien stimmen die Modelle in einem zentralen Punkt überein: antivirale Medikamente wirken am besten, wenn sie sehr früh verabreicht werden, bevor das Virus seinen Gipfel erreicht und den Großteil der verfügbaren Zellen infiziert hat. Wirkstoffe, die die Kopie des viralen Erbguts blockieren, erscheinen besonders vielversprechend, vor allem in Kombination mit anderen Medikamenten, die über unterschiedliche Mechanismen wirken. Späte Behandlungen haben in Simulationen dagegen meist wenig Wirkung, es sei denn, mehrere starke Wirkstoffe werden gleichzeitig eingesetzt. Impfungen schneiden durchweg besser ab als Medikamente allein, vor allem weil sie das Immunsystem vorbereiten, das Virus schnell zu erkennen und hohe Viruslasten kurzlebig zu halten.
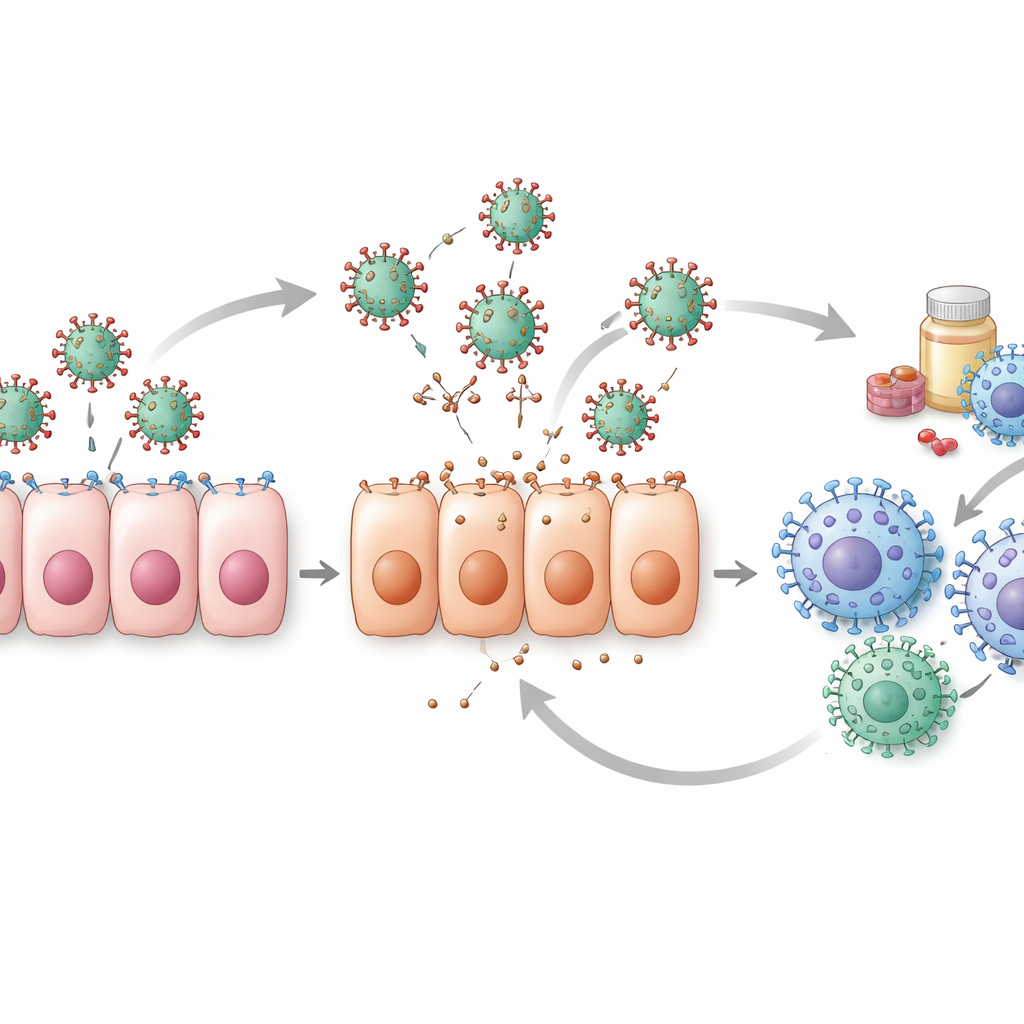
Verborgene Probleme in den Daten
Die Übersicht beleuchtet auch die Schwächen hinter den Zahlen. Die meisten klinischen Datensätze beginnen erst, nachdem Menschen bereits Symptome verspüren, was bedeutet, dass Modelle häufig die entscheidenden ersten Tage der Infektion verpassen, in denen die Viruskonzentrationen am schnellsten ansteigen. Ohne diese frühen Messungen können verschiedene Kombinationen von Modellparametern dieselben Daten erklären, wodurch es schwer wird, sicher zu sein, welche Erklärung zutrifft. Nur eine Minderheit der Studien führt rigorose Prüfungen durch, um zu prüfen, ob ihre Parameterschätzungen wirklich eindeutig und zuverlässig sind. Tierstudien und Experimente in Zellkulturen helfen, einige Lücken zu schließen, insbesondere für frühe Zeitpunkte, aber Unterschiede zwischen Arten und Laborsystemen begrenzen, wie direkt diese Ergebnisse auf den Menschen übertragbar sind.
Was das für die Zukunft bedeutet
Für Nicht-Spezialisten ist die Schlussfolgerung, dass sorgfältig gebaute mathematische Modelle unser Verständnis darüber, wie sich SARS-CoV-2 im Körper verhält und wie Timing, Wirkstoffkombinationen und vorherige Impfung den Ausgang beeinflussen, deutlich verbessert haben. Die Modelle sind sich weitgehend einig, dass frühzeitiges, starkes Eingreifen — insbesondere durch Impfung und rechtzeitig eingesetzte antivirale Mittel — dem Immunsystem die besten Chancen gibt zu siegen, während verzögerte Reaktionen, sei es vom Körper oder von der Behandlung, mit schwereren Verläufen verbunden sind. Gleichzeitig betonen die Autorinnen und Autoren, dass diese Werkzeuge nur so gut sind wie die Daten, die man ihnen zuführt. Zur Vorbereitung auf künftige Varianten oder neue Viren fordern sie reichhaltigere, frühere klinische Probenahmen und breitere Immunmessungen, damit die „Zahlen hinter der Infektion“ schnellere, genauere Entscheidungen in realen Ausbrüchen leiten können.
Zitation: Kapischke, T., Herrmann, S.T., Bertzbach, L.D. et al. Ordinary differential equation models of SARS-CoV-2 replication dynamics and antiviral drug efficacies. npj Viruses 4, 17 (2026). https://doi.org/10.1038/s44298-026-00183-8
Schlüsselwörter: SARS-CoV-2-Viraldynamik, Within-Host-Modellierung, Timing antiviraler Therapien, Immunantwort, COVID-19-Impfung