Clear Sky Science · de
Unterschiedliche Rollen der Hsp70‑Chaperone bei der Proteinsekretion und Virionbildung von Orthoflaviviren
Warum winzige Hitzeschock‑Helfer für gehirninfizierende Viren wichtig sind
Von Zecken und Mücken übertragene Viren wie das Frühsommer‑Meningoenzephalitis‑Virus und das West‑Nil‑Virus können das Gehirn befallen und schwere Erkrankungen auslösen, doch spezifische Medikamente gegen sie fehlen noch. Diese Studie untersucht, wie diese Viren eine Reihe körpereigener Proteinhilfen, die sogenannten Hsp70‑Chaperone, kapern, um neue Viruspartikel zu bauen und freizusetzen. Da Hsp70‑Proteine bereits als Wirkstoffziele in der Krebsforschung verfolgt werden, könnte das Verständnis dieser Wechselwirkung neue Wege eröffnen, gefährliche Virusinfektionen zu behandeln, ohne die Viren direkt anzugreifen.
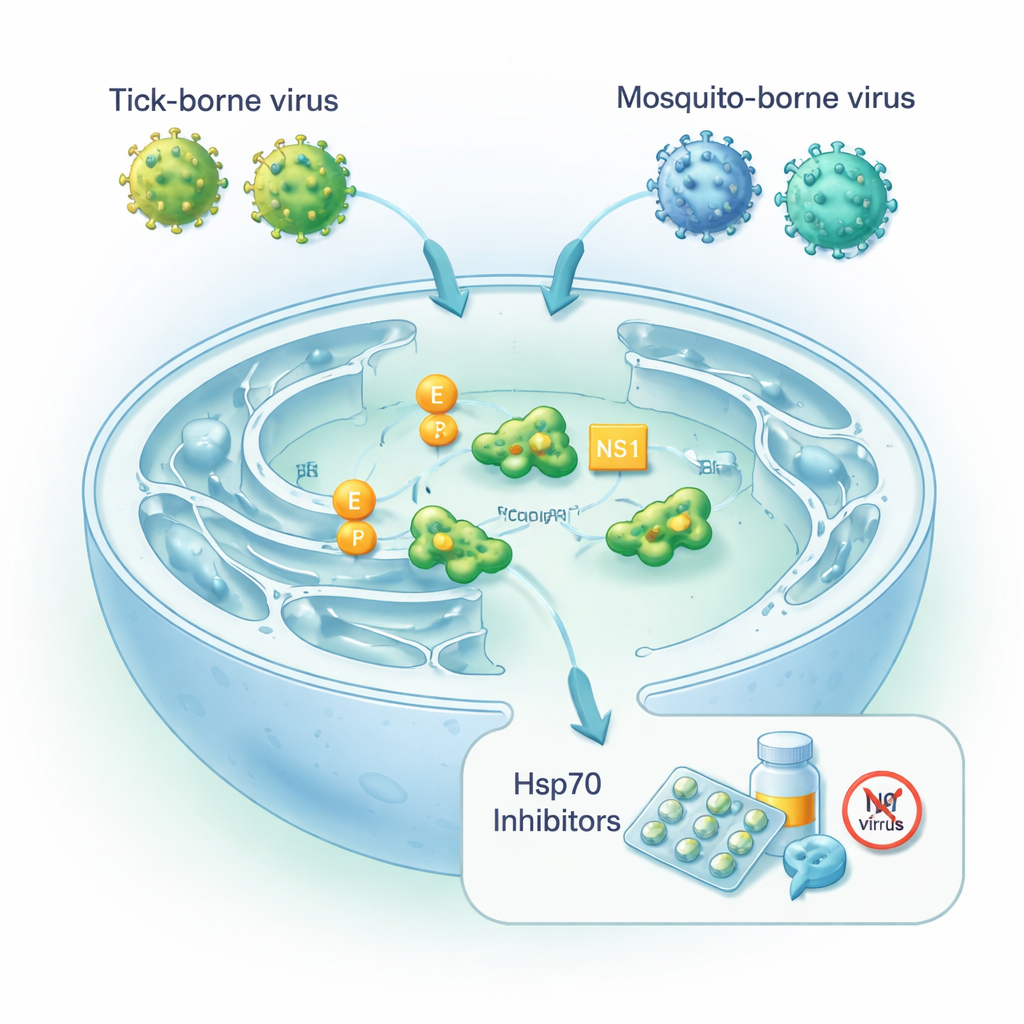
Viren, die auf die Faltungsmaschinerie der Zelle angewiesen sind
Orthoflaviviren sind kleine RNA‑Viren, deren Erbgut ein langes Polyprotein kodiert, das zugeschnitten und in mehrere funktionelle Teile gefaltet werden muss. Zwei wichtige virale Komponenten sind das Hüllprotein E, das das Partikel umgibt und den Eintritt in neue Zellen ermöglicht, und das nicht‑strukturale Protein NS1, das der Virusreplikation dient und sekretorisch freigesetzt werden kann, um das Immunsystem zu beeinflussen. All dies geschieht im endoplasmatischen Retikulum, dem Ort der Zelle, an dem viele Proteine gefaltet und für den Export vorbereitet werden. Dort verlässt sich die Zelle auf Hsp70‑Chaperone, einschließlich einer dort ansässigen Form namens BiP, um neu synthetisierte Proteine bei Stress vor Fehlfaltung zu schützen. Die Autoren fragten, wie stark neurotrope, von Zecken und Mücken übertragene Orthoflaviviren auf diese Chaperone angewiesen sind, um infektiöse Partikel zu assemblieren.
Direkte Handshakes zwischen viralen Proteinen und Hsp70
Mit Zellen, die so verändert wurden, dass sie bestimmte virale Proteine überproduzieren, sowie mit Zellen, die mit authentischen Viren infiziert waren, zogen die Forscher BiP oder Hsp70 herunter und untersuchten, welche viralen Partner mitkamen. Sie fanden, dass BiP und Hsp70 beständig Komplexe mit dem Hüllprotein E mehrerer Orthoflaviviren bildeten, unabhängig davon, ob diese von Zecken oder Mücken übertragen wurden. Das deutet darauf hin, dass die Faltung von E im endoplasmatischen Retikulum von diesen Chaperonen gesteuert wird. Bei NS1 zeigte sich ein selektiveres Bild: BiP und Hsp70 banden stark an NS1 der zeckenübertragenen Viren (Frühsommer‑Meningoenzephalitis‑Virus und Langat‑Virus), jedoch nicht an NS1 der mückenübertragenen West‑Nil‑ und Usutu‑Viren. Diese Unterschiede spiegeln wahrscheinlich Variationen in der Glykosylierung und Faltung von NS1 wider und deuten darauf hin, dass nicht alle verwandten Viren dieselben Wirtswege nutzen.
Blockade der Chaperone reduziert Virusproduktion stark
Da Hsp70‑Proteine medikamentös angreifbar sind, testete das Team zwei kleine Moleküle, die verschiedene Teile der Chaperon‑Maschinerie stören. YM‑1 richtet sich gegen die nukleotidbindende Domäne und hält Hsp70‑Proteine in einem inaktiven Zustand fest, während PES‑Cl die Substratbindetasche blockiert, die normalerweise die Klientenproteine greift. Bei Konzentrationen, die die meisten Zellen überleben ließen, verringerte YM‑1 die Menge an freigesetztem infektiösem Virus für alle vier getesteten Orthoflaviviren drastisch und senkte die Menge des im Kulturmedium nachweisbaren Hüllproteins, was auf einen allgemeinen Block der Partikelbildung oder ‑freisetzung hindeutet. PES‑Cl hatte dagegen wenig Einfluss auf infektiöse Titere oder Hüllproteinmengen, obwohl es in Bindungsassays die physische Interaktion zwischen Hsp70/BiP und dem Hüllprotein schwächte. Das legt nahe, dass eine vorübergehende Störung der Greifstelle nicht ausreicht, um die Virusassemblierung lahmzulegen, während das Abschalten des energieabhängigen Zyklus des Chaperons dies vermag.
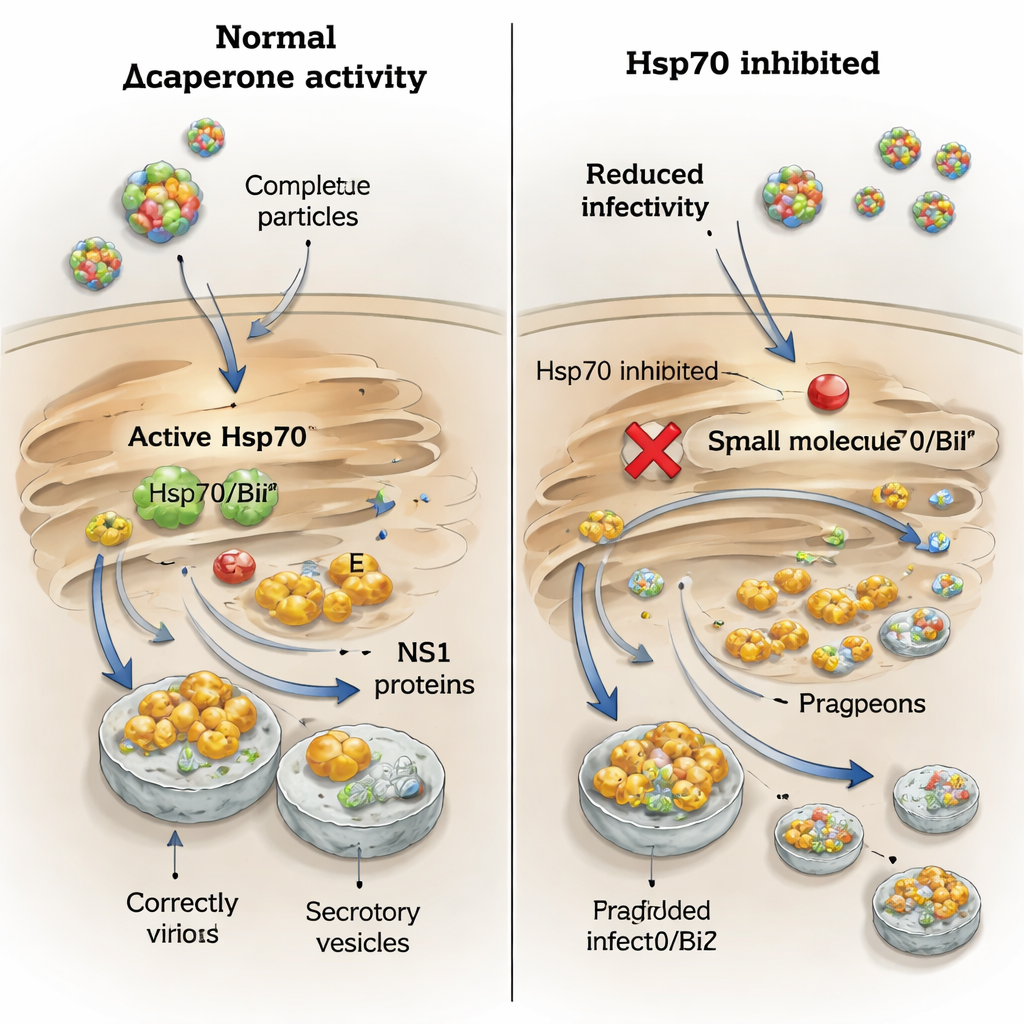
Eine besondere Abhängigkeit zeckenübertragener Viren von BiP für NS1
Die Geschichte für NS1 war nuancierter. Wurden infizierte Zellen mit PES‑Cl behandelt, sank die Sekretion von NS1 der Frühsommer‑Meningoenzephalitis‑ und Langat‑Viren stark, während NS1 von West‑Nil‑ und Usutu‑Viren unverändert blieb. Das spiegelt den früheren Befund wider, dass nur die zeckenübertragenen NS1‑Proteine stark an BiP und Hsp70 binden. Um BiPs Rolle näher zu beleuchten, setzten die Autoren kleine interferierende RNAs ein, um BiP‑Spiegel spezifisch zu senken. Dadurch verringerte sich die Menge sowohl des Hüllproteins als auch von NS1 innerhalb der Zellen und im umgebenden Medium für das Frühsommer‑Meningoenzephalitis‑ und das West‑Nil‑Virus, doch die infektiösen Virustiter fielen nur mäßig. Wenn BiP‑depletierte Zellen mit Medikamenten behandelt wurden, die den Proteinabbau blockieren, stiegen die intrazellulären NS1‑Mengen wieder an, doch seine Sekretion blieb aus, was zeigt, dass BiP nicht nur NS1 vor Abbau schützt, sondern es auch auf dem sekretorischen Weg lenkt.
Was das für künftige antivirale Strategien bedeutet
Für Nicht‑Spezialisten lautet die Hauptaussage, dass diese gehirninfizierenden Viren stark auf die zellulären Proteinfaltungshelfer angewiesen sind, um ihre Außenhülle zu bauen und – bei einigen Arten – NS1 als sekretiertes Werkzeug auszusenden. Ein breit wirkender Chaperon‑Inhibitor wie YM‑1 kann daher die Produktion infektiöser Partikel mehrerer verwandter Viren gleichzeitig drastisch reduzieren, wobei seine starken Effekte vermutlich über ein einzelnes Chaperon hinausgehen und auch gesunde Zellen belasten können. Zielgerichtetere Ansätze, die sich beispielsweise darauf konzentrieren, wie BiP und Hsp70 bestimmte virale Klienten wie NS1 handhaben, könnten eines Tages helfen, Therapien zu entwickeln, die für Viren schwerer zu umgehen sind und gleichzeitig die normale Proteinfaltung im Wirt weitgehend schonen.
Zitation: Blank, L., Lorenz, C. & Steffen, I. Divergent roles of Hsp70 chaperones in orthoflavivirus protein secretion and virion formation. npj Viruses 4, 8 (2026). https://doi.org/10.1038/s44298-026-00175-8
Schlüsselwörter: orthoflavivirus, Hsp70‑Chaperon, Frühsommer‑Meningoenzephalitis‑Virus, West-Nil‑Virus, antivirale Wirkstoffziele