Clear Sky Science · de
Mechanistische Einblicke in die Auswirkungen pränataler Virusinfektionen auf die Immunität von Mutter und Nachkommen
Viren und Schwangerschaft: Warum es für Familien wichtig ist
Jedes Jahr finden Millionen von Schwangerschaften vor dem Hintergrund von Virusausbrüchen wie HIV, COVID-19 und Influenza statt. Selbst wenn Babys nicht direkt infiziert werden, zeigt die Forschung zunehmend, dass die Immunantwort der Mutter auf diese Viren langfristige Spuren in der Gesundheit des Kindes hinterlassen kann. Diese Übersicht fasst aktuelle Forschungsergebnisse zusammen und erklärt, wie häufige pränatale Virusinfektionen die Gebärmutterumgebung, die Plazenta und das sich entwickelnde Immunsystem subtil umgestalten können – mit Folgen, die von der Geburt bis ins Erwachsenenalter nachhallen können.
Drei verschiedene Viren, eine gemeinsame Herausforderung
Der Artikel konzentriert sich auf drei global bedeutsame Viren: HIV, SARS-CoV-2 (Erreger von COVID-19) und Influenza. Diese Infektionen unterscheiden sich in ihrer Übertragungsweise und in ihrer Persistenz – HIV verläuft chronisch, während COVID-19 und Influenza meist kurzzeitig sind. Dennoch können alle drei das empfindliche Gleichgewicht des maternalen Immunsystems während der Schwangerschaft stören. Klassisch sorgten Ärztinnen und Ärzte vor allem wegen der „vertikalen Transmission“, also der direkten Übertragung des Virus über die Plazenta auf den Fötus. Neue Befunde zeigen jedoch, dass schon ohne direkte fetale Infektion die Immunreaktion und Entzündungsprozesse der Mutter die Struktur der Plazenta verändern, den Blutfluss und die Nährstoffversorgung beeinträchtigen und die Entwicklung des Immun- und Nervensystems des Kindes beeinflussen können.
Wie die Plazenta zum Schlachtfeld wird
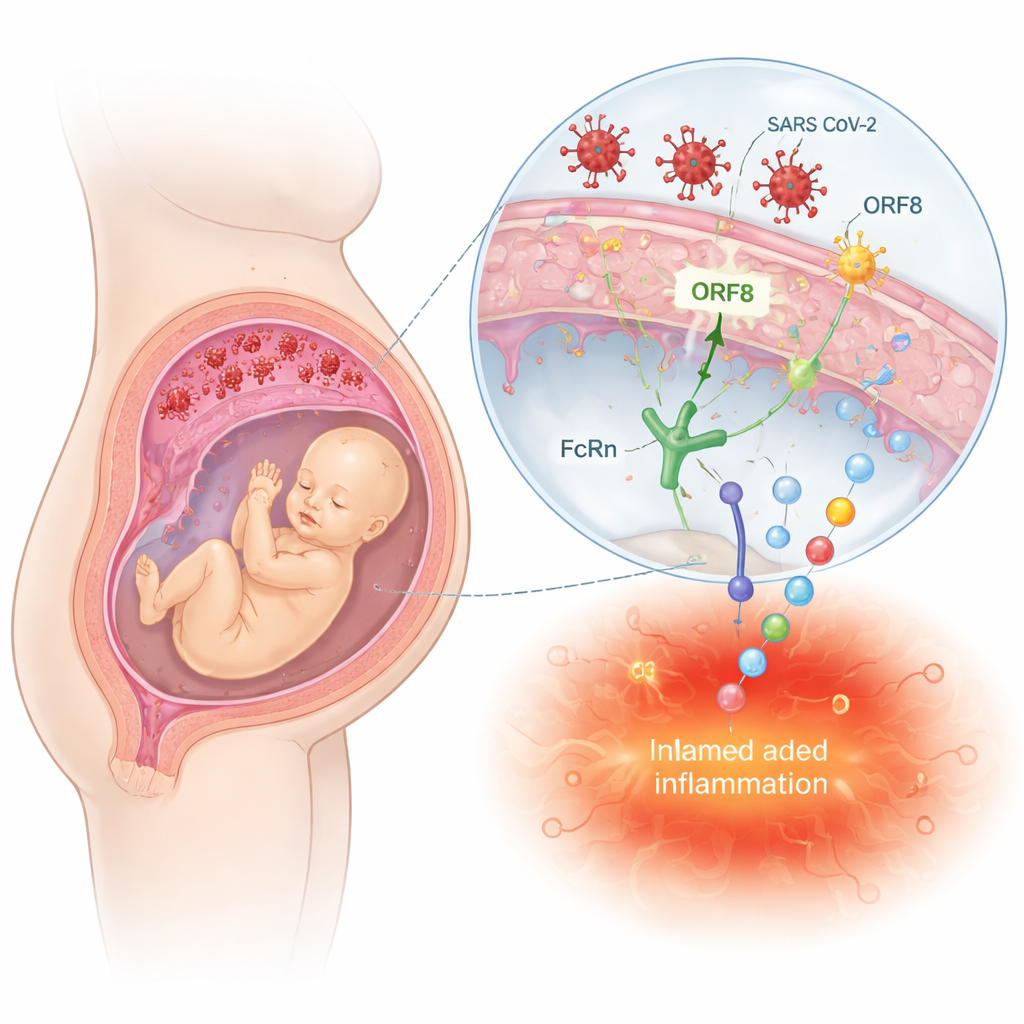
Die Plazenta dient zugleich als Schutzschild und als Brücke zwischen Mutter und Fötus. HIV kann diese Barriere überwinden, indem es Immunzellen und plazentäre Zellen infiziert oder indem es an Antikörpern andockt, die normalerweise schützende Faktoren zum Fötus transportieren. Im Gegensatz dazu erreichen SARS-CoV-2 und Influenza selten fetale Gewebe, können aber dennoch plazentäre Blutgefäße schädigen und entzündliche Kaskaden auslösen. Die Übersichtsarbeit beschreibt, wie virale Proteine – etwa die HIV-Proteine Tat und Nef oder ORF8 und das Spike-Protein von SARS-CoV-2 – mit Rezeptoren und Signalwegen in Plazenta- und Immunzellen interagieren. Solche Interaktionen können starke Entzündungsreaktionen auslösen, antivirale Abwehrmechanismen stören und die Hormonproduktion beeinträchtigen – Veränderungen, die möglicherweise keine offensichtlichen angeborenen Fehlbildungen verursachen, aber die fetale Entwicklung unauffällig umprogrammieren können.
Bleibende Spuren für Immun- und Gehirngesundheit des Kindes
Einer der zentralen Punkte in der Arbeit ist, dass eine pränatale Infektion das kindliche Immunsystem auf eine Weise „trainieren“ kann, die weit nach der Geburt anhält. Säuglinge, die im Mutterleib HIV ausgesetzt waren, aber uninfiziert geboren wurden, zeigen häufig veränderte Zahlen und Funktionen wichtiger Immunzellen, erhöhte Spiegel entzündlicher Moleküle und Unterschiede in ihrer Darmflora. Ähnliche Muster zeichnen sich bei Kindern ab, die SARS-CoV-2 ausgesetzt waren, und in Tierstudien bei Influenza. Diese frühen Verschiebungen stehen im Zusammenhang mit einem höheren Risiko für schwere Infektionen im Säuglingsalter, veränderten Impfantworten sowie möglichen Zunahmen von Allergien und immunvermittelten Erkrankungen. Für das Gehirn wurde in Human- und Tierstudien gezeigt, dass maternale Immunaktivierung – insbesondere Anstiege von Zytokinen wie IL-6 und IL-17 – mit späteren neuroentwicklungsbezogenen Problemen assoziiert ist, darunter Lernschwierigkeiten, Verhaltensauffälligkeiten und in einigen Fällen erhöhte Raten von Störungen wie Autismus und Schizophrenie.
Mütter und Babys schützen: Was getan werden kann
Die Übersicht behandelt auch, wie sich die klinische Versorgung weiterentwickelt, um diese Risiken zu mindern. Bei HIV haben eine frühe und anhaltende antiretrovirale Therapie der Mutter zusammen mit angepassten Medikamentenregimen für den Neugeborenen in vielen Bereichen direkte Übertragungsraten unter 1 % erreicht, wobei entzündungsbedingte Effekte weiterhin sorgfältige Nachsorge erfordern. Bei COVID-19 und Influenza ist die Impfung der Mutter ein wirkungsvolles Instrument: Geimpfte Mütter übertragen schützende Antikörper über die Plazenta, wodurch das Risiko sinkt, dass ihre Säuglinge in den ersten Lebensmonaten stationär behandelt werden müssen. Zu den aufkommenden Strategien gehören monoklonale Antikörper, niedermolekulare antivirale Wirkstoffe und Therapien, die übermäßige Entzündungen gezielt dämpfen, ohne die essenziellen Immunabwehrmechanismen zu unterdrücken – Ansätze, die speziell an Schwangeren getestet werden müssen.
Was dies für werdende Eltern und Kinder bedeutet
Insgesamt kommt der Artikel zu dem Schluss, dass pränatale Virusexposition nicht nur eine unmittelbare Bedrohung darstellt, sondern auch ein „Langzeitspiel“ für die Gesundheit ist. Selbst wenn Babys einer direkten Infektion entgehen, kann die Immunantwort der Mutter ihr Immunsystem, die Gehirnentwicklung und das Mikrobiom subtil prägen und beeinflussen, wie sie auf Infektionen reagieren und möglicherweise ihr Risiko für chronische Erkrankungen im späteren Leben. Das Verständnis dieser Mechanismen eröffnet Wege zu intelligenteren Impfstoffen, sichereren antiviralen Medikamenten während der Schwangerschaft und besserer langfristiger Überwachung exponierter Kinder. Für Familien und Kliniker gilt: den mütterlichen Gesundheitszustand während der Schwangerschaft zu schützen ist eine Investition in die lebenslange Gesundheit der nächsten Generation.
Zitation: Salem, G.M., Azamor, T., Familiar-Macedo, D. et al. Mechanistic insights into the impact of prenatal viral infections on maternal and offspring immunity. npj Viruses 4, 7 (2026). https://doi.org/10.1038/s44298-026-00174-9
Schlüsselwörter: pränatale Virusinfektion, maternale Immunaktivierung, plazentäre Entzündung, Immunität der Nachkommen, Neuroentwicklung