Clear Sky Science · de
STAT1-Signalgebung steuert den Cholesterinstoffwechsel in Epithelzellen und die RSV‑induzierte Syncytienbildung
Warum dieses Virus und Ihr Cholesterin zusammenhängen
Das respiratorische Syncytialvirus, kurz RSV, ist vor allem als Wintererreger bekannt, der Kinderstationen füllt und gebrechliche ältere Menschen gefährdet. Diese Studie zeigt, dass unsere Zellen RSV nicht nur mit Immunmolekülen bekämpfen – sie ordnen auch ihre Fette, insbesondere Cholesterin, neu, um das Virus in Schach zu halten. Zu verstehen, wie ein zentraler Immunumschalter namens STAT1 das Cholesterin kontrolliert, könnte neue Wege eröffnen, um Lungenschäden bei Menschen mit erhöhtem Risiko durch RSV zu begrenzen.
Ein Atemwegsvirus mit übergroßer Wirkung
RSV ist eine der Hauptursachen für schwere Atemwegsinfektionen wie Bronchiolitis und Pneumonie bei Säuglingen, älteren Erwachsenen und Menschen mit geschwächtem Immunsystem. Impfstoffe und langwirksame Antikörper helfen mittlerweile, Infektionen vorzubeugen, aber wenn jemand erkrankt ist, bleiben die Behandlungsmöglichkeiten begrenzt. Ein Kennzeichen schwerer RSV-Erkrankungen ist die Bildung von „Syncytien“ – große, verschmolzene Zellklumpen der Atemwege, die entstehen, wenn das Virus benachbarte Zellen zur Verschmelzung zwingt. Diese verschmolzenen Zellen können die empfindliche Auskleidung der Atemwege schädigen und die lokale Ausbreitung des Virus beschleunigen.
Ein Master‑Immunumschalter, der auch Lipide schützt
Die Forschenden konzentrierten sich auf STAT1, ein Protein, das durch Interferone aktiviert wird – die frühen Alarmsignale des Körpers bei Virusinfektionen. STAT1 ist dafür bekannt, Dutzende antivirale Gene hochzufahren, aber zunehmende Hinweise deuten darauf hin, dass es auch die Art und Weise verändert, wie Zellen mit Cholesterin umgehen. Cholesterin ist ein zentrales Bauelement von Zellmembranen und ein häufig genutztes Element, das viele Viren verwenden, um in Zellen einzudringen, sich zu vermehren und sie zu verlassen. Durch die Konstruktion von menschlichen, der Atemwegsoberfläche ähnlichen Zellen, die vollständig ohne STAT1 auskamen, und den Vergleich mit normalen Zellen, untersuchte das Team, wie dieser Immunumschalter das Cholesteringleichgewicht und folglich die RSV‑vermittelte Zellfusion beeinflusst.
Fehlt STAT1, häuft sich Cholesterin an und Zellen verschmelzen übermäßig
Mithilfe der Genom‑Editierung schalteten die Wissenschaftler beide Kopien des STAT1‑Gens in HEp‑2‑Epithelzellen aus. Die veränderten Zellen wuchsen mit normaler Geschwindigkeit, nahmen jedoch eine gestrecktere Form an, was darauf hindeutet, dass ihre Membranen verändert waren. Detaillierte Profile der Genaktivität zeigten umfassende Veränderungen in Signalwegen, die Produktion, Transport und Speicherung von Cholesterin steuern. Biochemische Tests bestätigten, dass STAT1‑defiziente Zellen selbst ohne Infektion etwa doppelt so viel freies Cholesterin ansammelten wie normale Zellen. Bei einer RSV‑Infektion beider Zelltypen waren die viralen Titer – die Menge an infektiösem Virus – überraschend ähnlich. Dramatisch verändert zeigte sich jedoch das Erscheinungsbild der Zellen: Kulturen ohne STAT1 bildeten deutlich größere und zahlreichere Syncytien als normale Zellen.
Das Hoch- und Runterregeln von Cholesterin verändert die Fusion, nicht die Virenmenge
Das Team manipulierte daraufhin direkt die Cholesterinwerte. Stoffe, die vorübergehend Cholesterin von der Zelloberfläche entfernten, oder Medikamente, die die Cholesterinsynthese und -verteilung reduzieren, verkleinerten alle die RSV‑induzierten Syncytien – insbesondere in STAT1‑defizienten Zellen. Ein natürlich vorkommendes Cholesterin‑Derivat, 25‑Hydroxycholesterol, war besonders wirksam: Es senkte das Membrancholesterin, störte die gleichmäßige Auflagerung des RSV‑Fusionsproteins (F‑Protein) auf der Zelloberfläche und schränkte die Infektion weitgehend auf einzelne Zellen statt auf großflächige verschmolzene Cluster ein. Dennoch blieb das Gesamtviruswachstum in der Kultur nahe dem Niveau unbehandelter Zellen, was darauf hinweist, dass die Cholesterinkontrolle hauptsächlich beeinflusst, wie destruktiv sich das Virus von Zelle zu Zelle ausbreitet.
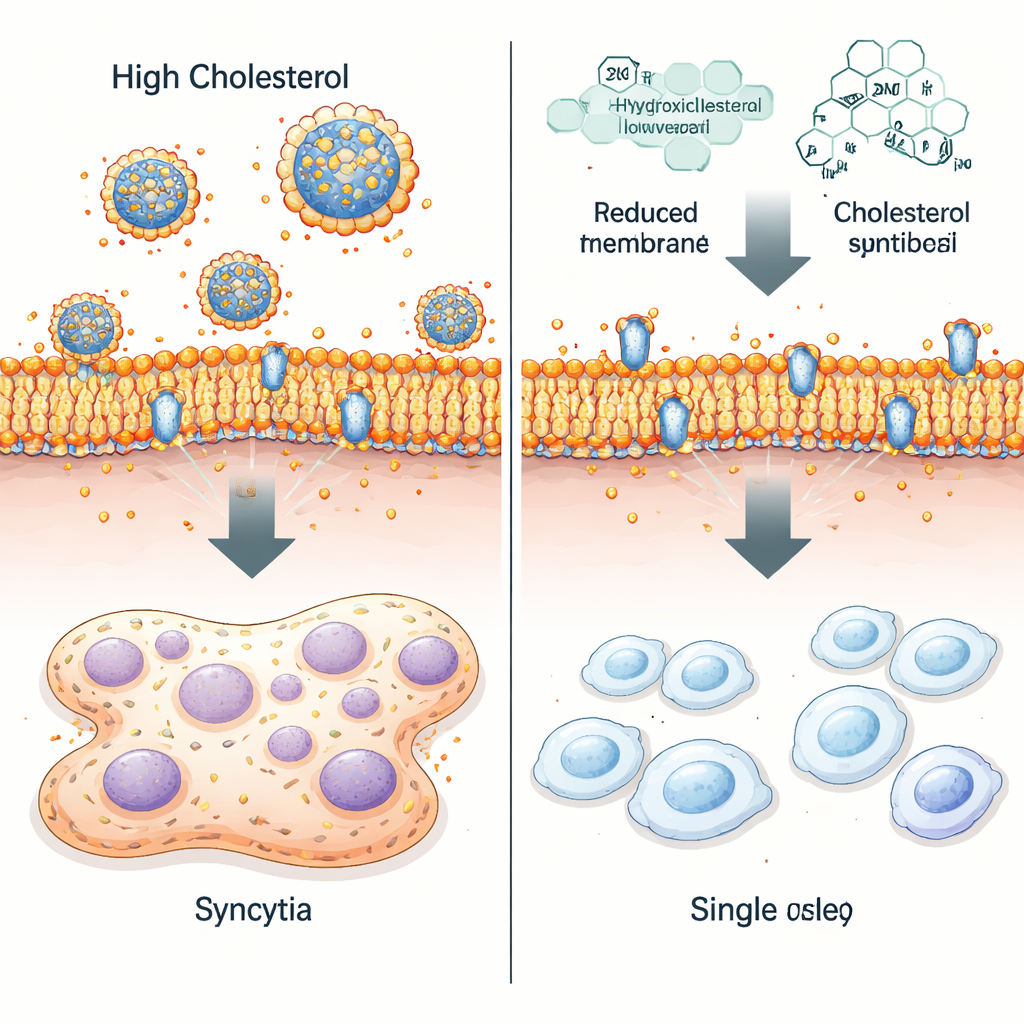
Warum das für gefährdete Patientengruppen wichtig sein könnte
Diese Ergebnisse skizzieren einen STAT1‑abhängigen „Immun‑metabolischen“ Weg, bei dem Interferon‑Signale helfen, RSV durch strengere Kontrolle von Cholesterin einzudämmen und übermäßige Zellfusion zu verhindern. Wenn die STAT1‑Signalgebung geschwächt ist – durch genetische Defekte, die unreife Immunität von Säuglingen oder altersbedingte Veränderungen bei älteren Menschen – wird die Cholesterinverarbeitung unsauber, Zellmembranen reichern sich an freiem Cholesterin an, und RSV kann aggressivere Syncytiumbildung fördern. Die Studie legt nahe, dass Medikamente, die zelluläres Cholesterin senken oder die Effekte von 25‑Hydroxycholesterol nachahmen, direkte Virostatika ergänzen könnten, insbesondere bei Menschen, die zu schweren RSV‑Verläufen neigen.
Das große Ganze: Cholesterin als Hebel für die Schwere von RSV
Für Nicht‑Fachleute lautet die Botschaft: Cholesterin in Lungenzellen ist nicht nur ein Thema für die Herzgesundheit; es entscheidet auch mit darüber, wie stark RSV die Atemwege schädigen kann. STAT1 wirkt wie ein Verkehrspolizist, der während einer Infektion das Cholesterin im Gleichgewicht hält, damit RSV weniger Gelegenheiten hat, Zellen miteinander zu verschmelzen. Versagt diese Kontrolle, häuft sich Cholesterin an und Syncytien breiten sich aus, was die Erkrankung potenziell verschlimmern kann. Da viele ältere Erwachsene bereits cholesterinsenkende Medikamente einnehmen, wirft die Arbeit die interessante Möglichkeit auf, dass das Management von Cholesterin eines Tages Teil des Schutzes gefährdeter Personen vor den gefährlichsten Formen der RSV‑Infektion sein könnte.
Zitation: Agac, A., Ludlow, M., Knittler, MC. et al. STAT1 signaling controls cholesterol metabolism in epithelial cells and RSV-induced syncytia formation. npj Viruses 4, 10 (2026). https://doi.org/10.1038/s44298-026-00173-w
Schlüsselwörter: respiratorisches Syncytialvirus, STAT1, Cholesterinstoffwechsel, Syncytiumbildung, antivirale Immunität