Clear Sky Science · de
Das lösliche G-Protein des respiratorischen Synzytialvirus fördert die Virenausbreitung über TLR2-vermittelte NLRP3-Priming und Pyroptose
Warum dieses Lungenvirus für alle wichtig ist
Der respiratorische Synzytialvirus, kurz RSV, ist vor allem als Wintergefahr für Säuglinge bekannt, bringt aber auch viele ältere Menschen und Personen mit geschwächtem Immunsystem ins Krankenhaus. Selbst mit neuen Impfstoffen und schützenden Antikörpern infiziert RSV Menschen immer wieder neu und kann schwere Lungenschäden verursachen. In dieser Studie wird ein wenig bekanntes Virusprotein untersucht, eine lösliche Form des RSV-G-Proteins, und aufgezeigt, wie es Lungenzellen stillschweigend auf explosive Entzündungen vorbereiten und das Virus dabei unterstützen kann, sich effizienter in den Atemwegen auszubreiten.
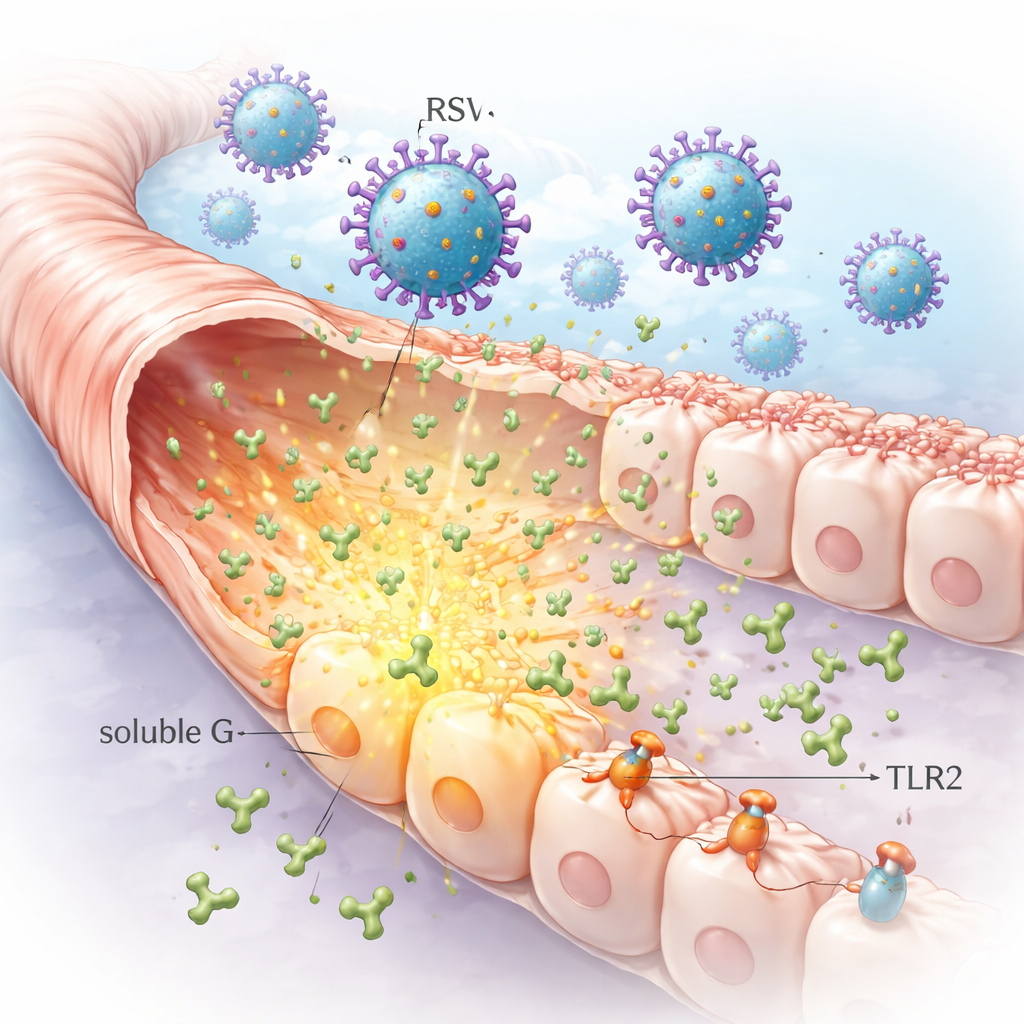
Ein sezerniertes Virusprotein, das der Infektion vorausreist
RSV besitzt ein Haftprotein namens G auf seiner Oberfläche, das ihm hilft, sich an Atemwegszellen anzuheften. Ungewöhnlich ist, dass infizierte Zellen auch große Mengen einer frei zirkulierenden Version dieses Proteins freisetzen, bekannt als lösliches G. Die Forschenden zeigten, dass infizierte Lungenzellen im Labor sehr hohe Mengen löslichen G in ihre Umgebung abgeben können. Da diese Form vom ursprünglichen Infektionsort wegdiffundieren kann, erreicht sie benachbarte Zellen, die noch nicht infiziert sind, und bereitet so eine breitere Veränderung der Lungenschleimhaut vor, als das Virus allein verursachen würde.
Lösliches G als doppelt wirkender Schlüssel für Zelloberflächen
Durch die Kombination von Mikroskopie, biochemischen Pull-down-Tests und Enzymbehandlungen kartierte das Team, wie sich lösliches G an Zellen anlagert. Sie fanden heraus, dass es sich an Zuckerketten namens Glykosaminoglykane binden kann sowie an einen bekannten RSV-Rezeptor namens CX3CR1. Entscheidenderweise bindet lösliches G auch an ein Muster-erkennendes Molekül auf Immun- und Atemwegszellen namens TLR2. Ein winziges Motiv im G-Protein, bekannt als CX3C, erwies sich als wichtig für die starke Bindung an CX3CR1 und für die robuste Rekrutierung von TLR2. Das bedeutet, dass lösliches G zunächst locker an der Zelloberfläche aufgefangen werden kann und anschließend spezifischere Rezeptoren anspricht, die steuern, wie Zellen auf Gefahren reagieren.
Priming von Lungenzellen für eine entzündliche Form des Zelltods
Die Bindung von TLR2 durch lösliches G erwies sich als alles andere als harmlos. In Reporter-Immunzellen und humanen Lungenzelllinien aktivierte lösliches G den MyD88–NF-κB-Signalweg downstream von TLR2, was zur Freisetzung entzündlicher Botenstoffe wie IL-6 und IL-8 führte. Gleichzeitig förderte es die Produktion von Komponenten eines molekularen "Alarmsystems" namens NLRP3-Inflammasom und von Enzymen, die reaktive Moleküle wie Stickstoffmonoxid und Sauerstoffradikale erzeugen. Für sich genommen verursachten diese Veränderungen nur geringe Schäden. Wurden die vorgeprimten Zellen jedoch später mit RSV infiziert, löste der zweite Treffer den vollständigen Zusammenbau des Inflammasoms aus, die Aktivierung des Enzyms Caspase‑1, die Bildung von Poren in der Zellmembran und eine feurige Form des Zelltods, bekannt als Pyroptose. Dieser Prozess riss Löcher in die Zellen, ließ entzündliche Inhalte auslaufen und ging mit höheren Mengen infektiöser Viren im Kulturmedium einher.
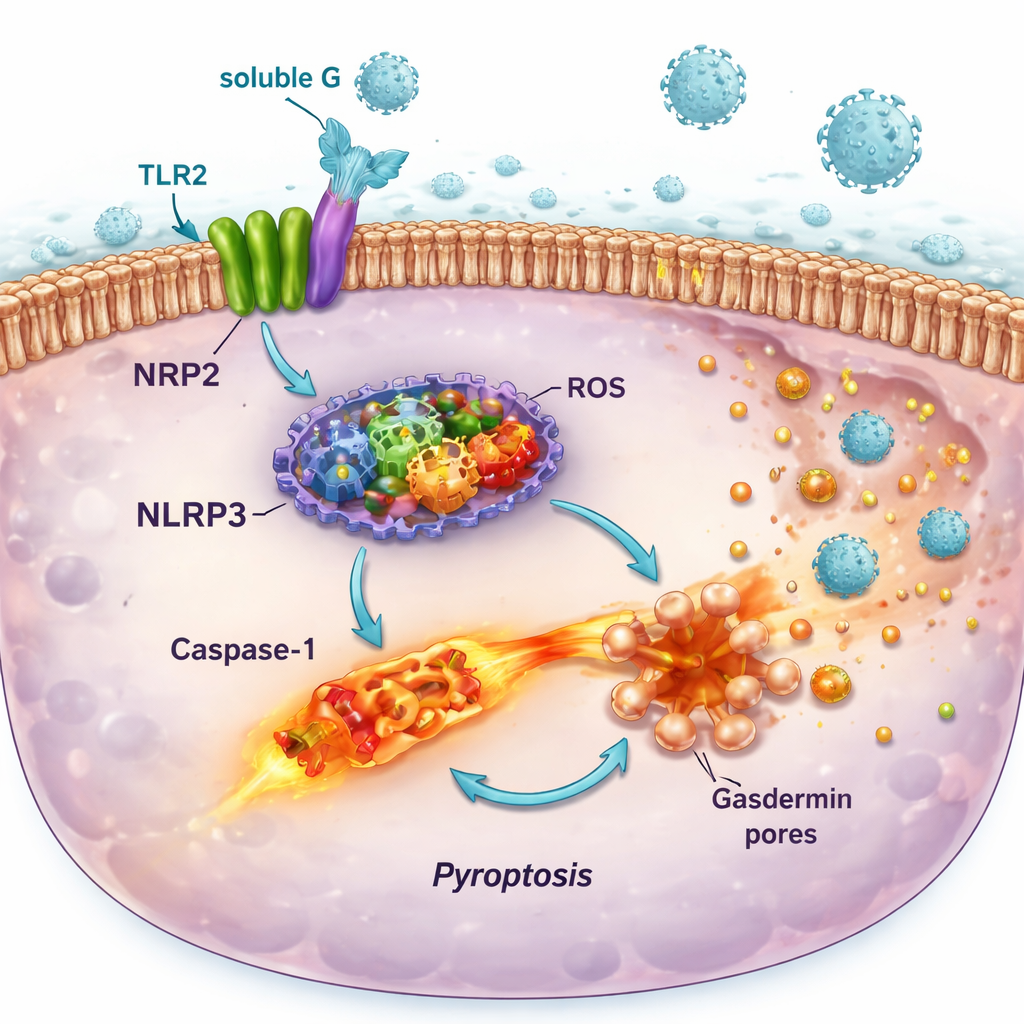
Wie diese Kettenreaktion die Lungenerkrankung verschlechtern kann
Die pro-death-Wirkung von löslichem G war am stärksten in respiratorischen Epithelzellen—den Zellen, die RSV bevorzugt infiziert—und hing vom NLRP3-Inflammasom ab, da ein spezifischer NLRP3-Inhibitor die Zellvitalität weitgehend rettete. Im Gegensatz dazu durchliefen bestimmte Immunzellen, die reich an TLR2, aber arm an CX3CR1 waren, unter denselben Bedingungen keinen starken lytischen Zelltod. Dieses Muster legt nahe, dass RSV lösliches G nutzt, um gezielt die schützende Auskleidung der Atemwege zu schwächen und zu zerstören, während einige Immunzellen erhalten bleiben, die weiterhin Signale produzieren können. Das Ergebnis ist eine Lungenumgebung mit mehr Entzündung, mehr Zelltrümmern und mehr Gelegenheiten für neue Viruspartikel, zu entkommen und benachbarte Zellen zu infizieren.
Was das für künftige Behandlungen bedeutet
Für Nicht-Spezialisten lautet die Kernbotschaft, dass RSV nicht allein auf direkte Schäden durch virale Invasion angewiesen ist. Durch die Freisetzung großer Mengen löslichen G-Proteins kann es nahegelegene Zellen über TLR2 "aufweichen", sodass sie eher auf entzündliche Weise sterben und Virus freisetzen. Diese Arbeit identifiziert mehrere Schritte in dieser Kette—das lösliche G selbst, sein CX3C-Motiv, TLR2 und das NLRP3-Inflammasom—als potenzielle Wirkstoffziele. Prinzipiell könnten Therapien, die die Wechselwirkung zwischen löslichem G und TLR2 blockieren oder die NLRP3-Aktivität dämpfen, sowohl Lungenverletzungen als auch die Virusausbreitung reduzieren. Solche Ansätze könnten eines Tages die bestehenden RSV-Impfstoffe und Antikörper ergänzen und einen besseren Schutz für die Jüngsten und Schwächsten bieten.
Zitation: Meineke, R., Agac, A., Knittler, MC. et al. The soluble G protein of respiratory syncytial virus promotes viral dissemination via TLR2-mediated NLRP3 priming and pyroptosis. npj Viruses 4, 6 (2026). https://doi.org/10.1038/s44298-026-00172-x
Schlüsselwörter: respiratorischer Synzytialvirus, lösliches G-Protein, TLR2-Inflammasom, Pyroptose, Lungenentzündung