Clear Sky Science · de
Menopausale Hormonersatztherapie und Risiko neuropsychiatrischer Erkrankungen: eine Mendelsche Randomisierungsstudie zu Arzneimittelzielen
Warum diese Forschung wichtig ist
Viele Frauen fragen sich, ob die Einnahme von Hormonen rund um die Menopause ihr Gehirn schützt oder es einem erhöhten Risiko für Probleme wie Gedächtnisverlust, Depression oder Angst aussetzt. Auch Ärztinnen und Ärzte sind uneins, weil frühere Studien widersprüchliche Ergebnisse lieferten. Dieser Artikel verwendet einen genetikorientierten Ansatz, ähnlich im Geist einer langfristigen randomisierten Studie, um eine einfache Frage zu stellen: Wenn die Östrogenrezeptoren im Gehirn so beeinflusst werden, wie es die menopausale Hormonersatztherapie tun könnte, ändert sich dadurch das Risiko für Alzheimer oder häufige psychische Erkrankungen?
Das Rätsel um Hormone und das Gehirn
Frauen sind häufiger betroffen als Männer von Depressionen, Angststörungen und Alzheimer. Eine führende Idee besagt, dass Östrogen, ein zentrales weibliches Sexualhormon, das Gehirn lebenslang mitgestaltet und es möglicherweise schützt — bis die Spiegel mittleren Alters schwanken oder sinken. Während der menopausalen Übergangsphase nutzen viele Frauen eine Hormonersatztherapie (HRT bzw. MHT), um Symptome wie Hitzewallungen und Schlafprobleme zu lindern. Studien dazu, ob MHT der Gehirngesundheit nutzt oder schadet, sind jedoch uneinheitlich: Einige fanden ein erhöhtes Demenzrisiko, andere deuteten auf Schutz hin, und viele zeigten keinen klaren Effekt. Diese Inkonsistenzen können aus kurzen Studiendauern, unterschiedlichen Arzneiformulierungen und daraus resultieren, dass Frauen mit stärkeren Beschwerden eher Hormone verschrieben bekommen.
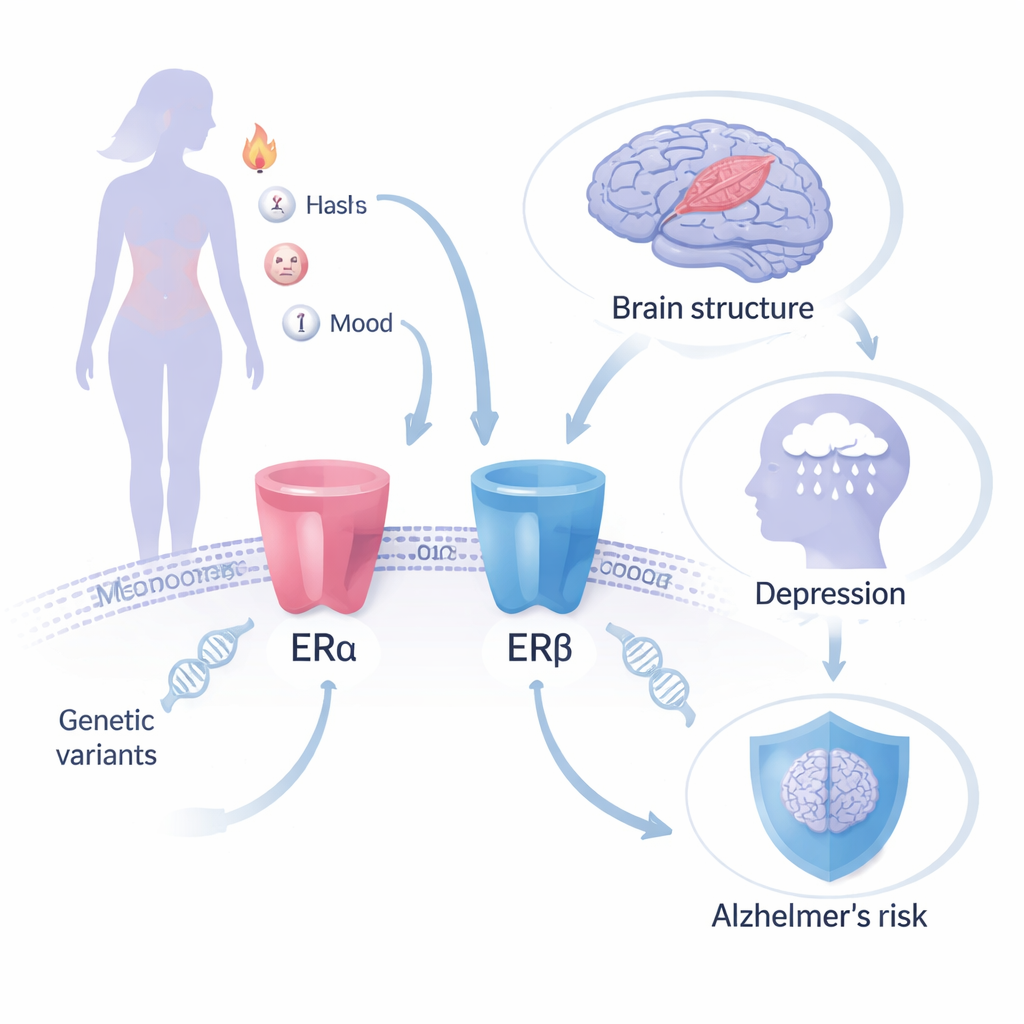
Gene als natürliches Experiment nutzen
Anstatt Frauen zu verfolgen, die Hormontabletten einnehmen, wandten sich die Forschenden der Mendelschen Randomisierung zu — einer Methode, die natürlich vorkommende genetische Unterschiede als Stellvertreter für eine lebenslange, zufällig zugewiesene „Behandlung“ nutzt. Sie konzentrierten sich auf zwei Proteine im Körper, die Östrogenrezeptoren ERα und ERβ, die durch MHT aktiviert werden sollen. Bestimmte genetische Varianten in den Genen, die diese Rezeptoren kodieren (ESR1 und ESR2), haben bekannte Effekte auf „downstream“-Merkmale, die sich ändern, wenn Östrogen wirkt, etwa die Knochenmineraldichte, ein Bluteiweiß, das Sexualhormone transportiert, und Hämoglobinwerte. Indem sie verfolgten, wie diese an Rezeptoren gebundenen Varianten mit großen genetischen Datensätzen zu Alzheimer, Gehirnstruktur, Depression und Angst in Zusammenhang stehen, konnte das Team abschätzen, wie das gezielte Beeinflussen jedes Rezeptors langfristige Risiken für Hirn- und psychische Gesundheit verändern könnte.
Was die genetischen Daten zeigten
Die Autorinnen und Autoren konstruierten drei genetische Instrumente: zwei, die ERα-Aktivität erfassen (über Varianten, die mit Knochenmineraldichte bzw. mit Sexualhormon-bindendem Globulin verbunden sind) und eines, das ERβ-Aktivität erfasst (über eine Variante, die mit Hämoglobin verbunden ist). Diese kombinierten sie mit einigen der größten verfügbaren genomweiten Assoziationsstudien zu Alzheimer, MRT-Messungen des Gehirns (Gesamtgraue Substanz, Hippocampusvolumen und „Flecken“ in der weißen Substanz, die mit Alterung assoziiert sind), Depression und Angst. Insgesamt fanden sie keinen überzeugenden Hinweis darauf, dass genetisch simulierte Veränderungen eines der beiden Östrogenrezeptoren das Alzheimer-Risiko oder diese Gehirnstrukturmaße in bedeutsamer Weise verändern. Einige schwache Signale für Veränderungen in der grauen Substanz oder im Hippocampusvolumen überlebten die statistische Korrektur nicht, was darauf hindeutet, dass sie eher Zufall als ein echtes biologisches Signal sein könnten.
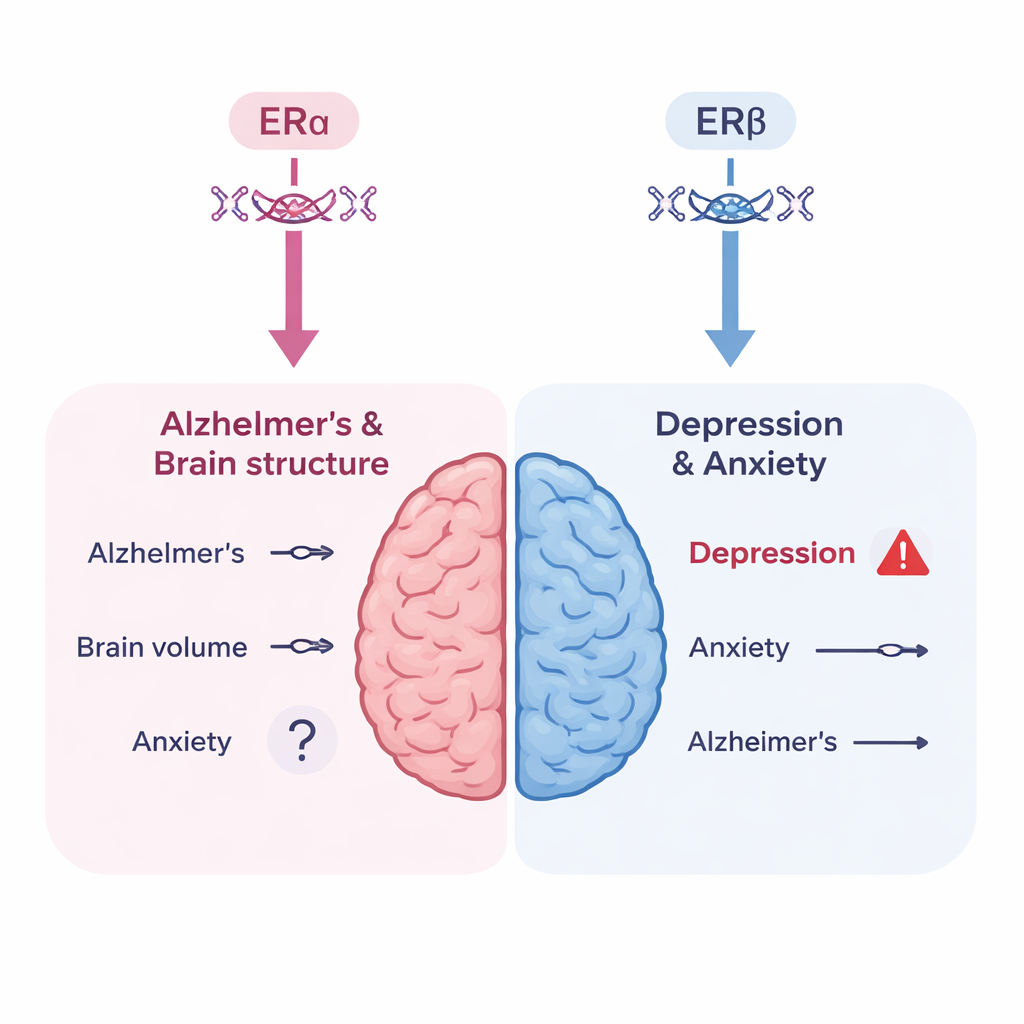
Ein Warnsignal für Depressionsrisiko
Die Geschichte war für die Stimmungslage anders. Als die Forschenden die ERβ-Aktivität betrachteten, erfasst durch den hämoglobinbasierten genetischen Proxy, beobachteten sie einen statistisch robusten Zusammenhang mit einem höheren Depressionsrisiko. Dieses Ergebnis passt zu dem, was über die Regionen bekannt ist, in denen ERβ im Gehirn besonders aktiv ist — Bereiche wie Hippocampus und Thalamus, die stark an der Stimmungsregulation beteiligt sind. Die Autorinnen und Autoren warnen jedoch, dass der Hämoglobin-Proxy unvollkommen ist: Niedrige Hämoglobinwerte selbst können zu Müdigkeit und gedrückter Stimmung beitragen und damit das Bild verwischen. Sie fanden keine starken genetischen Hinweise dafür, dass ERα-Aktivität allein das Depressionsrisiko erhöht, und nur einen suggestiven, nicht eindeutigen Hinweis darauf, dass ERα mit Angst in Zusammenhang stehen könnte. Wichtig ist, dass genetische Effekte, die beständig von Geburt an wirken, nicht identisch sind mit dem Beginn einer Hormontherapie in der Lebensmitte; diese Ergebnisse sollten daher nicht als direkte Vorhersage für ein bestimmtes MHT-Regime gelesen werden.
Was das für Frauen und ihre Ärztinnen und Ärzte bedeutet
Für den Alltag übersetzt deutet diese Studie darauf hin, dass das Ansprechen der Östrogenrezeptoren in einer Weise, die MHT ähnelt, nicht klar das Lebenszeitrisiko für Alzheimer erhöht oder verringert und keine großen Veränderungen der Gehirnstruktur bewirkt — zumindest bei Personen europäischer Abstammung. Zugleich unterstreicht das Ergebnis zu ERβ und Depression, dass hormonsensible Gehirnkreise mit der Stimmung verknüpft sind und dass verschiedene Östrogenrezeptoren unterschiedliche Implikationen für die psychische Gesundheit haben können. Die Arbeit ersetzt keine klinischen Studien, bietet aber einen kraftvollen genetischen "Realitätscheck", der helfen kann, zukünftige Hormontherapien zu verfeinern und die Forschung an sichereren, besser zugeschnittenen Behandlungen für Frauen in der Menopause zu leiten.
Zitation: Schindler, L.S., Gill, D., Oppenheimer, H. et al. Menopausal hormone therapy and risk of neuropsychiatric disease: a drug target Mendelian randomisation study. npj Womens Health 4, 10 (2026). https://doi.org/10.1038/s44294-026-00130-1
Schlüsselwörter: menopausale Hormonersatztherapie, Östrogenrezeptoren, Alzheimer-Krankheit, Depressionsrisiko, Mendelsche Randomisierung