Clear Sky Science · de
Ein umfassendes genomisches Rahmenwerk zur Identifizierung von Genen, die zu homologe‑Rekombinations‑Reparatur‑defizienten Brust‑ oder Eierstockkrebsen prädisponieren
Warum einige Familien ein höheres Krebsrisiko haben
Viele Frauen mit Brust‑ oder Eierstockkrebs haben eine ausgeprägte Familienanamnese der Erkrankung, dennoch liefert die genetische Diagnostik häufig keine klare Erklärung. Diese Lücke, oft als „fehlende Erblichkeit“ bezeichnet, lässt Familien ohne Antworten zurück und kann den Zugang zu maßgeschneiderter Überwachung oder Therapien wie zielgerichteten Medikamenten einschränken. Diese Studie hatte zum Ziel, eine neue, leistungsfähigere Methode zu entwickeln, um in unserem Erbgut nach versteckten Krebsrisikogenen zu suchen, indem verschiedene genomische und klinische Informationen kombiniert werden, statt jede isoliert zu betrachten. 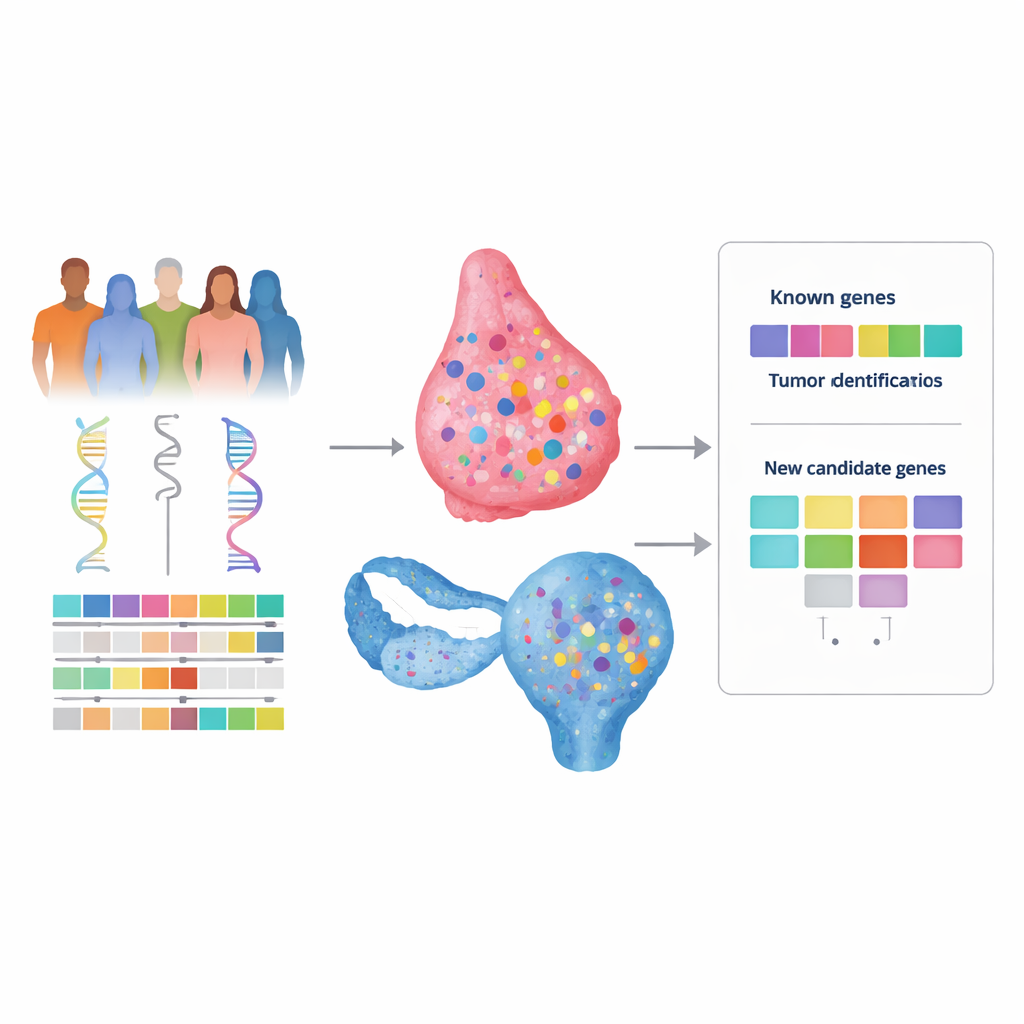
Suche nach dem Fingerabdruck fehlerhafter DNA‑Reparatur
Die Forscher konzentrierten sich auf eine bestimmte Form der DNA‑Schadensbehebung, die als homologe Rekombinationsreparatur bekannt ist und normalerweise gefährliche Brüche im genetischen Material repariert. Scheitert dieses Reparatursystem, sammeln sich in den Zellen ein charakteristisches „mutationales Signaturmuster“ an – ein typisches Muster von Veränderungen in der Tumor‑DNA, das wie ein molekularer Fingerabdruck wirkt. Dieses Muster ist besonders häufig in bestimmten schwer zu behandelnden Brust‑ und Eierstockkrebserkrankungen. Das Team nahm an, dass ein Tumor, der diesen Fingerabdruck zeigt, vermutlich beide funktionsfähigen Kopien eines DNA‑Reparaturgens verloren hat, bekannt oder unbekannt, und dass sich dies auf vererbte Veränderungen in diesem Gen zurückführen lässt.
Aufbau eines kombinierten genetischen und klinischen Rahmens
Um diese Idee zu testen, analysierten die Autoren DNA von Hunderten Brust‑ und Eierstockkrebspatientinnen aus The Cancer Genome Atlas, das sowohl Blut‑ (vererbt) als auch Tumor‑(erworben) genetische Daten sowie klinische Informationen bereitstellt. Sie durchsuchten das gesamte Exom – den protein‑kodierenden Teil des Genoms – nach seltenen vererbten Varianten, die schädlich erscheinen, und die im Tumor außerdem einen „zweiten Treffer“ aufwiesen, etwa den Verlust der verbleibenden gesunden Kopie. Für jedes Gen prüften sie anschließend, ob solche Zwei‑Schlag‑Ereignisse in Tumoren mit der Reparatur‑Defekt‑Signatur häufiger vorkommen als in solchen ohne diese Signatur. Entscheidend war, dass sie sich nicht auf ein vorgegebenes Genpanel beschränkten und so unerwartete Kandidaten zum Vorschein kommen konnten.
Prüfung der Methode und Finden neuer Verdächtiger
Als Plausibilitätsprüfung hob das Rahmenwerk die bereits gut bekannten Brust‑ und Eierstockkrebsgene BRCA1 und BRCA2 deutlich als stark mit der Reparatur‑Defekt‑Signatur assoziiert in beiden Krebsarten hervor, was bestätigt, dass der Ansatz wie erwartet funktioniert. Beim Brustkrebs wurde außerdem ein zusätzliches Gen, THBS4, markiert, und mögliche Rollen für die Gene KIF13B und TESPA1 angedeutet. Eine detaillierte Fall‑für‑Fall‑Überprüfung zeigte jedoch, dass Veränderungen in THBS4 häufig zusammen mit anderen, etablierteren reparaturbezogenen Ereignissen auftraten, wodurch seine Rolle als treibender Faktor weniger überzeugend wirkte. 
Fokussieren auf unerklärte Hochrisiko‑Tumoren
Um über rein statistische Analysen hinauszugehen, integrierten die Forschenden klinische Details wie Tumorsubtyp, Alter bei Diagnosestellung und Abstammung. Sie konzentrierten sich auf Patientinnen, deren Tumoren klar die Reparatur‑Defekt‑Signatur zeigten und die zu klinischen Gruppen gehörten, die bereits mit dieser Biologie in Verbindung gebracht werden – basal‑artige Brustkrebse und hochgradig seröse Eierstockkrebse –, aber keine bekannten BRCA‑artigen Ereignisse aufwiesen. Bei diesen Patientinnen suchten sie erneut nach vererbten Varianten mit zweiten Treffern, dieses Mal innerhalb einer breiten, kuratierten Liste von Krebs‑ und DNA‑Reparaturgenen. Diese „klinisch‑genomische“ Sichtweise rückte mehrere Gene in den Fokus, die an der Reparatur von DNA‑Doppelstrangbrüchen und dem eng verwandten Fanconi‑Anämie‑Weg beteiligt sind, darunter RAD51B, RAD54B, RAD54L, FANCD2 und andere, als plausible neue Mitwirkende an vererbtem Risiko.
Was das für Patientinnen und zukünftige Forschung bedeutet
Die Studie erhebt nicht den Anspruch, neue Krebsrisikogene endgültig bewiesen zu haben; die Zahl betroffener Patientinnen für jedes Kandidatengen ist weiterhin klein, und größere, diversere Kohorten werden nötig sein, um ihre Rollen zu bestätigen. Stattdessen liefern die Autorinnen und Autoren eine wiederverwendbare Blaupause: einen Weg, vererbte und Tumor‑DNA, charakteristische mutationelle Fingerabdrücke und klinische Merkmale zu kombinieren, um systematisch Gene zu priorisieren, die der unerklärten familiären Krebserkrankung zugrunde liegen könnten. Mit der Zeit könnte die Anwendung dieses Rahmens auf größere Datensätze und andere Krebsarten die Lücke der „fehlenden Erblichkeit“ verkleinern, genetische Testpanels verfeinern und mehr Patientinnen helfen, ihr persönliches Risiko sowie Optionen zur Prävention und gezielten Therapie besser zu verstehen.
Zitation: Camacho-Valenzuela, J., Matis, T., Roca, C. et al. A comprehensive genomic framework for identifying genes predisposing to homologous recombination repair-deficient breast or ovarian cancer. BJC Rep 4, 15 (2026). https://doi.org/10.1038/s44276-026-00218-w
Schlüsselwörter: homologe Rekombinations‑Defizienz, Genetik von Brustkrebs, Eierstockkrebs, DNA‑Reparaturgene, Krebsanfälligkeit