Clear Sky Science · de
STAR (stroma-tumor AI risk) Bewertung: Verbindung des AI-abgeleiteten Tumor-Stroma-Verhältnisses mit dem Überleben von Patientinnen bietet prognostischen Mehrwert über KELIM hinaus bei epithelialem Ovarialkarzinom
Warum die „Nachbarschaft“ um einen Tumor wichtig ist
Wenn wir an Krebs denken, stellen wir uns meist eine Masse abweichender Zellen vor. Tumoren existieren jedoch in einer belebten Nachbarschaft aus Stützgewebe, Blutgefäßen und Immunzellen, dem sogenannten Stroma. Diese Studie stellt eine einfache, aber kraftvolle Frage: Können wir das Verhältnis zwischen Tumorzellen und diesem umliegenden Gewebe — gemessen von künstlicher Intelligenz (KI) auf routinemäßigen Mikroskoppräparaten — nutzen, um vorherzusagen, welche Patientinnen mit Ovarialkarzinom eher bessere oder schlechtere Prognosen haben werden, noch bevor die Behandlung beginnt?
Eine neue Art, Standard-Biopsiepräparate zu lesen
Bei Frauen mit epithelialem Ovarialkarzinom werden typischerweise Gewebeproben bei Operation oder Biopsie entnommen. Diese Proben werden gefärbt und in jedem Krankenhaus am Mikroskop untersucht. Die Forschenden konzentrierten sich auf ein Merkmal, das Tumor–Stroma-Proportion (TSP) genannt wird: wie viel des Bildes aus Stützgewebe im Vergleich zu Krebszellen besteht. In früheren Arbeiten schätzten Pathologen diese Proportion „nach Auge“ und fanden, dass stroma-reiche Tumoren oft aggressiver sind und standardmäßiger platinhaltiger Chemotherapie widerstehen. In der aktuellen Studie nutzte das Team ein Deep‑Learning-KI-System, um TSP automatisiert auf digitalisierten Schnitten zu messen, mit dem Ziel, eine manuelle, teilweise subjektive Aufgabe in eine schnelle und reproduzierbare Messung zu verwandeln, die bereits bei der Diagnosestellung verfügbar ist.
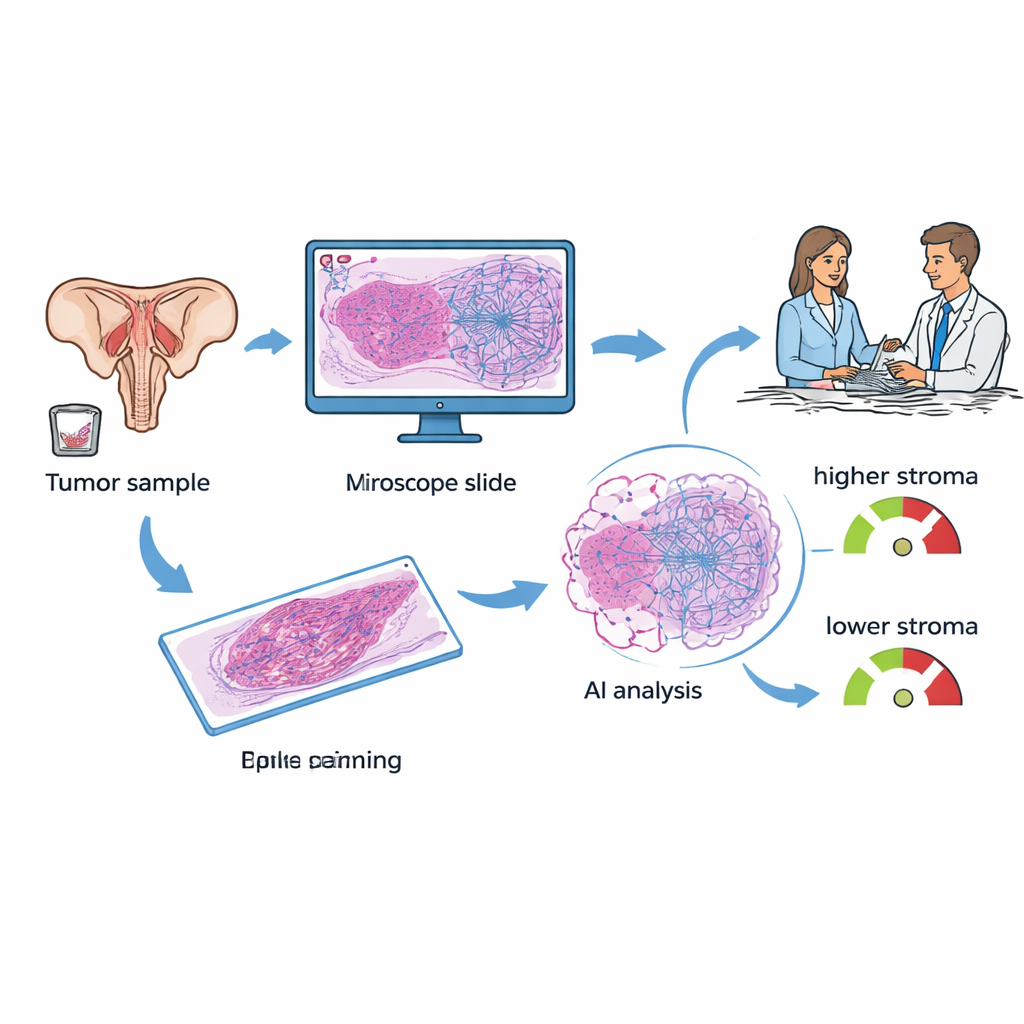
Vergleich der KI-Gewebeanalyse mit einem blutbasierten Score
Ein weithin diskutiertes Instrument beim Ovarialkarzinom ist heute KELIM, ein Score, der darauf basiert, wie schnell ein Blutmarker namens CA‑125 in den ersten 100 Tagen der Chemotherapie abfällt. KELIM ist kostengünstig und hilfreich, kann aber erst nach mehreren Wochen Behandlung berechnet werden, und nicht alle Patientinnen haben früh genug Blutkontrollen, um den Score zu generieren. Die Forschenden sammelten Daten von 89 Frauen, die an einem einzigen Krebszentrum behandelt wurden und sowohl Gewebeschnitte als auch mindestens drei CA‑125‑Messungen hatten. Sie berechneten für jede Patientin KELIM, ließen einen Pathologen Tumorregionen auf den Schnitten markieren und ließen dann das KI‑Modell die TSP schätzen, wobei jede Probe als „stroma‑niedrig“ (weniger als 50% Stroma) oder „stroma‑hoch“ (50% oder mehr) klassifiziert wurde.
Die KI entspricht Expertinnen und Experten und markiert Tumoren mit höherem Risiko
Die Einschätzung der KI stimmte eng mit der erfahrener Pathologen überein: in 94 % der Fälle war die automatisierte TSP‑Klassifikation mit der manuellen übereinstimmend, ein Maß an Übereinstimmung, das als ausgezeichnet gilt. Betrachtete man die Patientinnenergebnisse, zeigte sich, dass Frauen mit stroma‑hohen Tumoren nach KI deutlich schlechteres Gesamtüberleben hatten als solche mit stroma‑niedrigen Tumoren. Statistisch gesehen verdoppelte ein hoher TSP beinahe das Sterberisiko während der Nachbeobachtung, und dieser Effekt blieb bestehen, selbst nachdem der KELIM‑Score berücksichtigt worden war. Im Gegensatz dazu war in dieser realen Patientinnengruppe KELIM mit der Resistenz gegen Platin‑Medikamente verknüpft, zeigte aber keine klare Verbindung zur Gesamtüberlebenszeit.
Was das für Behandlungsentscheidungen bedeuten könnte
Da TSP aus routinemäßigen Schnitten gemessen werden kann, die zum Zeitpunkt der Diagnose entnommen werden, bietet KI‑basiertes TSP eine Möglichkeit, das Risiko vor Beginn der Chemotherapie einzuschätzen — potenziell Monate früher als KELIM. Ein hoher TSP‑Befund könnte Klinikern signalisieren, dass ein Tumor wahrscheinlicher aggressiv und schwerer zu behandeln ist, was engmaschigere Überwachung, frühere Erwägung zusätzlicher Therapien oder andere chirurgische Strategien nach sich ziehen könnte. Die Methode ist zudem relativ kostengünstig: Sie nutzt vorhandene pathologische Bilder und ein Softwaremodell statt neuer Labortests. Die Autorinnen und Autoren argumentieren, dass automatisierte TSP neben anderen Markern, wie genetischen Tests und CA‑125‑Verläufen, eingesetzt werden könnte, um die Prognose zu verfeinern, ohne Patientinnen oder Pathologieteams erheblich zu belasten.
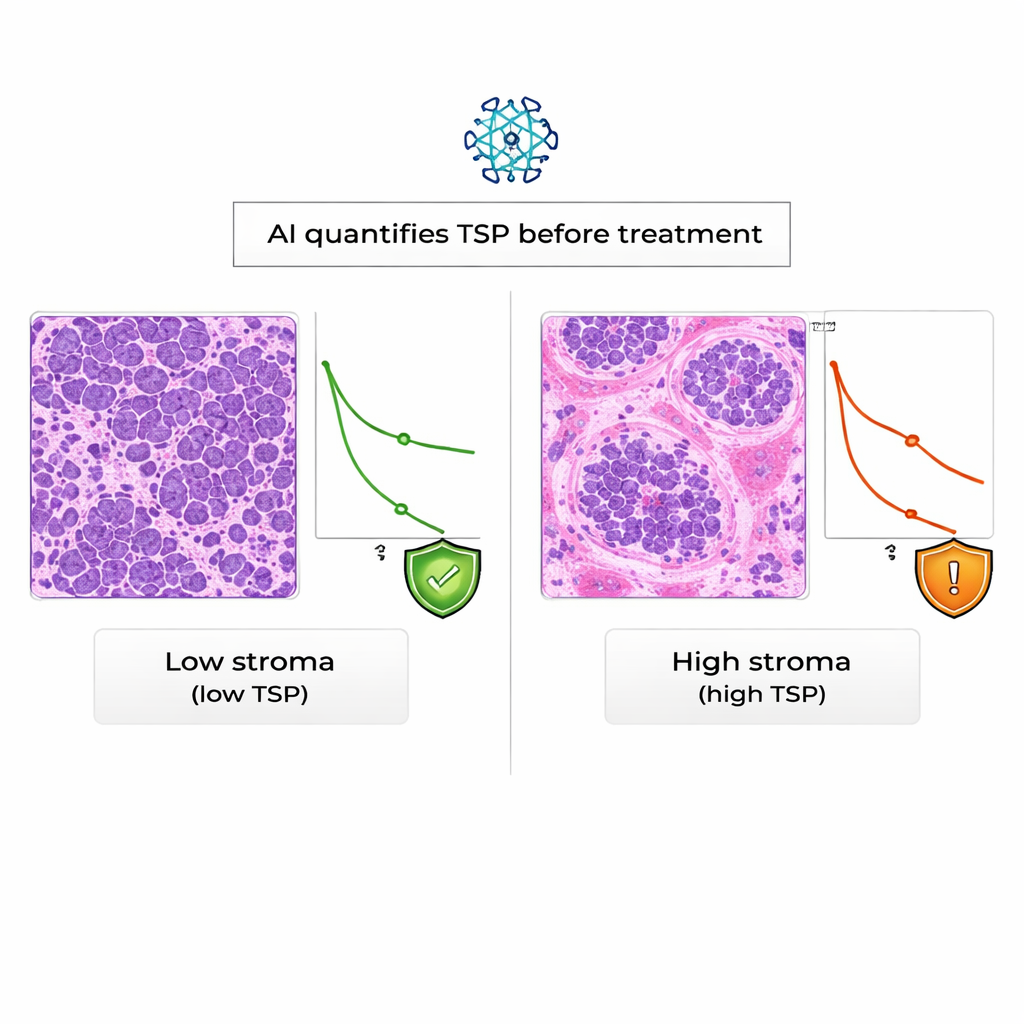
Blick nach vorn: klügere, frühere Orientierung für Patientinnen
Für Nichtfachleute ist die Kernbotschaft, dass nicht alle Ovarialkarzinome gleich sind und das umgebende Stützgewebe wichtige Hinweise darauf liefert, wie sich die Erkrankung verhalten wird. Diese Studie zeigt, dass KI diese Hinweise zuverlässig auf Standard‑Biopsieschnitten lesen kann und dass ein stroma‑reicher Tumor tendenziell mit schlechterem Überleben verbunden ist — unabhängig von bestehenden blutbasierten Scores. Obwohl vor einer routinemäßigen Anwendung größere und diversere Studien notwendig sind, birgt das von KI abgeleitete TSP das Potenzial, als Frühwarnzeichen zu dienen, das Ärzten hilft, Behandlungspläne besser anzupassen und Patientinnen von Anfang an klarere Erwartungen zu geben.
Zitation: Aggarwal, A., Madill, M., Jana, M. et al. STAR (stroma-tumor AI risk) assessment: association of AI-derived tumor-stroma proportion with patient survival provides added prognostic value beyond KELIM in epithelial ovarian cancer. BJC Rep 4, 4 (2026). https://doi.org/10.1038/s44276-026-00205-1
Schlüsselwörter: Ovarialkarzinom, künstliche Intelligenz, Tumormikroumgebung, prognostischer Biomarker, digitale Pathologie