Clear Sky Science · de
Genomische Untersuchung enthüllt das Auftauchen einer multiresistenten dominanten Linie in Proteus mirabilis-Populationen
Warum dieses Krankenhauskeim für Sie wichtig ist
Für viele Menschen sind Harnwegsinfektionen ein gelegentliches, schmerzhaftes Ärgernis. In Krankenhäusern und Pflegeeinrichtungen werden jedoch manche Infektionen von robusten Bakterien verursacht, die an Kathetern haften, mehreren Antibiotika trotzen und sich still zwischen Menschen und Tieren ausbreiten. Diese Studie verfolgt einen solchen Täter, Proteus mirabilis, weltweit und nutzt seine DNA als Reisetagebuch, um zu zeigen, wie sich über das letzte Jahrhundert eine einzelne, schwer zu behandelnde Familienlinie stillschweigend zur dominanten Form entwickelt hat.
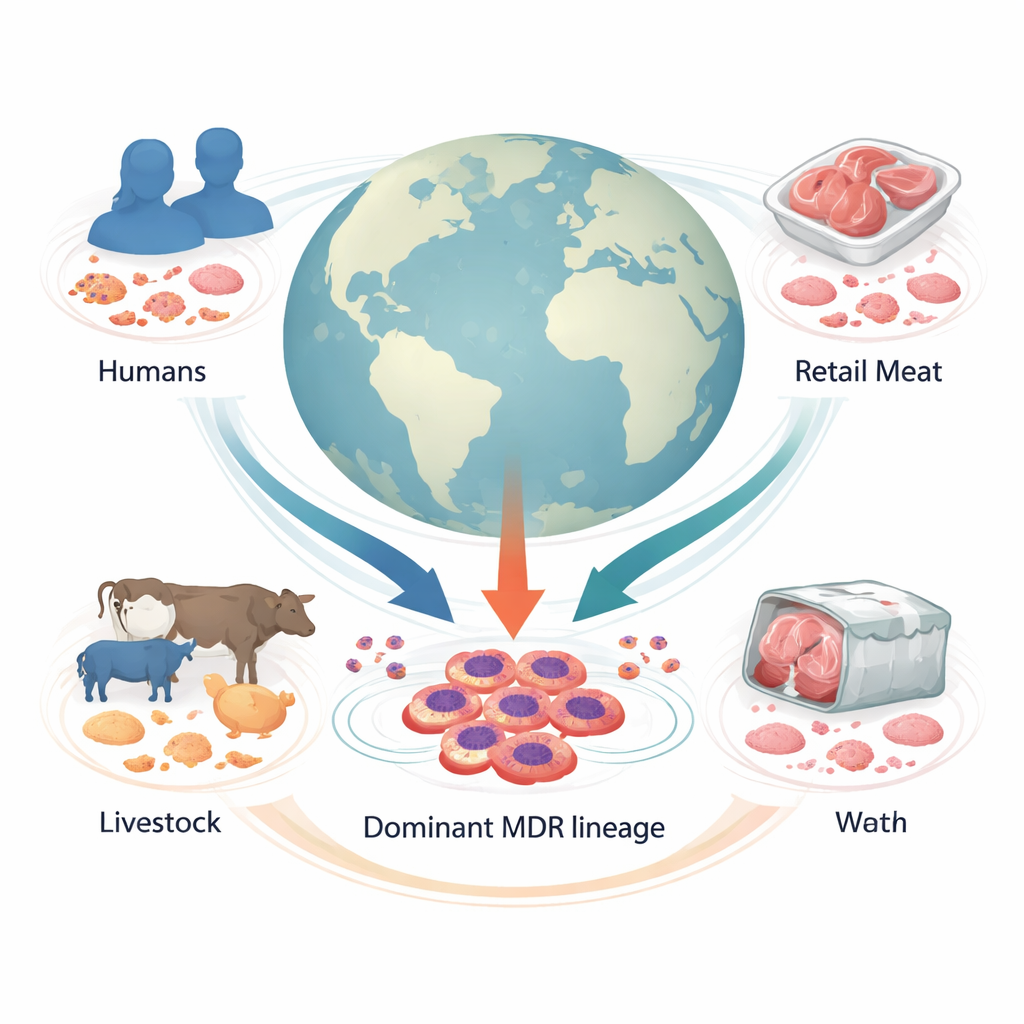
Ein weltweiter Blick auf eine verborgene Bedrohung
Die Forschenden stellten Genome von 1.142 Proteus mirabilis-Proben zusammen, die in 34 Ländern von Menschen, Nutztieren, im Einzelhandel verkauftem Fleisch und anderen Umgebungen gesammelt wurden. Durch den Vergleich ganzer Genome ordneten sie die Bakterien in 178 genetische Familien. Eine davon stach hervor: „Cluster-1“, eine große Linie, die ein Fünftel aller Proben ausmachte und Stämme aus Krankenhäusern auf mehreren Kontinenten einschloss. Die meisten dieser Stämme stammten von Menschen, ein beträchtlicher Anteil jedoch auch von Nutz- und Schlachttieren sowie aus Fleisch, was darauf hindeutet, dass diese Linie über Artengrenzen hinweg und entlang der Lebensmittelkette zirkuliert.
Eine Linie mit vielen Wirkstoffschutzschilden
Als das Team die Genome nach Antibiotikaresistenzgenen durchsuchte, zeigte Cluster-1 eine deutlich größere Last. Im Durchschnitt trugen seine Mitglieder fast 18 Resistenzen pro Stamm, deutlich mehr als andere Linien. Dazu gehörten Gene, die einige unserer stärksten Antibiotika außer Kraft setzen können, etwa Carbapeneme, die oft als letzte Reserve eingesetzt werden. Viele dieser Resistenzgene liegen in einem großen DNA-“Insel”-Abschnitt namens PmGRI1, der zwischen Bakterien springen kann. Manche Varianten dieser Insel tragen mehr als 20 Resistenzen gleichzeitig und verwandeln Proteus damit faktisch in eine wandelnde Apotheke von Abwehrmechanismen, was Ärztinnen und Ärzten nur wenige Behandlungsoptionen lässt.
Klebende Eigenschaften, die den Bakterien helfen zu bestehen
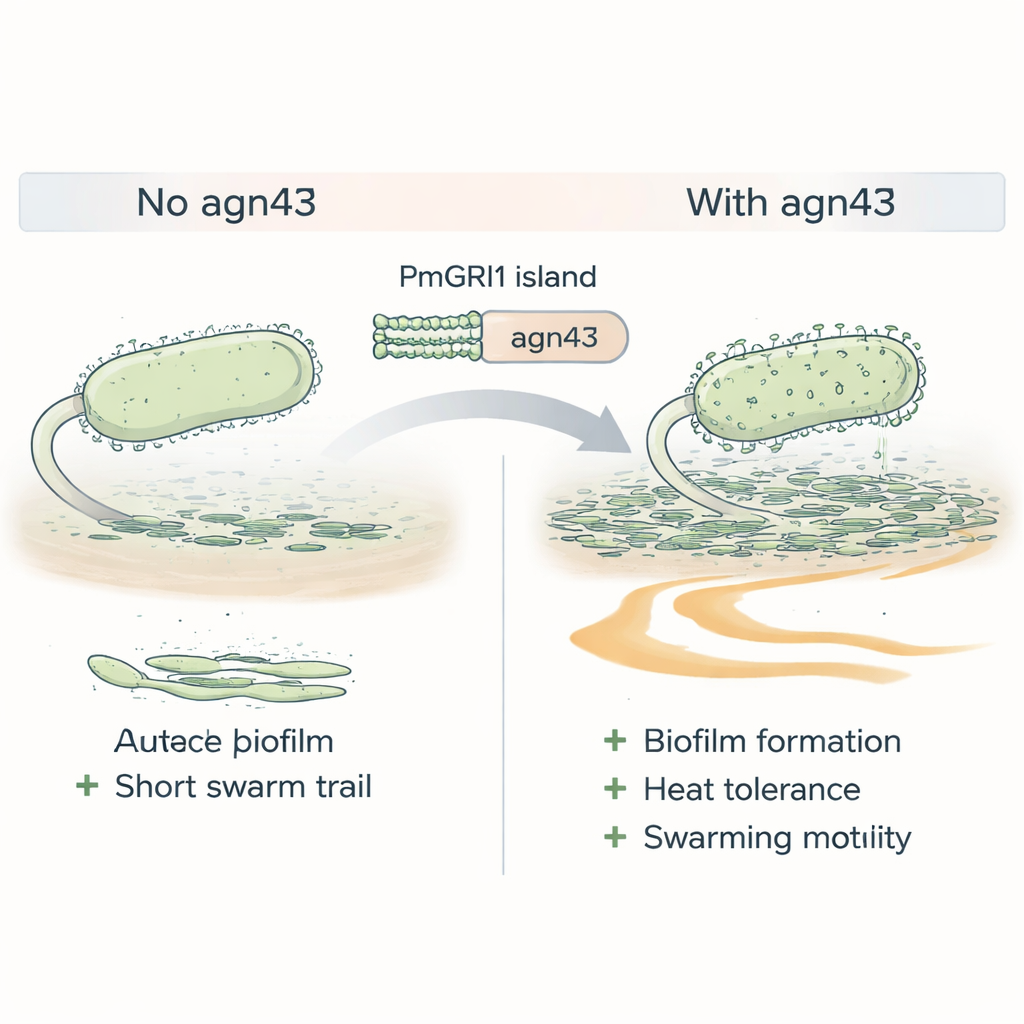
Resistenz allein garantiert keinen Erfolg; Bakterien müssen auch gut in Körper und Krankenhausumgebung überleben können. Cluster-1-Stämme wiesen vermehrt Gene auf, die mit dem Anhaften an Zellen und der Bildung von Biofilmen verknüpft sind – schleimige Gemeinschaften, die Bakterien vor Medikamenten und dem Immunsystem schützen. Ein markantes Gen auf der PmGRI1-Insel, agn43 genannt, codiert ein Oberflächenprotein, das wie molekulares Klett wirkt und Zellen zusammenhaften lässt. Als die Wissenschaftler agn43 in einem Cluster-1-Stamm entfernten, bildete der Mutant schwächere Biofilme, tolerierte Hitzestress schlechter und schwärmte weniger effizient über Oberflächen — Eigenschaften, die Proteus normalerweise helfen, Harnkatheter zu besiedeln und sich im Harntrakt auszubreiten.
Wie und wo sich diese Super-Linie ausbreitete
Durch die Kombination genetischer Unterschiede mit Isolationsdaten rekonstruierten die Forschenden einen Zeitstrahl für Cluster-1. Sie schätzten, dass sein jüngster gemeinsamer Vorfahr um 1910 auftrat, Jahrzehnte bevor moderne Antibiotika weitverbreitet eingesetzt wurden. Später teilte sich die Linie in zwei medizinisch bedeutsame Zweige: einen, der hauptsächlich in China gefunden wird und ein Carbapenem-aufhebendes Gen namens blaKPC-2 trägt, und einen anderen, der hauptsächlich in den Vereinigten Staaten vorkommt und ein verwandtes Gen, blaIMP-27, enthält. Ab den späten 1980er-Jahren expandierte Cluster-1 schnell und wurde wiederholt beim Wechsel zwischen Ländern sowie zwischen Menschen, Nutztieren und Fleisch nachgewiesen, was sein epidemisches Potenzial unterstreicht.
Was das für Patientinnen, Patienten und die öffentliche Gesundheit bedeutet
Für Laien lautet die Botschaft: Eine bestimmte Familie von Proteus mirabilis hat sich zu einem sehr erfolgreichen Krankenhauskeim entwickelt, indem sie zwei Vorteile kombinierte: eine dicke Rüstung aus Antibiotikaresistenzgenen und zusätzliche „Klebrigkeit“, die ihr hilft, schützende Filme zu bilden und an Kathetern und Gewebe zu haften. Diese Kombination macht Infektionen schwerer behandelbar und leichter übertragbar. Die Arbeit unterstreicht die Notwendigkeit einer engen genetischen Überwachung dieser Linie sowohl in Krankenhäusern als auch in der Landwirtschaft, strikterer Infektionskontrolle bei Kathetern und eines sorgfältigen Antibiotikaeinsatzes, um den Aufstieg und die globale Verbreitung solcher multiresistenter Stämme zu verlangsamen.
Zitation: Zhang, T., Wei, H., Ju, Z. et al. Genomic survey uncovers the emergence of a multidrug-resistant dominant lineage in Proteus mirabilis populations. npj Antimicrob Resist 4, 17 (2026). https://doi.org/10.1038/s44259-026-00189-5
Schlüsselwörter: Antibiotikaresistenz, Harnwegsinfektion, Krankenhausinfektionen, bakterielle Genomik, Biofilm