Clear Sky Science · de
Fünf Jahrzehnte globale Ausbreitung von Staphylococcus argenteus ST2250 prägen die Dynamik der antimikrobiellen Resistenz
Warum ein wenig bekanntes Keim wichtig ist
Die meisten Menschen haben schon von „MRSA“ gehört, dem medikamentenresistenten Staphylococcus aureus, der Krankenhäuser und Schlagzeilen beschäftigt. Viel weniger bekannt ist sein naher Verwandter, Staphylococcus argenteus. Diese Studie zeigt, dass sich eine bestimmte Familie von S. argenteus, genannt ST2250, in den letzten 50 Jahren stillschweigend weltweit verbreitet hat und dabei einen Werkzeugkasten von Antibiotika-Resistenzgenen angesammelt hat. Zu verstehen, wie das geschehen ist, hilft Ärzten und Gesundheitsbehörden, sich auf die nächste Welle schwer behandelbarer Infektionen vorzubereiten.
Ein neuer Störenfried in der Staph-Familie
S. argenteus wurde erst 2015 als eigene Art anerkannt, nachdem es jahrelang im Labor mit S. aureus verwechselt worden war. Dennoch kann es viele der gleichen Probleme verursachen: Lebensmittelvergiftungen, Haut- und Weichteilinfektionen, Blutstrominfektionen, Knochen- und Gelenkerkrankungen sowie Infektionen bei Tieren und in Lebensmitteln. Weil Routineuntersuchungen es oft als S. aureus fehlkennzeichnen, ist seine tatsächliche Bedeutung wahrscheinlich unterschätzt worden. Die Autorinnen und Autoren sammelten 379 hochwertig sequenzierte Genome von S. argenteus aus 28 Ländern auf sechs Kontinenten, überwiegend von menschlichen Patientinnen und Patienten, aber auch aus Lebensmitteln, Tieren und der Umwelt, um einen globalen Blick auf die Evolution dieser Art zu werfen.
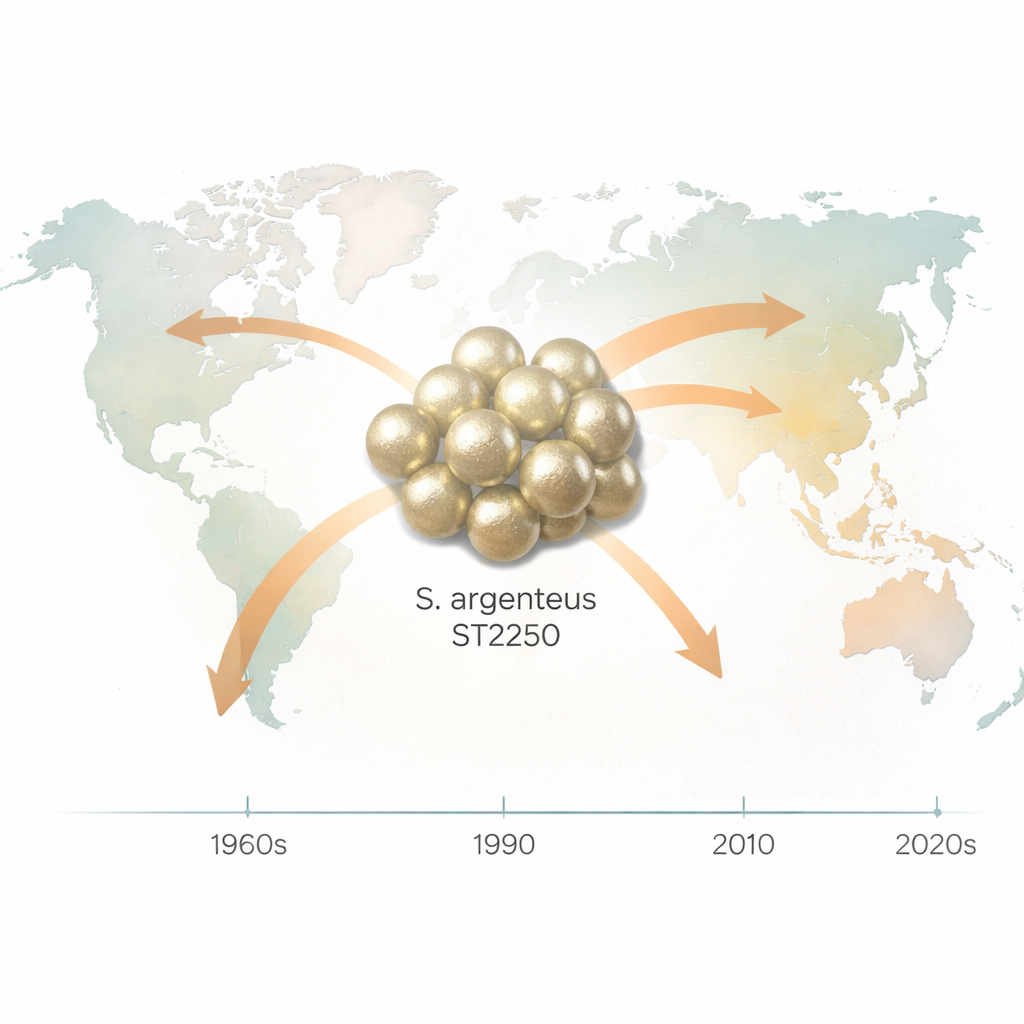
Ein dominanter Klon umkreist den Globus
Beim Vergleich der DNA all dieser Isolate stellten die Forschenden fest, dass S. argenteus aus mehreren unterschiedlichen Abstammungslinien besteht, die jeweils einem bestimmten genetischen „Sequenztyp“ entsprechen. Einer davon, ST2250, dominierte den Datensatz und machte mehr als die Hälfte aller Genome aus. ST2250 wurde auf mehreren Kontinenten und in vielen Probenarten gefunden, von hospitalisierten Patienten bis zu Lebensmitteln. Mithilfe eines zeitkalibrierten Stammbaums schätzten die Forschenden, dass der gemeinsame Vorfahr der heutigen ST2250-Stämme etwa um 1967 entstanden ist. Seitdem stieg seine effektive Populationsgröße – ein Indikator dafür, wie viele erfolgreiche Infektionen und Übertragungen stattfinden – über Jahrzehnte stark an, erreichte etwa 2012 einen Höhepunkt und zeigt seither Anzeichen eines jüngeren Rückgangs.
Beladen mit Resistenz- und Virulenzwerkzeugen
Die Studie katalogisierte Gene, die S. argenteus bei der Krankheitsentstehung helfen (Virulenzgene), sowie solche, die Antibiotikaresistenzen vermitteln (antimikrobielle Resistenz- oder AMR-Gene). Jedes Genom trug dutzende Virulenzgene, und ST2250-Stämme hatten nur geringfügig weniger davon als andere Linien, was auf ein ähnliches Erkrankungspotenzial hindeutet. Der größere Unterschied lag in der Resistenz. Insgesamt identifizierten die Autorinnen und Autoren 29 verschiedene AMR-Gene, die 12 Klassen von Antibiotika und Desinfektionsmitteln abdecken. ST2250-Stämme trugen typischerweise mehr Resistenzgene als andere Typen und zeigten oft dieselben Kombinationen. Viele ST2250-Isolate enthielten außerdem fosB, ein Gen, das gegen Fosfomycin schützt — ein „altes“ Antibiotikum, das gegen schwer zu behandelnde Staph-Infektionen wieder vermehrt eingesetzt wird. Der nahe Verwandte ST1850 trug ebenfalls fosB, was darauf hindeutet, dass dieses Gen bereits im gemeinsamen Vorfahren vorhanden gewesen sein könnte.
Wie sich Resistenzmerkmale zusammen verbreiten
Die Forschenden suchten nach Resistenzgenen, die häufiger gemeinsam in denselben Stämmen auftreten, als es Zufall erklären würde. Sie fanden starke Paarungen wie das Tetrazyklin-Resistenzgen tetL mit dem Aminoglykosid-Resistenzgen aph(3')-IIIa und das Trimethoprim-Resistenzgen dfrG mit Methicillin-Resistenz (mecA). Diese Cluster spiegeln wahrscheinlich frühere Ereignisse wider, bei denen mehrere Gene gleichzeitig auf mobilen DNA-Elementen wie Plasmiden aufgenommen und dann vererbt wurden, als sich die bakteriellen Linien ausbreiteten. Tatsächlich entdeckte das Team Dutzende von Plasmid-„Replikon“-Typen und zeigte, dass einige Plasmide stark mit bestimmten Resistenzgenen zusammen vorkommen. Innerhalb von ST2250 traten zwei große Sublinien hervor: eine in Asien und eine in Europa, jeweils mit einem charakteristischen Resistenzpaket und in Europa zusätzlich mit der Methicillin-Resistenzkassette SCCmec.
Was das für die Zukunft bedeutet
Für Nicht-Spezialisten ist die Kernbotschaft, dass S. argenteus keine harmlose Kuriosität ist, sondern ein aufstrebendes Mitglied der medikamentenresistenten Staph-Familie. Innerhalb von etwa fünf Jahrzehnten hat sich eine einzelne erfolgreiche Linie, ST2250, weit verbreitet und eine reiche Mischung an Resistenzgenen angesammelt, wodurch Bedingungen entstanden sind, in denen leicht multiresistente Stämme entstehen können. Obwohl es erste Hinweise gibt, dass das Wachstum von ST2250 langsamer werden könnte, lauern andere Linien mit eigenen Resistenzmerkmalen bereits im Hintergrund. Die Autorinnen und Autoren plädieren dafür, S. argenteus genauer zu identifizieren, Probenahmen über Krankenhäuser hinaus auszuweiten und eine enge genetische Überwachung einzuführen, um zu verhindern, dass dieser leise Erreger zur nächsten großen Staph-Bedrohung wird.
Zitation: Costa, L.R.M., Marmion, M., Buiatte, A.B.G. et al. Five-decade global expansion of Staphylococcus argenteus ST2250 shapes antimicrobial resistance dynamics. npj Antimicrob Resist 4, 14 (2026). https://doi.org/10.1038/s44259-026-00188-6
Schlüsselwörter: Staphylococcus argenteus, antimikrobielle Resistenz, genomische Epidemiologie, ST2250-Klon, medikamentenresistente Bakterien