Clear Sky Science · de
Phagen‑Meropenem-Synergie gegen OXA‑48‑produzierende klinische Isolate von Klebsiella pneumoniae
Warum winzige Viren versagende Antibiotika retten könnten
Krankenhäuser weltweit kämpfen mit Infektionen, die auf unsere stärksten Antibiotika nicht mehr ansprechen. Einer der schlimmsten Übeltäter ist ein Bakterium namens Klebsiella pneumoniae, das Lungenentzündungen, Blutbahninfektionen und Harnwegsinfektionen verursachen kann. Diese Studie untersucht, ob sorgfältig ausgewählte Viren, die Bakterien angreifen – sogenannte Phagen – zusammen mit einem starken Antibiotikum, Meropenem, hochresistente Stämme eliminieren können, die derzeit das Leben von Patientinnen und Patienten bedrohen.
Ein heimlicher Krankenhauskeim auf dem Vormarsch
Klebsiella pneumoniae ist zu einem wichtigen Krankenhaus‑Superkeim geworden, weil viele Stämme gelernt haben, Carbapeneme zu widerstehen, einer Antibiotikagruppe, die als letzte Verteidigungslinie reserviert ist. Diese Bakterien tragen oft Resistenzgene auf winzigen DNA‑Kreisen, sogenannten Plasmiden, die sie wie Sammelkarten untereinander austauschen können. Eines dieser Plasmide, bekannt als pOXA‑48, kodiert ein Enzym, das Carbapeneme abbaut und Medikamente wie Meropenem weitgehend wirkungslos macht. Wenn sich diese Plasmide durch hochriskante Bakterienklone in Europa und darüber hinaus ausbreiten, werden Standardbehandlungen unzuverlässiger und selbst routinemäßige medizinische Eingriffe riskanter.
Phagen als präzise Angreifer rekrutieren
Da neue Antibiotika langsam entwickelt werden, wenden sich Forschende der Phagentherapie zu – dem Einsatz von Viren, die spezifisch Bakterien infizieren und abtöten. In dieser Studie konzentrierte sich das Team auf einen lytischen Phagen namens vB_Kpn_2-P4, der eine breite Palette klinischer Klebsiella-Isolate aus spanischen Krankenhäusern infizieren kann. In Laborversuchen attackierte dieser Phage Bakterien, die verschiedene Carbapenem‑Resistenzmechanismen trugen. Allerdings überlebten, wie bei Antibiotika und Phagen häufig, einige Bakterienzellen und wuchsen nach, was die Notwendigkeit von Kombinationsstrategien statt des Vertrauens auf ein einzelnes Mittel unterstreicht.
Wenn Medikament und Virus besser zusammenwirken
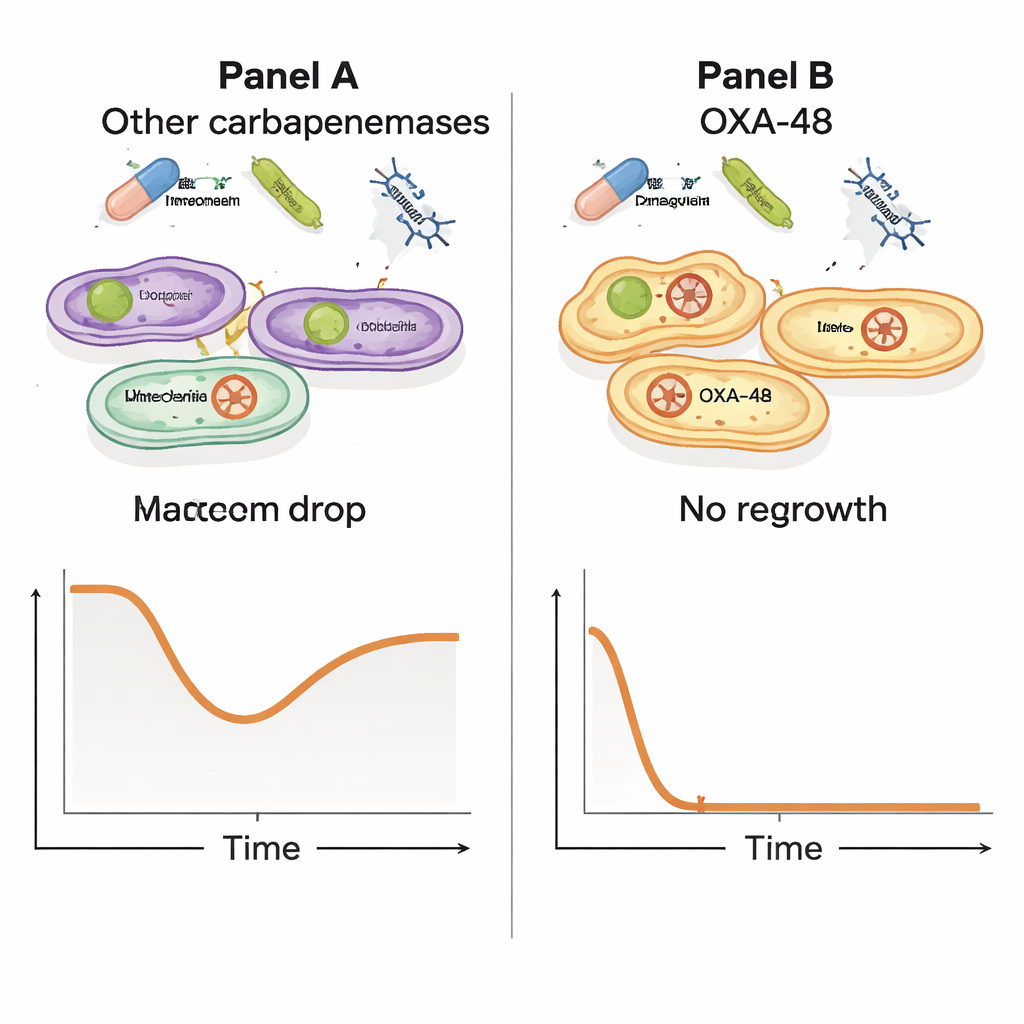
Die Forschenden testeten dann, wie Meropenem und der Phage gemeinsam wirken. Sie kultivierten zwölf resistente bakterielle Isolate und setzten sie Meropenem allein, dem Phagen allein oder beidem gleichzeitig aus und verfolgten das Wachstum über viele Stunden. Während alle Isolate unter den Testbedingungen Meropenem tolerieren konnten, zeigte sich ein auffälliges Muster: In Stämmen, die das OXA‑48‑Plasmid trugen, führte die Kombination aus Phage und hoher Meropenem‑Dosis zu einem dramatischen Einbruch der Bakterienzahlen, gefolgt von keiner nachweisbaren Wiederentwicklung. Bei niedrigeren Meropenem‑Konzentrationen zeigten diese OXA‑48‑Stämme immer noch einen starken Rückgang der bakteriellen Belastung. Im Gegensatz dazu zeigten Stämme mit anderen Resistenzenzymen diesen kraftvollen gemeinsamen Effekt nicht, was darauf hindeutet, dass ein besonderes Merkmal des OXA‑48‑Plasmids die Bakterien bei gleichzeitiger Konfrontation beider Bedrohungen einzigartig verwundbar macht.
Das versteckte genetische Helferlein verfolgen
Um zu verstehen, warum nur die OXA‑48‑Produzenten diese Synergie zeigten, verglich das Team die Genome der verschiedenen bakteriellen Isolate. Sie identifizierten Dutzende von Genen, die mit der synergistischen Reaktion assoziiert waren, fast alle gruppiert auf dem pOXA‑48‑Plasmid. Wichtig ist, dass bei isolierten Bakterien, die Resistenzen gegen den Phagen entwickelt hatten, diese Überlebenden weiterhin ein intaktes OXA‑48‑Gen trugen; sie hatten das Plasmid nicht einfach verworfen, um zu entkommen. Das deutet auf ein subtileres Bild hin, in dem das Plasmid, das Arzneimittelresistenz verleiht, auch versteckte Kosten für die Biologie der Bakterien mit sich bringt – Kosten, die tödlich werden, wenn Phage und Antibiotikum gemeinsam zuschlagen und das Gleichgewicht gegen den Erreger kippen.
Was das für zukünftige Behandlungen bedeuten könnte
Für Nicht‑Spezialisten lautet die Kernbotschaft, dass die genetischen Tricks, mit denen Bakterien unsere Medikamente umgehen, manchmal gegen sie verwendet werden können. In diesem Fall scheint ein spezifisches Resistenzplasmid bestimmte Klebsiella-Stämme äußerst empfindlich gegenüber einem kombinierten Angriff durch einen maßgeschneiderten Phagen und Meropenem zu machen. Obwohl diese Arbeit unter Laborbedingungen durchgeführt wurde und weitere Forschung in Tiermodellen und an Patientinnen und Patienten nötig ist, legt sie nahe, dass das passende Zusammenführen von Phagen und Resistenzprofilen Antibiotika wiederbeleben könnte, die ihren Nutzen verloren zu haben scheinen. Phagen könnten nicht die Antibiotika ersetzen, sondern intelligente Verbündete werden, die uns helfen, Superkeime zu überlisten, die einst unbesiegbar schienen.
Zitation: Cantallops, I., Ferriol-González, C., Barcos-Rodríguez, T. et al. Phage-meropenem synergy against OXA-48-producing Klebsiella pneumoniae clinical isolates. npj Antimicrob Resist 4, 12 (2026). https://doi.org/10.1038/s44259-026-00186-8
Schlüsselwörter: Phagentherapie, Antibiotikaresistenz, Klebsiella pneumoniae, OXA‑48‑Plasmid, Meropenem‑Synergie