Clear Sky Science · de
Globale Reaktion auf Antibiotikabelastung offenbart eine entscheidende Rolle des Nukleotidstoffwechsels für hochgradige β-Laktam-Toleranz
Warum manche Bakterien unseren besten Antibiotika trotzen
Antibiotika sollen schädliche Bakterien auslöschen, doch viele Infektionen halten sich hartnäckig oder kehren nach der Behandlung zurück. Diese Arbeit untersucht einen wenig beachteten Grund dafür: Manche Bakterien können sich zurückziehen und vorübergehend selbst sehr hohe Dosen starker Wirkstoffe wie Penicillin überstehen. Indem die Forschenden aufdecken, wie diese Mikroben ihre innere Chemie umstellen, um die Attacke auszusitzen, zeigen sie Wege auf, wie man die Wirksamkeit vorhandener Antibiotika wiederherstellen könnte.
Ein heimlicher Überlebenstrick in Infektionen
Wenn sie β-Laktam-Antibiotika wie Penicillin ausgesetzt sind, sterben viele gefährliche gramnegative Bakterien nicht einfach ab. Stattdessen können sie ihre starre Zellwand abwerfen und in fragilere, kugelförmige Körper, sogenannte Spheroplaste, übergehen. In dieser Form vermehren sie sich nicht, bleiben aber am Leben und stoffwechselaktiv. Sobald das Medikament verschwunden ist, bauen sie ihre Wand wieder auf, nehmen ihre normale stabförmige Gestalt an und können die Infektion erneut entfachen. Da diese „Toleranz“ ein Zwischenschritt auf dem Weg zu ausgewachsener Antibiotikaresistenz und Therapieversagen ist, ist das Verständnis, wie Spheroplaste überleben, für die Medizin der Zukunft entscheidend.
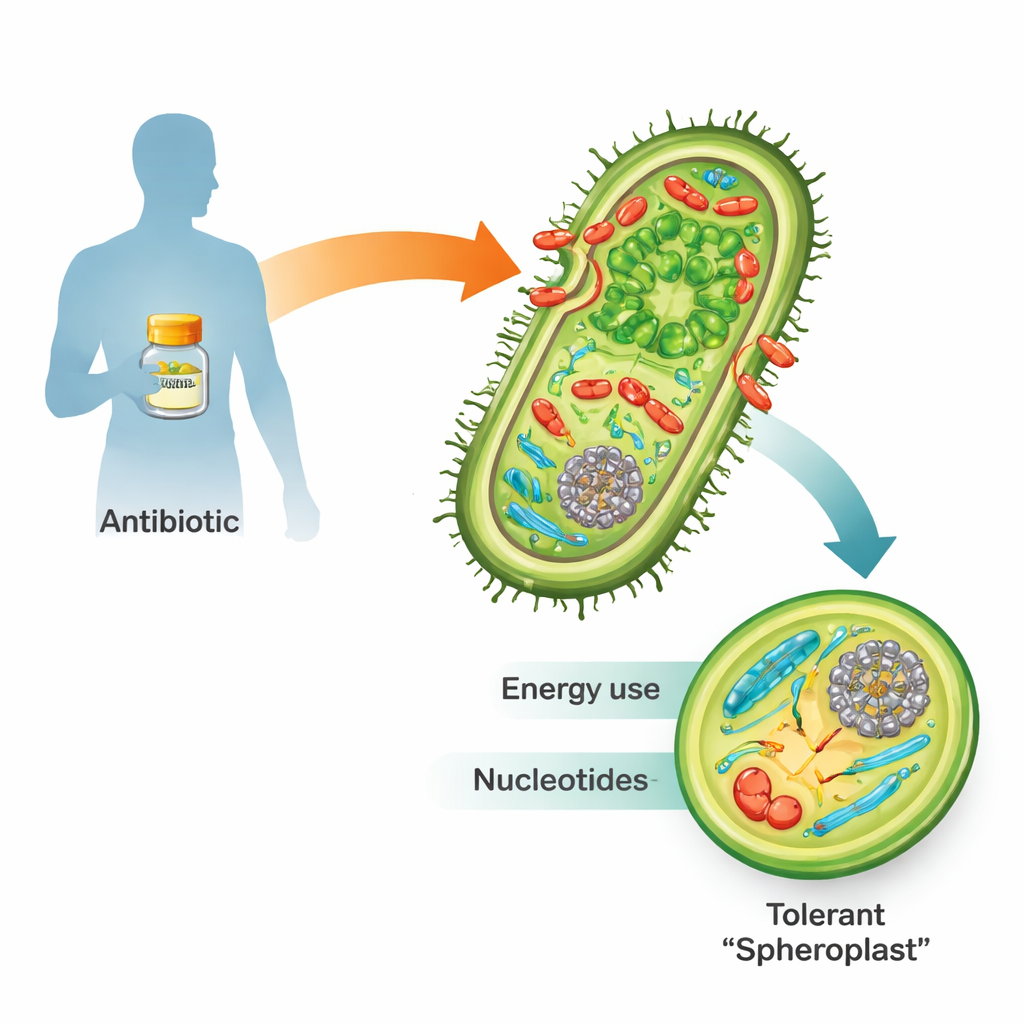
In den Notfunk der Zelle hineinhören
Das Team nutzte Vibrio cholerae, das Bakterium, das Cholera verursacht, als Modell, weil es gegenüber β-Laktamen außergewöhnlich tolerant ist und sich genetisch leicht manipulieren lässt. Sie setzten die Bakterien dem Zehnfachen der minimal tödlichen Penicillindosis aus und verfolgten die Reaktion über die Zeit mit zwei leistungsfähigen Werkzeugen. Die Transkriptomik zeichnete auf, welche Gene ein- oder ausgeschaltet wurden, während die Metabolomik Hunderte kleiner Moleküle maß, die die Zelle antreiben und aufbauen. Zusammen erzeugten diese Multi-Omics-Techniken eine zeitaufgelöste Karte, wie eine tolerante Zelle ihre inneren Abläufe während eines Wirkstoffangriffs umgestaltet.
Metabolische Umleitung und eine verborgene Schwachstelle
Die Daten zeigten weitreichende Veränderungen in zentralen Stoffwechselwegen. Gene für den Aufbau der Zellwand wurden stark hochreguliert, was zur Reparatur und Vorbereitung auf die Erholung passt. Hitzeschock- und Stressantwortsysteme gingen ebenfalls hoch, vermutlich um fehlgefaltete oder oxidierte Proteine zu bewältigen, die durch Antibiotikastress entstehen. Gleichzeitig verschob sich der zentrale Kohlenstoffstoffwechsel: Bestimmte Schritte des TCA-Zyklus (dem wichtigsten Energieerzeuger der Zelle) wurden verstärkt, während zentrale Glykolyse-Intermediäre wie Glukose-6-phosphat und Fruktose-6-phosphat dramatisch erschöpft waren. Diese Zwischenprodukte speisen normalerweise sowohl die Energieproduktion als auch den Zellwandaufbau, was darauf hindeutet, dass ein kontinuierliches, verschwenderisches „futile cycling“ von Wandmaterial Ressourcen erschöpft.
Nukleotide unter Druck
Die auffälligste Veränderung betraf Nukleotide, die Bausteine von DNA, RNA und vielen energietragenden Molekülen. Die Konzentrationen vieler Nukleotide und ihrer Vorstufen fielen in penicillibehandelten Zellen stark ab, obwohl die Gene für deren de-novo-Synthese stark aktiviert waren. Gleichzeitig wurden Gene, die am „Recycling“ von Nukleotiden beteiligt sind, heruntergefahren, als ob die Zelle versuche, das Wenige zu sparen, das noch vorhanden ist. Dieses Muster deutete darauf hin, dass Spheroplaste unter massivem Nukleotidstress stehen. Als die Forschenden gezielt Wege blockierten, die Nukleotidvorstufen liefern—etwa die Pentosephosphatweg—oder die Nukleotidproduktion mit einem anderen Medikament, Trimethoprim, hemmten, tötete die Kombination mit β-Laktamen deutlich mehr Bakterien als eines der Mittel allein. Diese starke Synergie zeigte sich nicht nur bei Vibrio cholerae, sondern auch bei hoch toleranten klinischen Stämmen von Klebsiella pneumoniae und Escherichia coli.
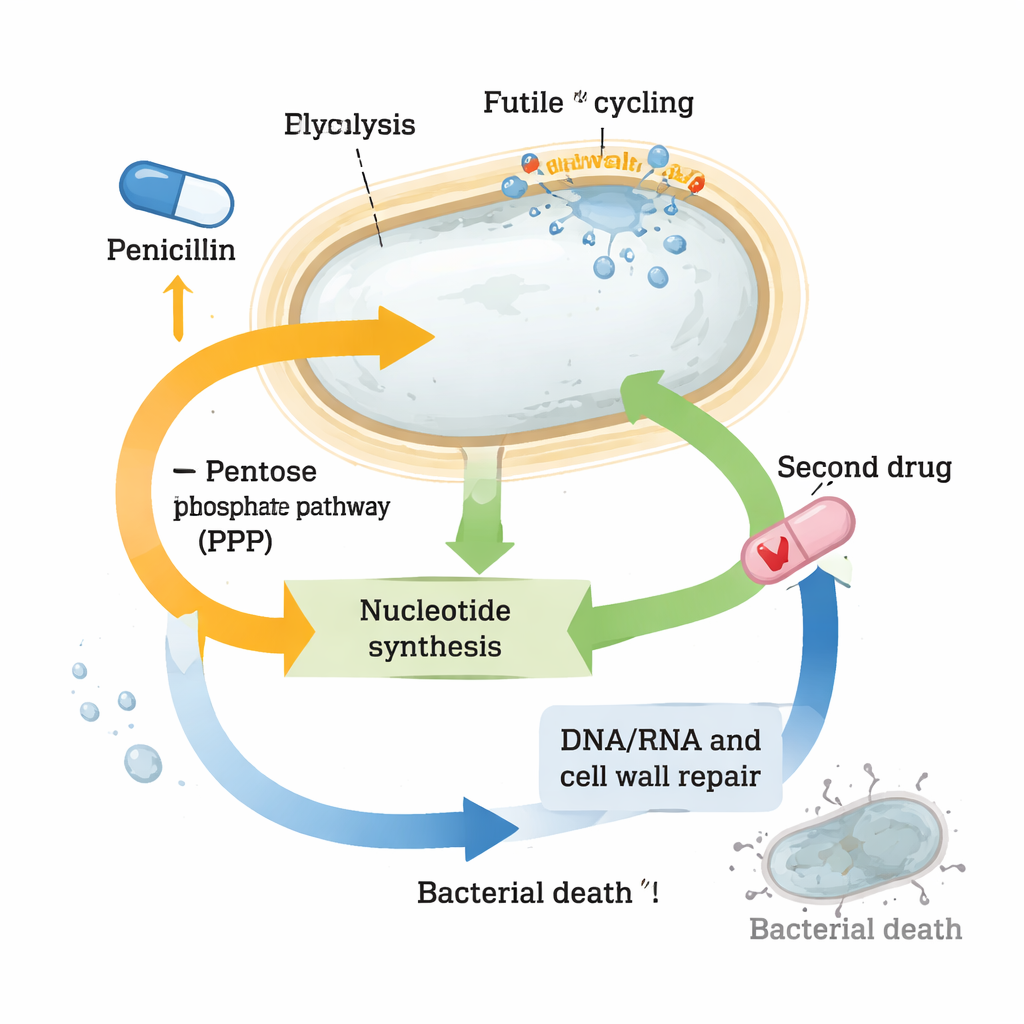
Überlebenschemie in einen therapeutischen Vorteil verwandeln
Trotz umfassender Umgestaltung ihres Stoffwechsels schaffen es tolerante Spheroplaste, ihre Energiewährung ATP relativ stabil zu halten und katastrophale Schäden zu vermeiden, was ihnen hilft, lange Antibiotikabelastungen zu überstehen. Die Studie zeigt jedoch, dass sie dabei ihre Nukleotidvorräte an den Rand des Abgrunds treiben. Dieses prekäre Gleichgewicht schafft eine Verwundbarkeit: Schiebt man den Nukleotidstoffwechsel mit einem zweiten Wirkstoff nur wenig weiter, kollabieren ihre Abwehrmechanismen und die tödliche Wirkung kehrt zurück. Für Nichtfachleute lautet die Kernbotschaft: Manche Bakterien überleben Antibiotika nicht, weil die Medikamente ihre Ziele nicht treffen, sondern weil die Zellen ihre Chemie schnell umstellen, um den Schlag auszuhalten. Indem Forschende die schwachen Stellen dieser Überlebensverkabelung finden und ausnutzen—hier den Nukleotidstoffwechsel—könnten alte Antibiotika zu wirksamen Kombinationstherapien werden, die selbst hoch tolerantem Pathogenen überlegen sind.
Zitation: Keller, M.R., Kazi, M.I., Saleh, A. et al. Global response to antibiotic exposure reveals a critical role for nucleotide metabolism in high-level β-lactam tolerance. npj Antimicrob Resist 4, 11 (2026). https://doi.org/10.1038/s44259-026-00183-x
Schlüsselwörter: Antibiotika-Toleranz, β-Laktam-Antibiotika, Nukleotidstoffwechsel, bakterielle Persistenz, Arzneimittelkombinationen