Clear Sky Science · de
Maschinelles Lernen ermöglicht Echtzeit-Akustikfallen in zeitlich veränderlichen Mehrschicht‑Medien — hin zu MRI‑geführter Mikroschaum‑Manipulation
Kleine Wirkstoffträger mit Schall und Bildgebung führen
Moderne Krebsbehandlungen setzen zunehmend auf intelligente Wirkstoffträger, die Medikamente gezielt an Tumore liefern und gesundes Gewebe schonen. Diese Studie untersucht eine futuristische Methode, solche Träger im Körper mithilfe von Ultraschall‑„Fallen“ zu steuern, die durch Magnetresonanztomographie (MRT) geführt werden. Durch die Kombination von Schallwellen, medizinischer Bildgebung und maschinellem Lernen wollen die Forschenden mikroskopische Bläschen mit Wirkstoff so positionieren, dass sie in der Nähe sich bewegender Tumore verbleiben — selbst wenn sich der Körper mit jeder Atembewegung verschiebt.
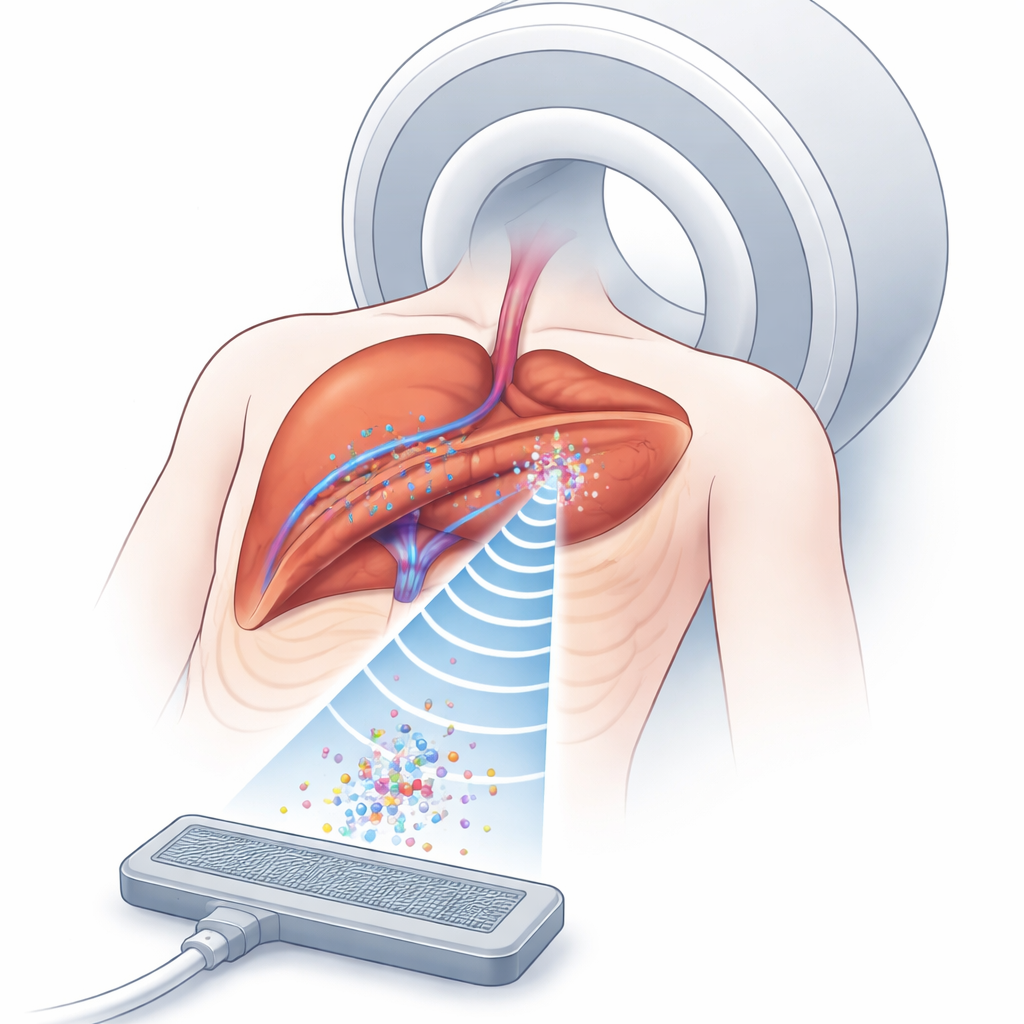
Warum das Einfangen mikroskopischer Bläschen wichtig ist
Wirkstofftragende Mikroschaum‑Bläschen bewegen sich durch Blutgefäße und können ihre Fracht freisetzen, wenn sie durch Ultraschall ausgelöst werden. Die Herausforderung besteht darin, genügend dieser Bläschen lange genug an der richtigen Stelle tief im Körper zu halten. Ultraschall kann unsichtbare Kraftfelder erzeugen — akustische Fallen — die kleine Objekte berührungsfrei in Flüssigkeiten fixieren. Die MRT kann gleichzeitig Gewebe und das Muster der Ultraschalleffekte sichtbar machen, selbst innerhalb von Organen. Die Kombination dieser Werkzeuge ermöglicht eine präzisere Konzentration von Wirkstoffträgern um Tumore als mit Medikamenten allein. Im echten Menschen brechen und verzerren jedoch unterschiedliche Gewebetypen — Fett, Muskel, Organe und bewegliche Lungen — Schallwellen, sodass es sehr schwierig ist, eine stabile Falle genau über dem Tumor zu formen und aufrechtzuerhalten.
Das Problem eines bewegten, geschichteten Körpers
In einfachen Medien wie Luft oder Wasser wissen Ingenieure bereits, wie phasengesteuerte Ultraschallarrays verwendet werden, um winzige Objekte zu schieben, zu ziehen oder zu drehen. Im Körper muss Schall jedoch mehrere Schichten mit unterschiedlichen Dichten und Schallgeschwindigkeiten durchdringen, und die Grenzflächen zwischen ihnen bewirken Brechung und Verzerrung. Traditionelle rechnerische Methoden können dies prinzipiell korrigieren, indem sie berechnen, wie lange Schall von jedem Sender bis zum Zielpunkt benötigt. Solche Ansätze teilen den Körper jedoch in Millionen winziger Blöcke und simulieren die Wellenausbreitung durch jeden einzelnen — ein extrem zeitaufwändiges Verfahren, das nur funktioniert, wenn das Gewebe nahezu vollkommen still bleibt. Allein das Atmen kann abdominale Gewebe um mehrere Millimeter verschieben und schnell jede vorab berechnete Lösung veralten lassen.
Ein Modell lehren, Schallwege vorherzusagen
Die Autorinnen und Autoren begegnen diesem Engpass mit einem lernbasierten Modell, das als schneller Umweg dient: Anstatt bei jeder Aktualisierung Schallwellen zu simulieren, trainieren sie ein neuronales Netzwerk, das vorhersagt, wie lange jeder Ultraschallimpuls braucht, um einen Zielpunkt zu erreichen. Zunächst bauen sie eine detaillierte virtuelle Umgebung mit einer gasgefüllten Kammer, die durch eine dünne Plastikfolie von der Luft getrennt ist — ein Nachbild dafür, wie Schall verschiedene Gewebeschichten durchläuft. Mithilfe eines physikbasierten Simulators erzeugen sie einen Trainingssatz mit Schalllaufzeiten zwischen vielen Zielpunkten und einem 14×14‑Ultraschallarray. Die Kammer darf sich außerdem in zwei Richtungen verschieben, um Bewegung zu imitieren, und ihre Lage wird durch drei sichtbare Marker beschrieben, analog zu künftigen MRT‑sichtbaren Markern, die die Atmung eines Patienten verfolgen würden. Das trainierte Netzwerk lernt, die gewünschte Fallenposition plus Kammerstellung direkt in das notwendige Zeitmuster für alle 196 Sender zu überführen und erreicht Mikrosekunden‑Genauigkeit in nur etwa 26 Millisekunden.
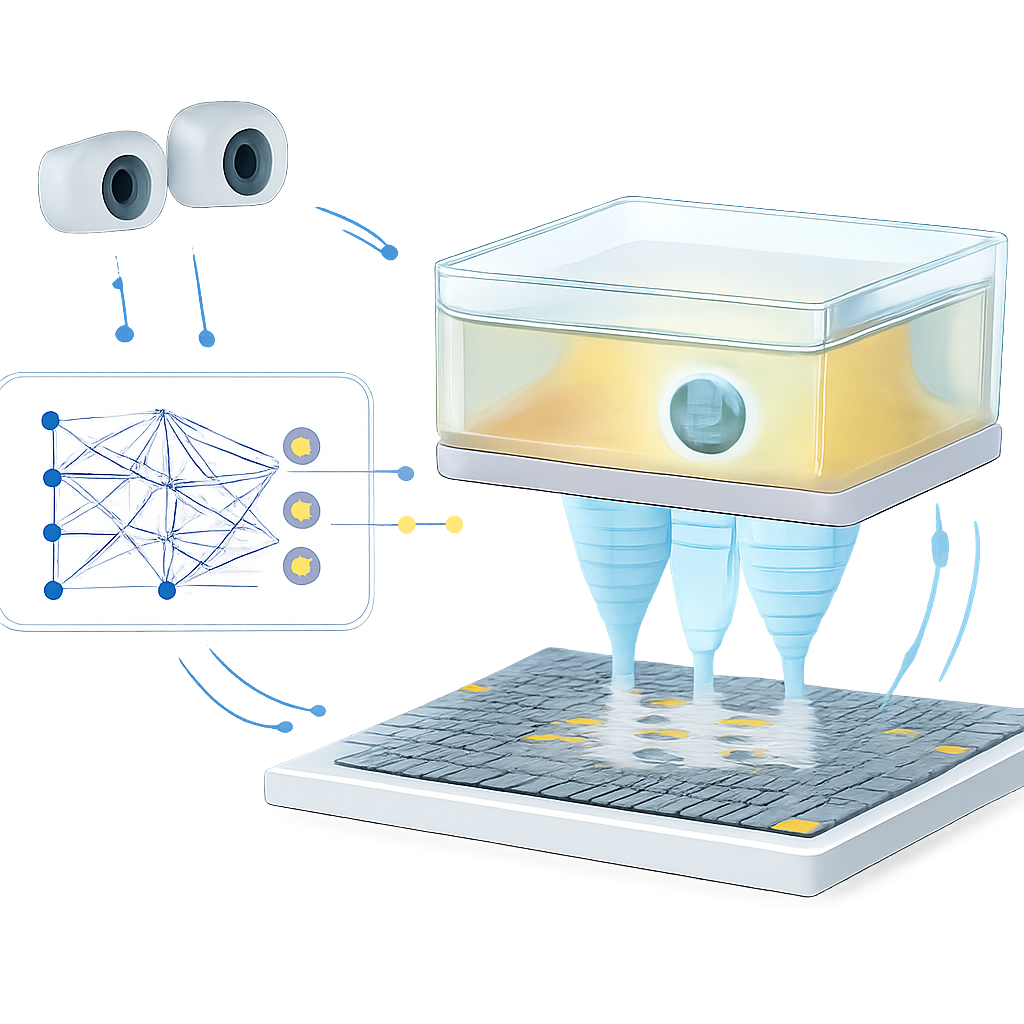
Regelkreis mit Sicht und schnellen Aktualisierungen
Geschwindigkeit allein reicht nicht; die Falle muss sich auch an unerwartete Änderungen der Umgebung anpassen. Um das zu demonstrieren, baut das Team ein geschlossenen Regelkreissystem. Stereo‑Kameras beobachten eine kleine Polystyrolkugel, die von der akustischen Falle innerhalb der bewegten Kammer in der Schwebe gehalten wird. Weicht die Kugel über einen festgelegten Schwellenwert vom Ziel ab, verschiebt das System die Zielposition, übergibt die aktualisierten Koordinaten und die Kammerpose an das Lernmodell und aktualisiert schnell das Phasenmuster, das das Array antreibt. In Experimenten kann das System das Phasenmuster bis zu 15 Mal pro Sekunde aktualisieren und die Kugel entlang H‑, K‑ und U‑förmigen Bahnen mit etwa 1 Millimeter mittlerem Fehler steuern — vergleichbar mit der Positioniergenauigkeit einiger klinischer fokussierter Ultraschallsysteme. Dasselbe Rückkopplungsprinzip verkürzt auch die Zeit, die die Kugel bei Bewegung der Kammer vom Ziel abweicht, und zeigt, dass der Regelkreis für Bewegung und nicht modellierte Effekte durch die Plastikfolie und die Trägerstruktur kompensieren kann.
Was das für künftige Behandlungen bedeutet
Für Nicht‑Spezialisten lautet die Kernaussage: Die Forschenden haben eine Art ferngesteuerten, berührungslosen „Traktorstrahl“ entwickelt, der eines Tages Wirkstoff‑gefüllte Bläschen in der Nähe eines Tumors parken und dort halten könnte, selbst wenn der Patient atmet. Ihr Modell des maschinellen Lernens ersetzt aufwändige Simulationen durch einen schnellen Prädiktor, während Kameras (und schließlich MRT‑Marker) dem System mitteilen, wie sich der Körper bewegt, sodass die Falle in Echtzeit nachgestimmt werden kann. Obwohl die vorliegende Arbeit Luft, Gase und Plastik statt echten Geweben verwendet und eine Plastikperle statt echter Mikroschaum‑Bläschen levitiert, demonstriert sie Echtzeitsteuerung in einem bewegten, geschichteten Medium. Mit leistungsfähigerer Hardware, höheren Ultraschallfrequenzen und MRT‑basierter Bewegungsverfolgung könnte dieser Ansatz zu einem klinischen Werkzeug für MRI‑geführte, robotergestützte Ultraschalltherapien werden, die Medikamente tiefer im Körper genauer und sicherer abliefern.
Zitation: Wu, M., Li, X. & Tang, T. Machine learning-facilitated real-time acoustic trapping in time-varying multi-medium environments toward magnetic resonance imaging-guided microbubble manipulation. Commun Eng 5, 52 (2026). https://doi.org/10.1038/s44172-026-00600-z
Schlüsselwörter: akustische Falle, MR‑geführte Therapie, Mikroschaum‑Arzneimittelabgabe, Maschinelles Lernen in der Ultraschalltechnik, nichtinvasive robotische Manipulation