Clear Sky Science · de
Photoaktivierte Ultraschall-Lokalisationsbildgebung mit laseraktivierten Nanotropfen
Schärfere Ansichten winziger Blutgefäße
Ärztinnen, Ärzte und Forschende verlassen sich zunehmend auf Ultraschall, um in Echtzeit ins Körperinnere zu blicken. Bei den kleinsten Blutgefäßen können heutige Scanner jedoch wichtige Details verwischen. Diese Studie stellt eine neue Methode vor, mit der Ultraschallkontrast im Blutstrom per Licht kontrollierbarer Nanotropfen „eingeschaltet“ werden kann. Das eröffnet die Möglichkeit für klarere Bilder von Gehirn und anderen Organen, längere Untersuchungszeiten und potenziell sicherere, präzisere bildgeführte Behandlungen.
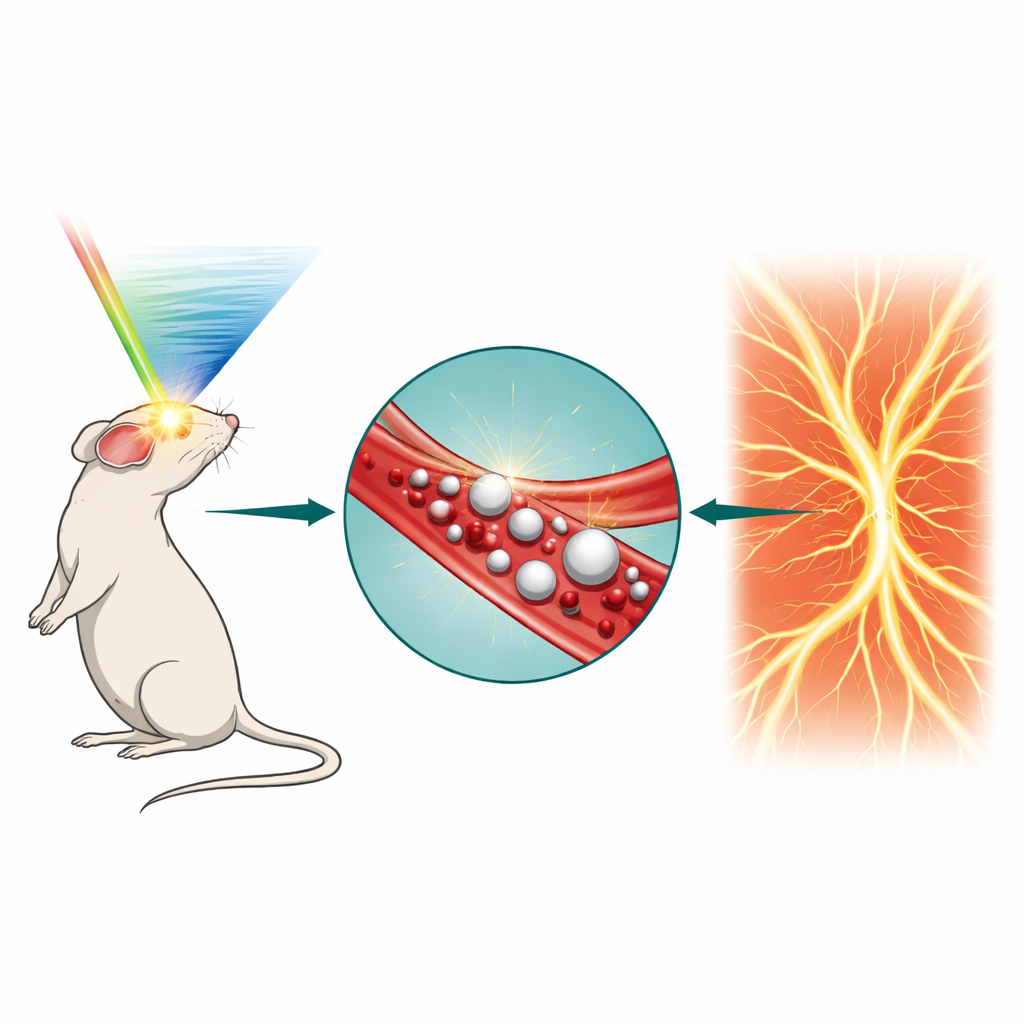
Warum das Sichtbarmachen kleiner Gefäße so schwierig ist
Konventioneller Ultraschall funktioniert gut für größere Strukturen, doch seine Auflösung ist durch die Physik der Schallwellen begrenzt: Objekte, die kleiner sind als etwa die halbe Wellenlänge, verschwimmen. Ein jüngster Fortschritt, die Ultraschall-Lokalisationsbildgebung, umgeht dieses Problem, indem sie einzelne Mikroschaumbläschen verfolgt, die in den Blutkreislauf injiziert werden, und aus ihren Bahnverläufen eine hochaufgelöste Gefäßkarte erstellt – ähnlich dem Nachverfolgen von Straßen durch das Beobachten tausender Autos bei Nacht. Diese Mikroschaumbläschen sind allerdings relativ groß, zirkulieren nur wenige Minuten, verteilen sich in kleinen Gefäßen nicht gleichmäßig, und ihr Signal lässt bei langen oder wiederholten Aufnahmen schnell nach. Diese Einschränkungen begrenzen, wie gründlich und wie lange Ärzt:innen empfindliche mikrovaskuläre Netze im Gehirn, in Tumoren oder Nieren untersuchen können.
Nanotropfen auf Anforderung zum Leuchten bringen
Die Autor:innen gingen diese Grenzen an, indem sie winzige Nanotropfen entwickelten, die durch kurze Laserpulse nur dort und dann in Mikroschaumbläschen verwandelt werden, wo es benötigt wird. Jeder Tropfen hat einen flüssigen Kern aus Perfluorpentan, umgeben von einer wässrigen Lösung eines lichtabsorbierenden Farbstoffs (Indocyaningrün) und stabilisiert durch eine Tensidschicht. Bei Körpertemperatur und normalen Ultraschallpegeln verbleiben diese Tropfen als harmlose, stabile nanoskalige Kugeln, die lange zirkulieren. Wird ein kurzer Puls nahinfraroten Laserlichts auf das Untersuchungsgebiet gerichtet, erwärmt sich der Farbstoff leicht, sodass der Kern verdampft und zu einer Gasblase aufschäumt, die Ultraschall stark reflektiert. Durch Anpassung der Laserenergie konnte das Team steuern, wie viele Tropfen konvertieren, und erreichte eine siebenfach niedrigere Lichtdosis als frühere lichtaktivierte Tropfensysteme, während weiterhin starke Ultraschall- und photoakustische Signale erzeugt wurden.
Von ausgelösten Blasen zu superauflösenden Karten
Um diesen Effekt in eine praktische Bildgebungsmethode zu überführen, bauten die Forschenden ein System, das Laserpulse mit Serien ultraflacher Ultraschallaufnahmen verknüpft. Nach einer einzigen intravenösen Injektion von Nanotropfen in Mäuse feuerte das System wiederholt einen niedrigfrequenten Laserimpuls ab und erfasste sofort Hunderte Ultraschallbilder, während die neu entstandenen Mikroschaumbläschen entlang der Blutgefäße schwammen. Mithilfe fortschrittlicher Filter zur Entfernung des Hintergrundgewebesignals, gefolgt von Lokalisationsalgorithmen, bestimmten sie die Position einzelner Bläschen Bild für Bild und stapelten diese Positionen über die Zeit zu einer feingliedrigen Karte des Mikrogefäßsystems. Im Mausgehirn zeigte diese photoaktivierte Ultraschall-Lokalisationsbildgebung (PaUL) Gefäße bis zu etwa 21 Mikrometern — ungefähr ein Viertel der Breite eines menschlichen Haares — durch intakte Haut und Schädel hindurch, mit schärferem Kontrast als beim üblichen Power-Doppler-Ultraschall.
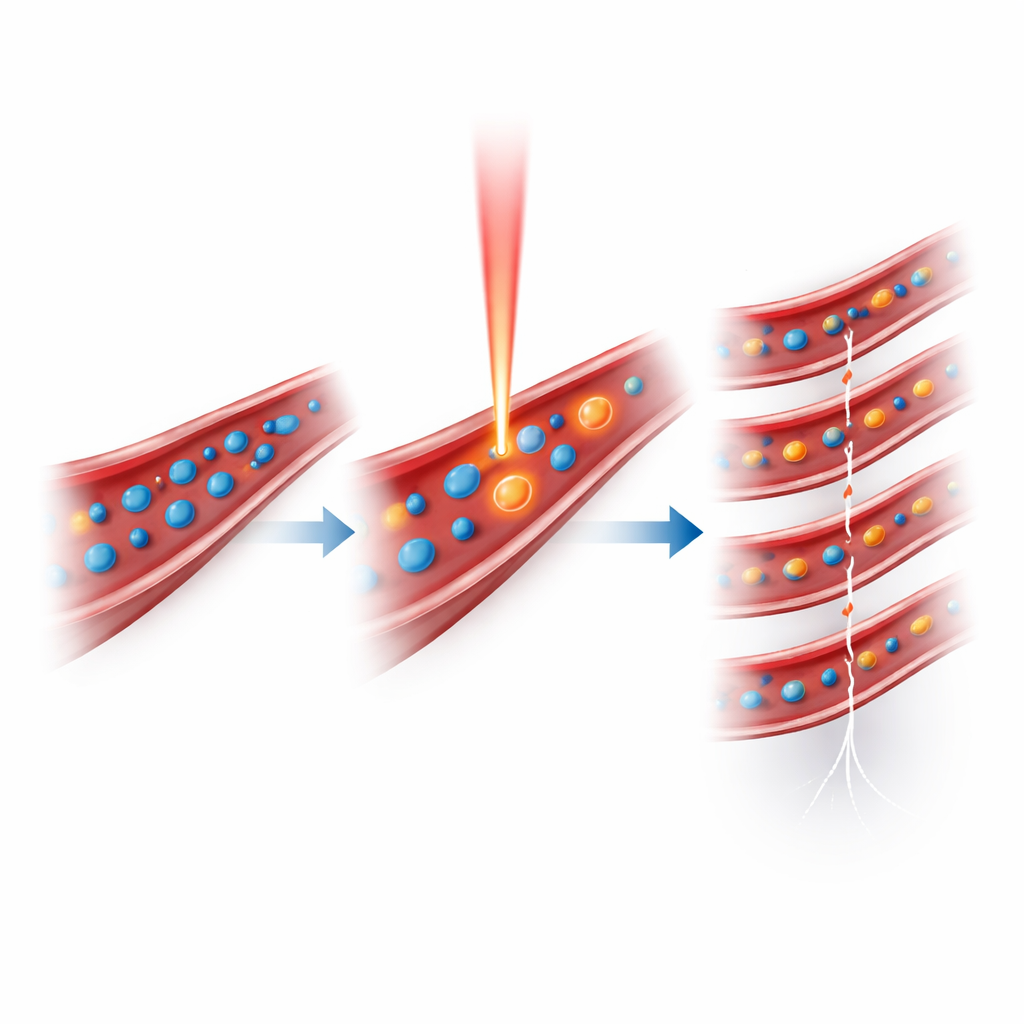
Schnellere Aufnahmen und längere Bildgebungsfenster
Weil Nanotropfen vor der Aktivierung viel kleiner sind als konventionelle Mikroschaumbläschen, können sie in feinere Kapillaren gelangen und gezielt in ausgewählten Regionen ausgelöst werden. In direkten Vergleichen rekonstruierte die PaUL-Bildgebung detaillierte Gehirngefäßnetzwerke etwa 2,4-mal schneller als die herkömmliche mikroschaumblasenbasierte Lokalisationsbildgebung, dank der höheren Dichte lokalisierter Ereignisse in kleinen Gefäßen. Die Methode erzeugte außerdem hämodynamische Karten — die Flussgeschwindigkeiten anzeigen — mit vergleichbarer Genauigkeit wie die Standardtechnik, jedoch mit dichterer Abtastung und längeren nachverfolgbaren Bahnen für einzelne Bläschen. Wichtig ist, dass die Nanotropfen deutlich länger zirkulierten: Während Mikroschaumblasen-Signale innerhalb weniger Minuten stark nachließen, blieben Signale aus Nanotropfen länger als 20 Minuten stark erhalten. Das ermöglichte bis zu dreimal mehr Lokalisationsereignisse und erlaubte den Forschenden, mehrere Gehirnregionen nacheinander ohne erneute Injektion zu scannen.
Mögliche Anwendungen und künftige Verbesserungen
Die Ergebnisse deuten darauf hin, dass lichtaktivierte Nanotropfen flexible, hochauflösende Bildgebung winziger Gefäße über längere Zeiträume ermöglichen könnten, was besonders wertvoll für das Studium der Hirnfunktion, die Überwachung von Schlaganfällen oder die Beurteilung der Tumorperfusion sein könnte. Dieselben Tropfen erzeugen auch photoakustischen Kontrast, so dass sich gleichzeitig Sauerstoffsättung und Farbstoffverteilung neben Gefäßstruktur und Fluss kartieren lassen. Die Autor:innen weisen darauf hin, dass die aktuelle Leistungsfähigkeit durch die Eindringtiefe des Lichts begrenzt ist, wodurch die effizienteste Aktivierung auf Tiefen von wenigen Millimetern beschränkt bleibt. Sie skizzieren jedoch mehrere Wege, um tiefer zu kommen: bessere Lichtzuführungsgeometrien, Farbstoffe, die in stärker durchdringenden Wellenlängenbereichen absorbieren, und minimal invasive faserbasierte Beleuchtung. Mit künftigen Verbesserungen und Sicherheitsstudien könnte die PaUL-Bildgebung bestehende Ultraschall- und photoakustische Werkzeuge ergänzen und letztlich bildgeführte Therapien wie gezielte Medikamentenabgabe unterstützen, bei denen Ärzt:innen Kontrast- oder Wirkstoffträger nur in den Regionen aktivieren, die sie benötigen.
Was das für Patientinnen und Patienten bedeutet
Einfach ausgedrückt verwandelt diese Arbeit die Ultraschallbildgebung in etwas, das eher wie eine steuerbare Taschenlampe im Blutkreislauf wirkt: winzige Tropfen bleiben stumm, bis ein Lichtpuls ihnen sagt, für den Ultraschall „aufzuleuchten“. Diese Steuerbarkeit macht es möglich, kleinere Gefäße deutlicher zu sehen, die Blutströmung länger zu verfolgen und potenziell präzisionsgesteuerte Behandlungen mit weniger Injektionen und geringeren Energieniveaus zu unterstützen. Zwar sind weitere Tests vor einer Anwendung beim Menschen nötig, doch der Ansatz weist in Richtung sichererer, aussagekräftigerer Aufnahmen der kleinsten und wichtigsten Verkehrsadern des Körpers — der Mikrovaskulatur, die unsere Organe und Tumoren versorgt.
Zitation: Zhao, S., Yi, J., Qiu, Y. et al. Photo-activated ultrasound localization imaging with laser-activated nanodroplets. Commun Eng 5, 43 (2026). https://doi.org/10.1038/s44172-026-00592-w
Schlüsselwörter: Ultraschallbildgebung, Mikrogefäßsystem, Nanotropfen, photoakustische Bildgebung, Hirndurchblutung