Clear Sky Science · de
Multi-Kontrast-Magnetic-Particle-Imaging für tomographische pH-Überwachung mit stimuli-responsiven Hydrogelen
Warum die Messung der Säuretiefe im Körper wichtig ist
Ärzte wissen, dass subtile Änderungen der Säure — gemessen als pH — oft frühzeitig auf Probleme hinweisen, noch bevor andere Symptome auftreten. Entzündete Gewebe, infizierte Implantate und wachsende Tumoren können alle ihren lokalen pH-Wert verschieben, doch ist es derzeit schwierig, diesen sicher und präzise im Körperinneren zu messen. Diese Arbeit stellt eine Machbarkeitsstudie einer Bildgebungsmethode vor, die Klinikern eines Tages erlauben könnte, pH tief im Körper ohne Nadeln oder Strahlung zu „sehen“, indem winzige magnetische Partikel in intelligenten Gelen verwendet werden.
Ein neuer Weg, magnetische Partikel sichtbar zu machen
Magnetic Particle Imaging (MPI) ist eine aufkommende medizinische Bildgebungstechnologie, die nicht direkt die Anatomie abbildet. Stattdessen detektiert sie ausschließlich speziell entwickelte magnetische Nanopartikel, die in den Körper injiziert oder implantiert werden. Anders als bei der MRT, bei der das Gewebe das Signal erzeugt und Kontrastmittel es nur verändern, sind bei MPI die Partikel selbst die einzige Signalquelle. Das ermöglicht, sie sehr präzise zu zählen und zu verfolgen. In den letzten Jahren haben Forschende MPI zu einem „Multi-Kontrast“-Werkzeug weiterentwickelt, bei dem Veränderungen in der Umgebung der Partikel — etwa Temperatur oder Flüssigkeitsdicke — das Signal auf messbare Weise beeinflussen. Die vorliegende Arbeit ergänzt diese Liste um einen weiteren wichtigen Umweltfaktor: den pH-Wert.
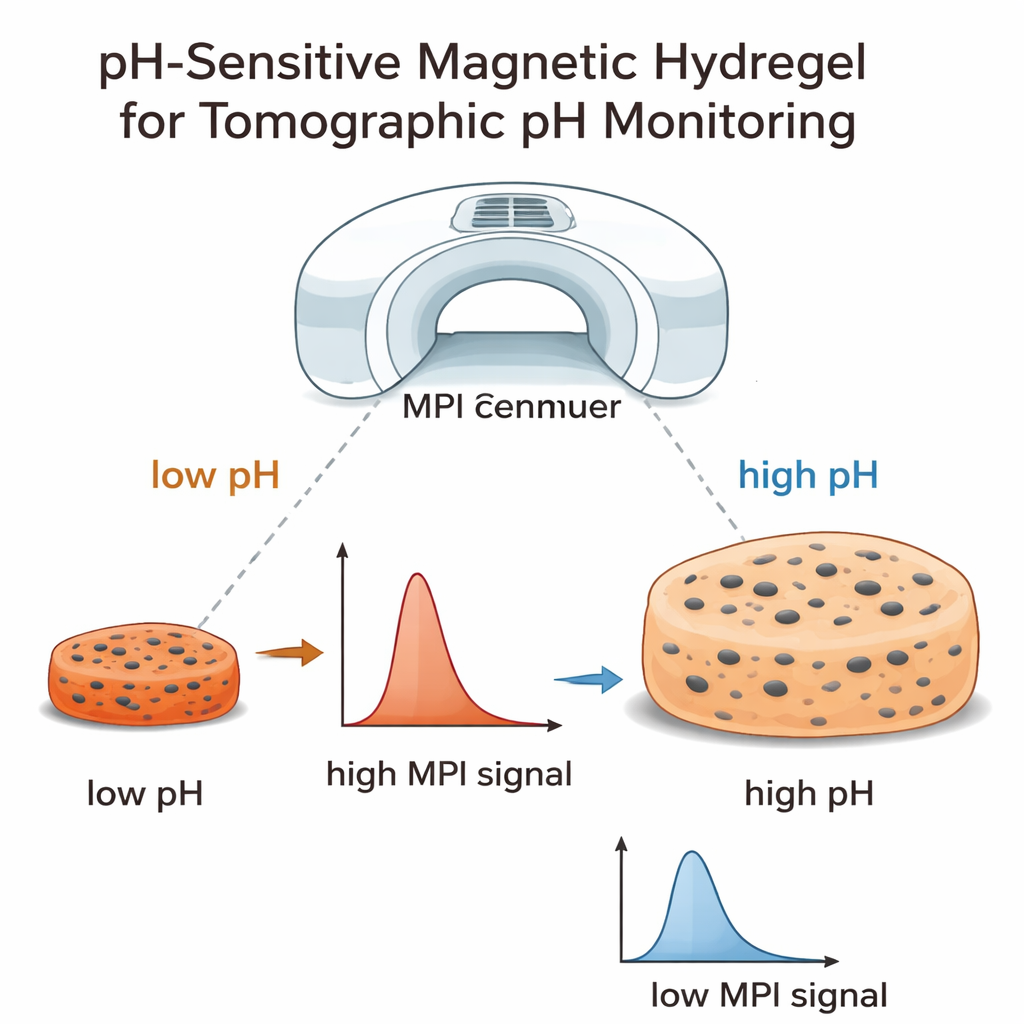
Intelligente Gele, die sich mit Säure ausdehnen
Der Schlüsselbestandteil dieser Studie ist ein weiches, wasserliebendes Material, das als Hydrogel bekannt ist. Das Team verwendete ein synthetisches Hydrogel, das chemische Gruppen enthält, die je nach pH-Wert Ladung aufnehmen oder abgeben. Bei niedrigem pH (saurer) sind diese Gruppen weniger geladen und das Gel bleibt relativ kompakt. Bei höherem pH (basischer) werden sie stark geladen und stoßen sich gegenseitig ab, sodass das Gel stark anschwillt, mehr Wasser aufnimmt und sein Volumen um mehrere hundert Prozent vergrößert. Durch das Einlagern dieser Gele in eine Lösung mit superparamagnetischen Eisenoxid-Nanopartikeln verwandelten die Forschenden sie in winzige magnetische pH-Sensoren. In sauren Lösungen sind die Partikel dicht in engem Volumen gepackt; in basischen Lösungen dehnt sich das Gel aus und die Partikel verteilen sich weiter.
Wie das Anschwellen das magnetische Signal verändert
Um zu testen, wie sich das Anschwellen auf das von einem MPI-Scanner wahrgenommene Signal auswirkt, nutzte das Team zunächst eine begleitende Methode namens magnetische Partikelspektrometrie. Sie maßen die magnetische Antwort trockener Gele und von Gele, die bei unterschiedlichen pH-Werten angeschwollen waren. Mit steigendem pH und zunehmendem Anschwellen der Gele wurde das gemessene Signal schwächer und das Frequenzspektrum des Signals schmaler. Mit anderen Worten: Je stärker das Gel sich ausdehnte, desto weniger starke „Obertöne“ nahm der Detektor wahr. Dieses Verhalten spiegelt vermutlich Veränderungen in der Wechselwirkung der Partikel untereinander und mit dem Gelnetzwerk wider, wenn sich ihre Abstände vergrößern. Wichtig ist, dass der Effekt reproduzierbar war und einen klaren, statistisch signifikanten Trend zeigte: Im medizinisch relevanten sauren Bereich führte höherer pH zu stärkerem Anschwellen und zu einem niedrigeren magnetischen Signal, mit einer einigermaßen linearen Beziehung.
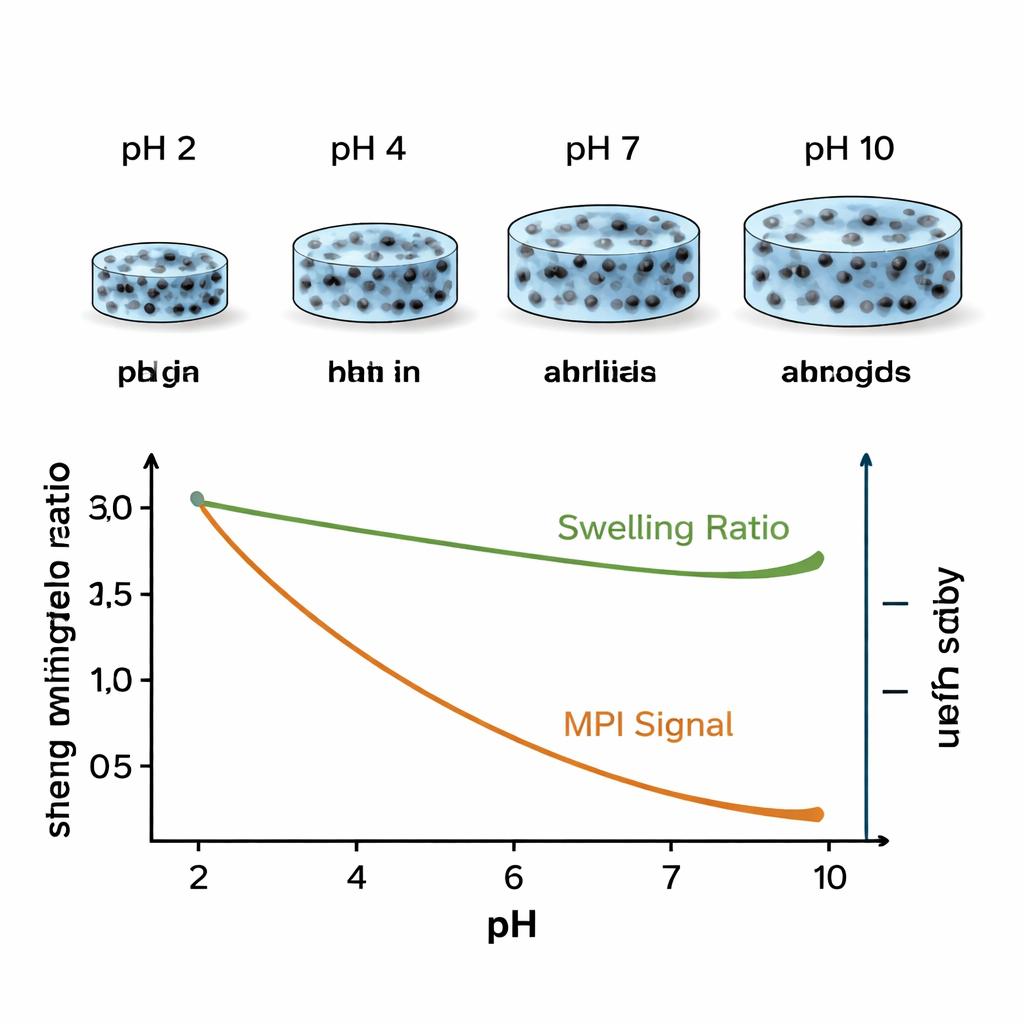
Signaländerungen in pH-Karten umwandeln
Im nächsten Schritt zeigten die Forschenden, dass sich diese Signalunterschiede in Bilder umsetzen lassen, die pH-Werte unterscheiden. Sie platzierten mehrere Gelpatches in einem 3D-gedruckten Halter und ließen sie in Lösungen mit verschiedenen pH-Werten anschwellen. Mit einem präklinischen MPI-Scanner erfassten sie Bilder und nahmen gleichzeitig separate „Systemmatrizen“ für Gele auf, die bei bestimmten Referenz-pH-Werten gehalten wurden. Durch die Rekonstruktion der Bilder mit mehreren Kanälen — je einer auf jeden Referenz-pH abgestimmt — konnten sie verschiedenen pH-Antworten unterschiedliche Farben zuweisen. In diesen Mehrfarbenbildern leuchteten Gele in sauren Lösungen in den entsprechenden Kanälen stark auf, während Gele in basischeren Lösungen entweder schwächer erschienen oder bei sehr hohem pH mit der aktuellen Messanordnung nahezu verschwanden, weil ihr Signal zu klein war. Dies bestätigte, dass MPI zumindest für gut getrennte pH-Werte wie 2, 4 und 7 pH räumlich unterscheiden kann.
Wohin das in der Medizin führen könnte
Zusammenfassend zeigt diese Arbeit, dass pH-reaktive magnetische Hydrogele unsichtbare chemische Säure in ein magnetisches Signal umwandeln können, das MPI-Scanner detektieren und separieren können. Die Autoren demonstrieren, dass im für Krankheiten relevanten sauren Bereich Gelanschwellung und Änderung des magnetischen Signals den pH auf vorhersagbare Weise abbilden und als unterschiedliche Farben in einem Bild sichtbar machen. Obwohl es sich um eine frühe Laborstudie mit Millimeter-großen Patches handelt, bildet sie die Grundlage für künftige miniaturisierte Sensoren, die injiziert oder implantiert werden könnten, um Entzündungen, Infektionen oder Tumorumgebungen nichtinvasiv zu überwachen. Mit weiterer Verfeinerung zur Verbesserung der Empfindlichkeit im Bereich des normalen Körper-pH und zur Erfassung kleiner pH-Verschiebungen könnte dieser Ansatz der MPI eine „chemische Sicht“ hinzufügen und es Klinikern ermöglichen, nicht nur zu sehen, wo Gewebe sind, sondern auch wie krank sie aufgrund ihrer lokalen Säure sein könnten.
Zitation: Kluwe, B., Ackers, J., Graeser, M. et al. Multi-contrast magnetic particle imaging for tomographic pH monitoring using stimuli-responsive hydrogels. Commun Eng 5, 33 (2026). https://doi.org/10.1038/s44172-026-00586-8
Schlüsselwörter: magnetic particle imaging, pH-Sensorik, intelligente Hydrogele, Nanopartikelbildgebung, nichtinvasive Diagnostik