Clear Sky Science · de
Abschwächung der epikardialen Aktivierung und Myofibroblasten‑Fülle über die Fbln2–Nupr1b‑Achse fördert die Herzerneuerung bei Zebrafischen
Warum einige Herzen sich selbst heilen können
Wenn ein Mensch einen Herzinfarkt erleidet, wird das beschädigte Muskelgewebe meist durch eine steife Narbe überzogen, die sich nie vollständig regeneriert. Zebrafische, die kleinen gestreiften Aquarienfische, verhalten sich bemerkenswert anders: Sie wachsen Herzgewebe nach und bauen einen Großteil der Narbe schließlich wieder ab. Diese Studie stellt eine auf den ersten Blick einfache Frage mit großen medizinischen Auswirkungen: Wie weiß ein heilendes Herz, wann es Narbengewebe aufbauen und wann es dieses wieder entfernen soll, damit neues Muskelgewebe entstehen kann? Indem sie dieses Gleichgewicht bei Zebrafischen entschlüsselt, weist die Arbeit auf Strategien hin, die eines Tages verletzten menschlichen Herzen helfen könnten, sich selbst zu reparieren, statt zu versagen.
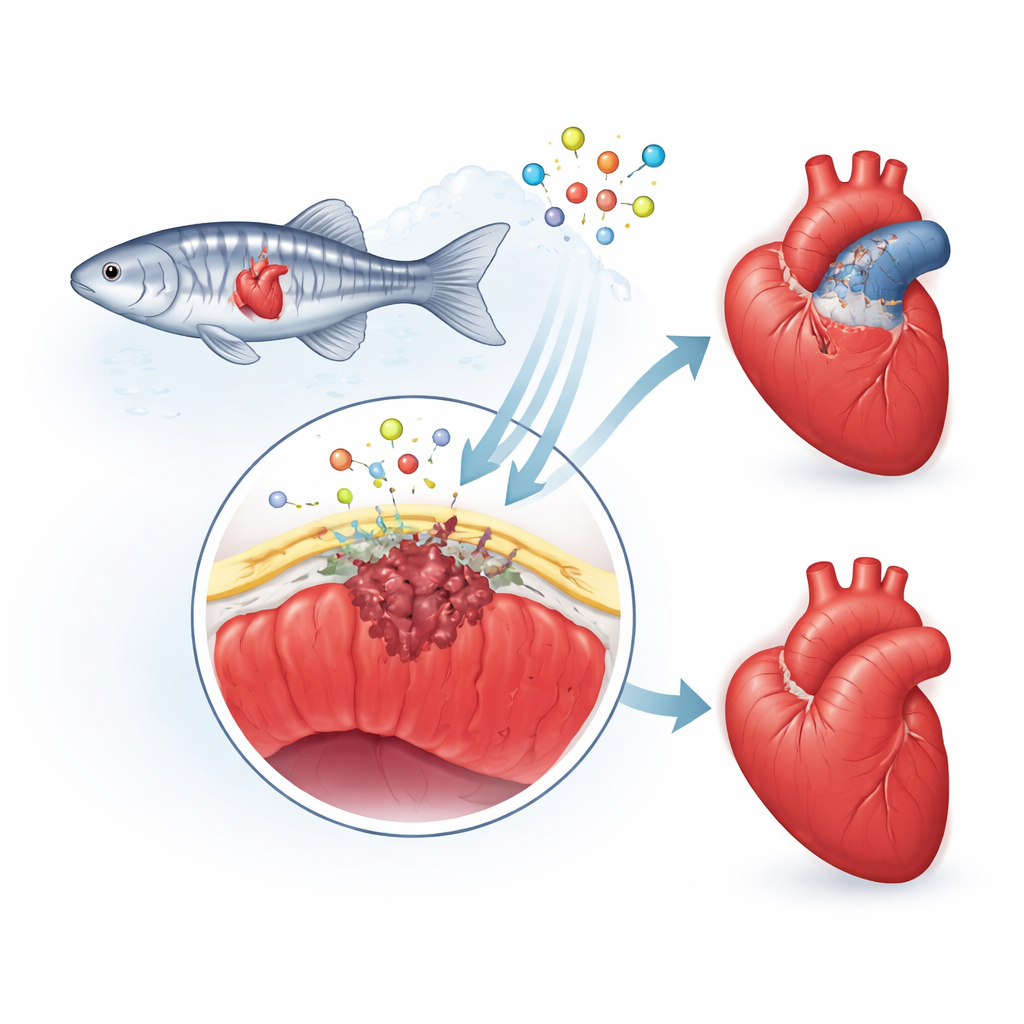
Die schützende Außenhaut des Herzens
Die Forschenden konzentrieren sich auf das Epikard, eine dünne „Haut“, die das Herz überzieht. Nach einer Verletzung erwacht diese Schicht, ihre Zellen ändern ihre Identität und einige dringen in den beschädigten Bereich ein. Dort werden sie zu Unterstützungs‑ und narbenbildenden Zellen und geben chemische Signale ab, die neues Gefäß- und Herzmuskelwachstum leiten. Beim Menschen läuft diese Reparaturreaktion oft über das Ziel hinaus und hinterlässt eine dicke, dauerhafte Narbe. Beim Zebrafisch hingegen ist die Narbe vorübergehend und wird nach und nach abgebaut, sobald gesundes Muskelgewebe zurückkehrt. Das Team vermutete, dass ein Protein namens Fibulin‑2 (Fbln2), das im umgebenden Gerüst des Herzens vorkommt, die Geschwindigkeit und Intensität dieser epikardialen Reaktion mitbestimmt.
Ein molekularer Dimmer für die Narbenbildung
Mit Geneditierung in Zebrafischen erzeugten die Wissenschaftler zwei Tierlinien mit unterschiedlichen Fbln2‑Spiegeln: eine Linie mit reduziertem Fbln2 und eine andere ganz ohne das Protein. Sie verletzten die Fischherzen mit einer Gefrier‑Sonde, um einen Herzinfarkt zu imitieren, und verfolgten die Heilung über Wochen bis Monate. Bei vermindertem Fbln2 fiel die frühe Zellteilung im Herzmuskel und in der Gefäßauskleidung ab, doch die entstandene faserige Narbe war kleiner und ließ sich leichter umgestalten. Nach drei Monaten hatten diese Herzen gut regeneriert und wiesen nur wenig Kollagen auf, das Hauptmaterial der Narbe. Im Gegensatz dazu zeigten Fische ohne Fbln2 einen stärkeren Stillstand eines wichtigen Wachstums‑ und Narbenbildungswegs, an dem die Signalfamilie TGFβ beteiligt ist, und deutlich weniger narbenbildende Zellen direkt unter dem Epikard. Ihre frühen Narben waren ebenfalls kleiner – später jedoch gelang es diesen Herzen nicht, Kollagen abzubauen, sodass große, dauerhafte Narben und eine schlechte Regeneration zurückblieben.
Ein Blick auf epikardiale Zustandsänderungen
Um zu sehen, wie sich epikardiale Zellen auf Einzelzellniveau verhielten, verwendete das Team kurz nach der Verletzung Einzelzell‑RNA‑Sequenzierung. Sie identifizierten mehrere epikardiale Zell„zustände“, darunter ruhende Zellen, neu aktivierte Zellen, gestresste Zellen, die sich an niedrigen Sauerstoff anpassen, und Zellen, die sich aktiv teilten. Bei Fischen mit normalem Fbln2 durchliefen die epikardialen Zellen einen glatten Übergang von ruhend zu aktiviert bis hin zu reiferen Zuständen. Bei Fischen mit reduziertem oder fehlendem Fbln2 stockte dieser Verlauf: Zellen verharrten in frühen Stadien und die reiferen aktivierten Gruppen waren unterrepräsentiert, besonders bei vollständigem Verlust. Zahlreiche Gene, die normalerweise während der epikardialen Aktivierung und als Reaktion auf TGFβ‑Signale hochreguliert werden, waren abgeschwächt, was Fbln2 als Stellglied dieses Signalwegs nahelegt, das darüber entscheidet, wie stark das Epikard sich der Narbenbildung und -umgestaltung verpflichtet.
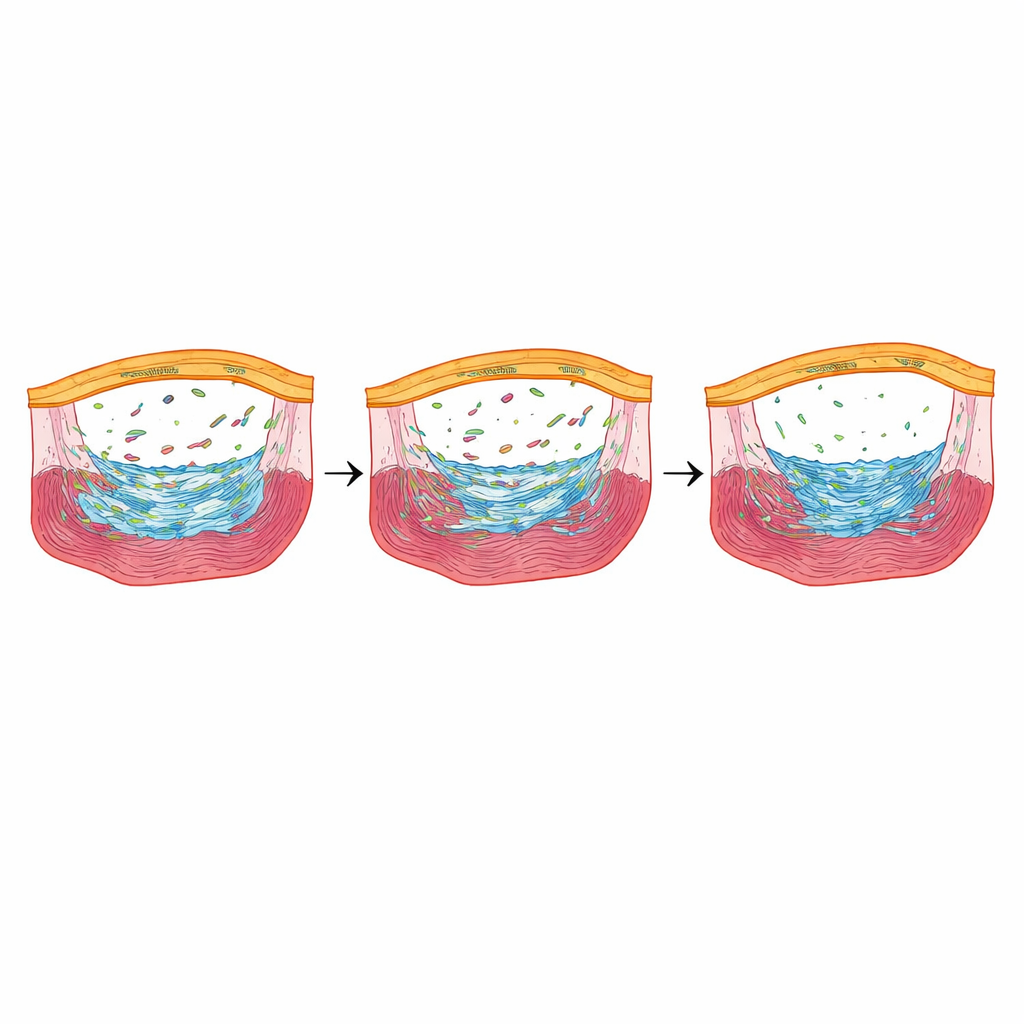
Ein Stress‑Rezeptor, der die Reparatur feinjustiert
Unter den Genen, die bei reduziertem Fbln2 am stärksten reduziert waren, stach eines hervor: nupr1b, ein stressantwortabhängiger Regulator, der in epikardialen Zellen während der frühen Heilung aktiv ist. Als die Forschenden nupr1b entfernten, zeigten Zebrafische weniger epikardiale narbenbildende Zellen und eine verringerte Teilung der Herzmuskelzellen, und sie behielten Monate nach der Verletzung große Kollagenablagerungen – ähnlich wie die Fische ohne Fbln2. Bemerkenswerterweise erholten sich bei kurzzeitiger Wiederaktivierung von nupr1b ausschließlich in epikardialen Zellen von Fbln2‑reduzierten Fischen die Anzahl der narbenbildenden Zellen und die Proliferation der Herzmuskelzellen, und die späte Narbenbildung nahm zu. Die chemische Blockade von TGFβ‑Rezeptoren verringerte nupr1b‑Spiegel, wodurch nupr1b nachgeschaltet in einer Fbln2–TGFβ‑Signalachse eingeordnet wird.
Was das für die Heilung des menschlichen Herzens bedeutet
Zusammen ergeben diese Befunde eine „epikardiale Fbln2–Nupr1b‑Achse“, die Zebrafischherzen hilft, ein Gleichgewicht zwischen zu wenig und zu viel Fibrose zu halten. Eine leichte Dämpfung dieser Achse zügelt den frühen Narbenstoß und begünstigt einen effizienten Narbenabbau, während ein vollständiges Abschalten die Regeneration entgleisen lässt und eine starre Narbe zurücklässt. Für die humanmedizinische Anwendung lautet die Lektion: Ziel ist es nicht, die Narbenbildung vollständig zu blockieren, sondern sie fein abzustimmen – ausreichend Struktur zu belassen, um Rupturen zu verhindern, und zugleich sicherzustellen, dass das Narbengewebe vorübergehend ist und durch gesundes Muskelgewebe ersetzt werden kann. Das Verständnis und die mögliche Nutzung dieses Kontrollsystems aus Zebrafischen könnte künftige Therapien informieren, die das verletzte menschliche Herz eher zur echten Regeneration als zur chronischen Vernarbung bewegen.
Zitation: Kayman Kürekçi, G., Kaur Bajwa, G., Zhang, S. et al. Attenuation of epicardial activation and myofibroblast abundance via the Fbln2–Nupr1b axis stimulates cardiac regeneration in zebrafish. Nat Cardiovasc Res 5, 218–233 (2026). https://doi.org/10.1038/s44161-026-00785-8
Schlüsselwörter: Herzregeneration, Fibrose, Zebrafisch, Epikard, TGF‑beta‑Signalgebung