Clear Sky Science · de
Selektive Blockade der Aktivierung von latentem TGF-β1 unterdrückt Gewebefibrose bei guter Sicherheit
Warum versteckte Vernarbung wichtig ist
Viele chronische Erkrankungen schädigen unsere Organe im Verborgenen, indem sie starres Narbengewebe ablagern – ein Prozess, der als Fibrose bezeichnet wird. Diese Vernarbung kann die normale Funktion von Leber, Nieren, Lunge und sogar das Gewebe um Tumoren herum allmählich ersticken; dort kann sie zudem die Wirkung moderner Krebsimmuntherapien abschwächen. Das Protein TGF-β1 steht im Zentrum dieses Vernarbungsprozesses, doch ein generelles Abschalten im ganzen Körper erwies sich als gefährlich. Diese Studie beschreibt einen neuen Antikörper namens SOF10, der so konstruiert ist, nur die schädliche Aktivierung von TGF-β1 zu blockieren, während seine wesentlichen Funktionen erhalten bleiben; in Tiermodellen von Lebererkrankung, Nierenversagen und Krebs zeigte er vielversprechende Wirkungen.
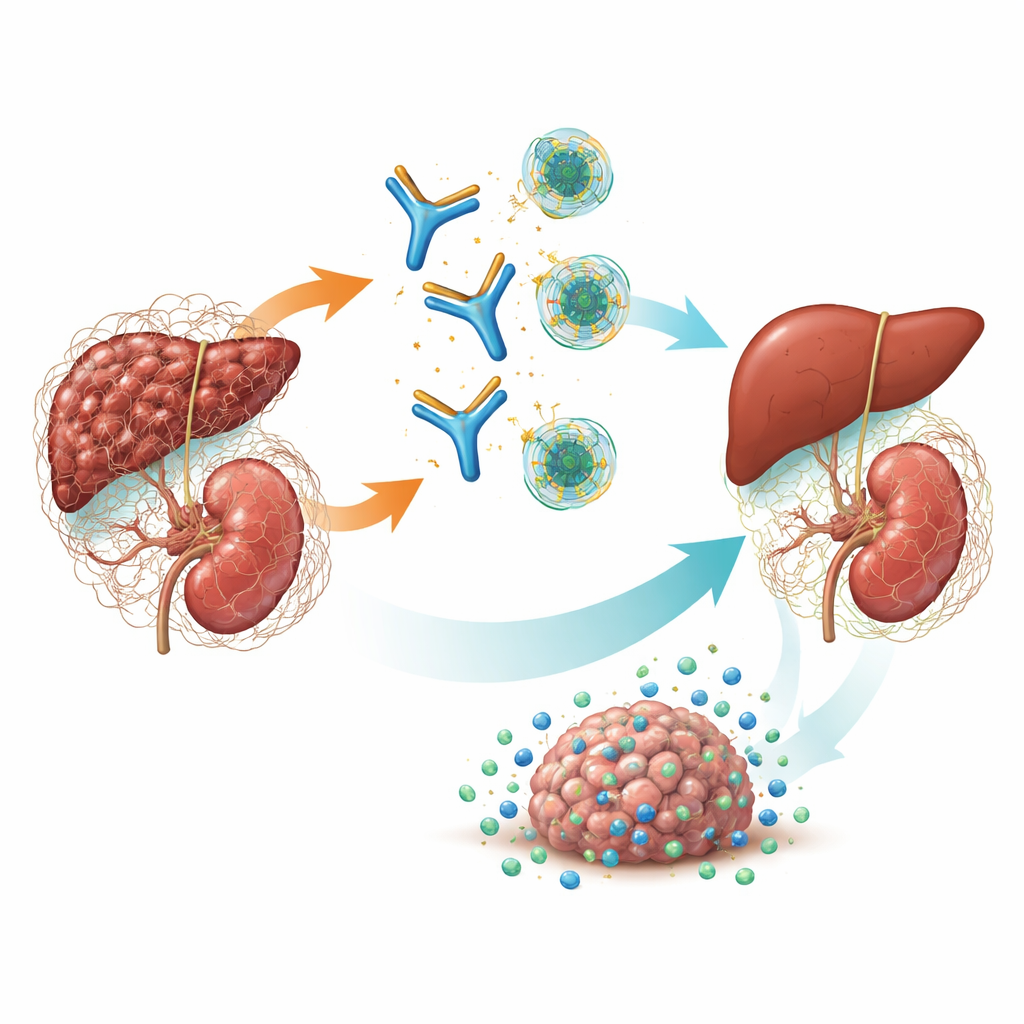
Ein Hauptschalter für Vernarbung und Krebs
TGF-β ist ein starkes Signalmolekül, das das Zellwachstum, die Heilung und die Wechselwirkung mit dem Immunsystem steuert. Bei chronischen Erkrankungen treibt eine Form—TGF-β1—Fibroblasten dazu, überschüssiges Bindegewebe aufzubauen, was zur Versteifung und zum Versagen von Organen führt. Gleichzeitig formt es eine immununterdrückende, fibrotische Hülle um Tumoren, die Immunzellen und Medikamente davon abhält, Krebszellen zu erreichen. Frühere Wirkstoffe versuchten, alle drei TGF-β‑Formen gleichzeitig zu blockieren, doch diese „Pan‑Blockade“ verursachte schwerwiegende Nebenwirkungen wie Herzklappenschäden, Blutungen und Hauttumoren. Genetische Studien und frühere Modelle deuteten darauf hin, dass TGF-β1 der Hauptverursacher bei fibrotischen Nierenerkrankungen und vielen soliden Tumoren ist, sodass die gezielte Blockade nur dieses Isoforms sowohl effektiv als auch sicherer sein könnte.
TGF-β1 in seiner inaktiven Form einklemmen
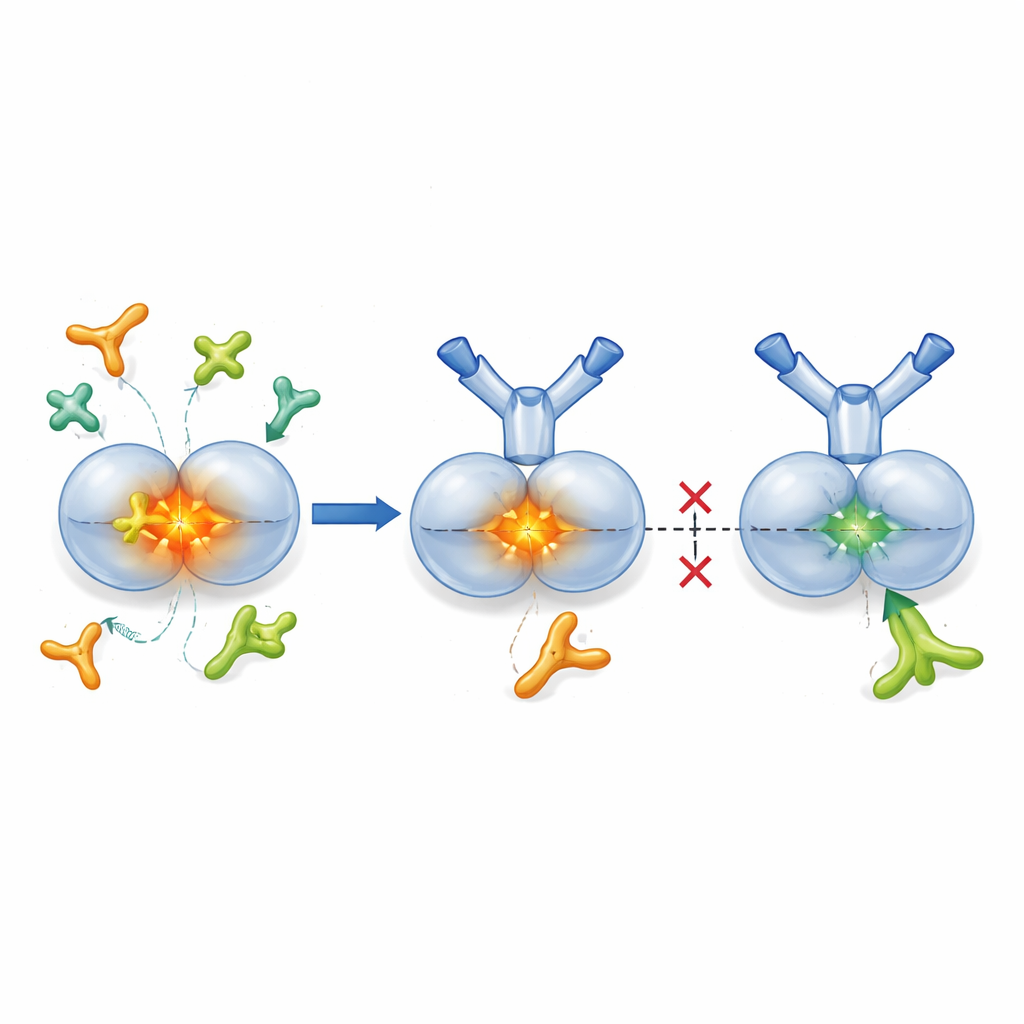
TGF-β1 wird üblicherweise in einem „latenten“ Paket produziert, wobei der aktive Kern von einem Partnerprotein umhüllt ist, das ihn inaktiv hält, bis er benötigt wird. Proteasen und bestimmte zelloberflächengebundene Haftproteine, sogenannte Integrine, können dieses Paket öffnen und aktives TGF-β1 in das umliegende Gewebe freisetzen. Die Forscher entwickelten SOF10, einen humanisierten Antikörper, der ausschließlich an die latente Form von TGF-β1 bindet, nicht an das aktive Hormon oder andere Isoformen. Strukturelle Untersuchungen mittels Röntgenkristallographie zeigten, dass SOF10 in die Schnittstelle zwischen den beiden Hälften des latenten Komplexes hineinragt und diesen wie eine Klammer stabilisiert. In Laborversuchen verhinderte dies, dass Proteasen und ein Integrin (αvβ8) aktives TGF-β1 freisetzen, während ein anderes Integrin (αvβ6) – das wichtig für die Aufrechterhaltung des Immungleichgewichts in gesunden Geweben ist – weitgehend unberührt blieb. Effektiv stilllegt SOF10 selektiv die schädlichen Aktivierungswege und schont gleichzeitig einen zentralen homöostatischen Pfad.
Leber und Nieren vor schleichendem Schaden schützen
Um zu prüfen, ob diese selektive Klammer um TGF-β1 tatsächlich die Vernarbung begrenzen kann, testete das Team SOF10 in mehreren Mausmodellen. In einem schnellen, diätinduzierten Modell der Fettlebererkrankung, das zur Leberfibrose fortschreitet, reduzierte SOF10 die Expression von TGF-β‑induzierten Genen und Kollagenaufbaugenen in der Leber und senkte die Hydroxyprolinwerte, einen chemischen Marker akkumulierten Narbengewebes. In zwei verschiedenen Nierenmodellen—einem chirurgischen Obstruktionsmodell, das interstitielle Fibrose antreibt, und einem genetischen Alport‑Syndrom‑Modell, das sowohl glomeruläre Vernarbung als auch Nierenversagen entwickelt—senkte SOF10 die fibrotische Genaktivität, verringerte den Kollagengehalt und verkleinerte unter dem Mikroskop sichtbar die vernarbten Bereiche. Im chronischen Alport‑Modell zeigten Blutwerte eine verbesserte Nierenfunktion, und diese Vorteile waren mit denen eines breiter wirkenden TGF-β‑blockierenden Antikörpers vergleichbar, jedoch ohne Blockade anderer TGF-β‑Isoformen.
Das Immunsystem im Tumor befreien
Da fibrotisches Gewebe um Tumoren sowohl als physische Barriere als auch als immunologische Bremse wirken kann, untersuchten die Forscher, ob SOF10 die Ansprechraten auf Checkpoint‑Inhibitoren verbessern kann. In Mausmodellen für Brust‑ und Darmkrebs, die normalerweise schlecht auf Anti‑PD‑L1‑Therapie ansprechen, verlangsamte die Zugabe von SOF10 das Tumorwachstum deutlich, während SOF10 oder Anti‑PD‑L1 allein wenig Effekt hatten. Tumoren aus kombinationsbehandelten Tieren enthielten mehr killerfähige CD8‑T‑Zellen und mehr der toxischen Enzyme, mit denen diese Zellen Krebszellen zerstören. Aus diesen Tumoren isolierte Fibroblasten zeigten geringere Aktivität in Kollagen‑ und matrixaufbauenden Pfaden, aber höhere Aktivität in Interferon‑ und Antigenpräsentationswegen – eine Verschiebung hin zu einem immununterstützenden Stroma. Diese Veränderungen spiegelten weitgehend das wider, was bei einer breiten TGF-β‑Blockade beobachtet wurde, und deuten darauf hin, dass die gezielte Blockade von latentem TGF-β1 allein die Tumorumgebung ähnlich umprogrammieren kann.
Sicherheitssignale in Tieren
Da frühere Versuche, TGF-β breit zu blockieren, auf Sicherheitsprobleme gestoßen waren, führte das Team 13‑wöchige Toxizitätsstudien an Mäusen und Zynomolgusaffen durch und verabreichte wiederholt hohe Dosen von SOF10. Der Wirkstoff verhielt sich im Blutkreislauf wie ein typischer Antikörper, und über einen weiten Dosisbereich waren keine Anzeichen von Schäden in wichtigen Organen, keine Veränderungen der Blutbildwerte oder Beeinträchtigungen von Herz‑ und Lungenfunktion zu sehen. Die höchsten getesteten Dosen—bis zu 200 mg/kg alle zwei Wochen bei Mäusen und 100 mg/kg bei Affen—wurden als Bereiche ohne beobachtbare schädliche Effekte bezeichnet. Dieses Sicherheitsprofil stützt die Idee, dass das Schonend‑lassen von TGF-β2, TGF-β3 und αvβ6‑vermittelter Aktivierung die bei früheren, weniger selektiven Ansätzen beobachteten Risiken verringert.
Was das für Patienten bedeuten könnte
Insgesamt deuten die Befunde darauf hin, dass das Einklemmen von TGF-β1 in seiner inaktiven Hülle—statt eines vollständigen Ausschaltens aller TGF-β‑Signale—die Vernarbung in mehreren Organen verringern, die Nierenfunktion verbessern und hartnäckige Tumoren für die Immuntherapie empfänglicher machen kann, und das alles bei ermutigender Sicherheit in Tierversuchen. Menschliche Studien sind notwendig, um diese Vorteile zu bestätigen und Langzeiteffekte zu überwachen, doch SOF10 und ähnliche Strategien könnten einen neuen Weg eröffnen, chronische fibrotische Erkrankungen und bestimmte Krebserkrankungen zu behandeln, indem sie schädliche Vernarbung dämpfen und gleichzeitig die heilenden und immunbalancierenden Rollen des Tissues bewahren.
Zitation: Kanamori, M., Sato, I., Koo, C.X. et al. Selective blockade of latent TGF-β1 activation suppresses tissue fibrosis with good safety. Commun Med 6, 131 (2026). https://doi.org/10.1038/s43856-026-01408-w
Schlüsselwörter: Fibrose, TGF-beta1, monoklonaler Antikörper, Nieren- und Lebererkrankung, Krebsimmuntherapie