Clear Sky Science · de
Pembrolizumab und epigenetische Modifikation mit Azacitidin verändern das Tumormikromilieu bei platinresistentem epithelialem Ovarialkarzinom: eine Phase‑2‑nichtrandomisierte klinische Studie
Warum diese Studie wichtig ist
Für viele Frauen mit fortgeschrittenem Ovarialkarzinom versagt die Standardchemotherapie im Verlauf der Zeit, sodass nur wenige sinnvolle Optionen bleiben. Diese Studie untersucht eine neue Strategie: die Kombination einer immunbasierten Behandlung mit einem Medikament, das Krebszellen „umprogrammieren“ kann, in der Hoffnung, einen bislang ruhigen, schwer erkennbaren Tumor in einen für das Immunsystem sichtbaren und angreifbaren Tumor zu verwandeln. Zu klären, ob dieser Ansatz sicher ist, wie gut er das Tumorwachstum kontrolliert und welche Veränderungen er innerhalb der Tumoren bewirkt, könnte künftige Behandlungen für eine der tödlichsten gynäkologischen Krebserkrankungen beeinflussen.
Eine schwer zu behandelnde Form von Eierstockkrebs
Ovarialkarzinome werden häufig in einem fortgeschrittenen Stadium diagnostiziert, und viele Tumoren entwickeln eine Resistenz gegen ein zentrales Chemotherapeutikum, Platin. Dann sind Reaktionen auf weitere Chemotherapien meist nur von kurzer Dauer. Immune-Checkpoint-Medikamente, die die Bremsen der Immunzellen lösen, haben die Behandlung mehrerer anderer Krebsarten verändert, erzielten beim Eierstockkrebs aber nur bescheidene Erfolge. Ein Grund ist, dass viele Ovarialtumoren „kalt“ sind: Sie enthalten relativ wenige aktive Immunzellen, was es schwierig macht, dass Checkpoint-Medikamente wirken. Die Forschenden dieser Studie fragten, ob sich diese Tumoren durch vorherige Veränderungen der Genregulation in den Krebszellen „aufwärmen“ lassen.
Kombination von Immuntherapie mit einem epigenetischen Wirkstoff
Das Team testete eine Kombination aus Pembrolizumab, einem weitverbreiteten Checkpoint-Inhibitor, und oralem Azacitidin, einem Mittel, das die chemischen Markierungen an der DNA beeinflusst, die die Genaktivität steuern. Durch die Veränderung dieser Markierungen kann Azacitidin stillgelegte Gene wieder aktivieren und antiviralen Alarm innerhalb von Tumorzellen auslösen. In Labor‑Modellen zieht eine solche „Viral‑Mimikry“ Immunzellen in zuvor ruhige Tumoren. In dieser Phase‑II‑Studie erhielten 34 Frauen mit platinresistentem oder platinrefraktärem epithelialem Ovarialkarzinom Pembrolizumab zusammen mit einem von vier Dosierungsschemata von Azacitidin. Alle hatten messbare Erkrankung und bereits die Standardoperation und Chemotherapie durchlaufen.
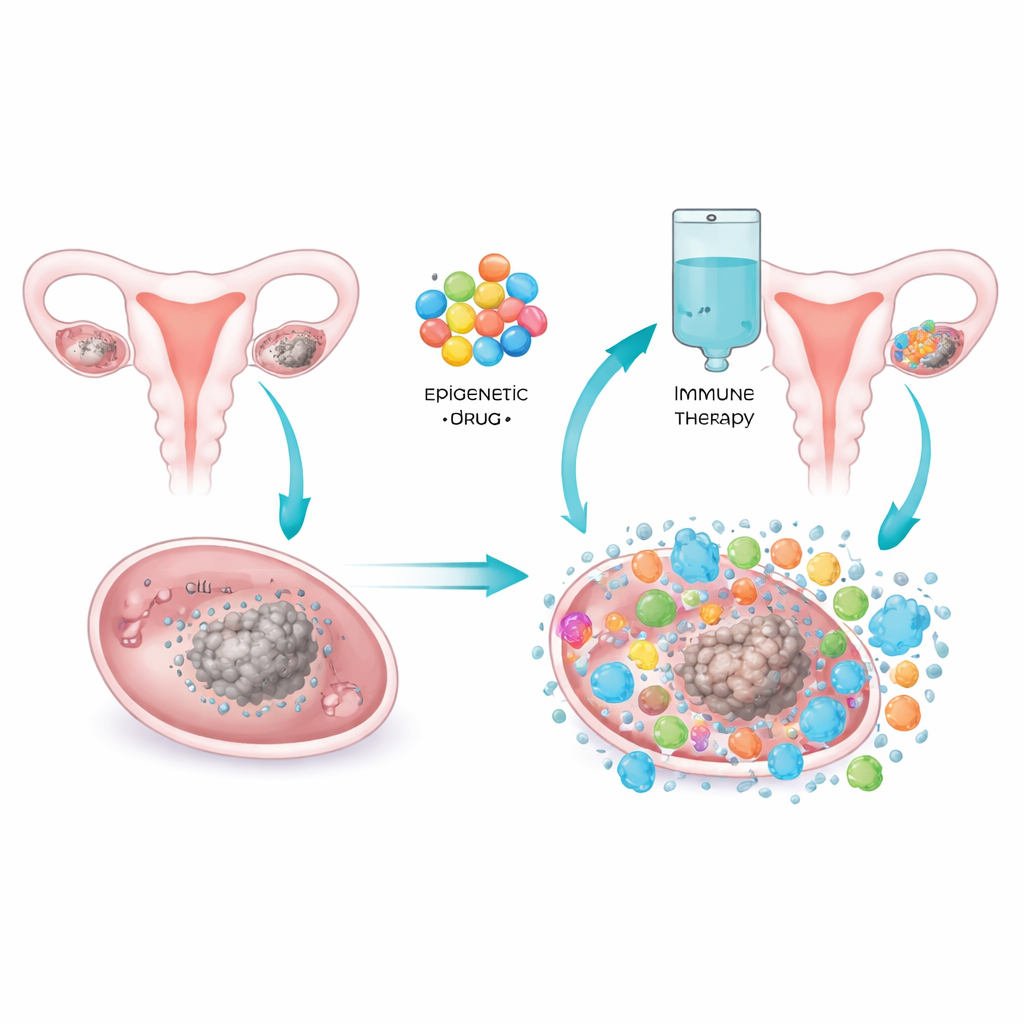
Was bei den Patientinnen geschah
Die Kombination wurde als mäßig gut verträglich eingeschätzt. Häufige Nebenwirkungen waren Übelkeit, Erbrechen, Durchfall, Müdigkeit, Anämie und verminderte weiße Blutkörperchen, besonders bei höheren Azacitidin‑Dosen. Die meisten dieser Probleme ließen sich durch Dosisanpassungen handhaben, und es traten keine unerwarteten Sicherheitsprobleme über das bekannte Nebenwirkungsprofil der einzelnen Wirkstoffe hinaus auf. Hinsichtlich Tumorverkleinerung zeigte nur eine Patientin eine partielle Remission, und keine Patientin eine komplette Remission, was einer Gesamtansprechrate von etwa 3 % entspricht. Etwa die Hälfte der Frauen verzeichnete jedoch entweder Tumorverkleinerung oder Krankheitsstabilität, sodass die Krankheitskontrollrate bei 50 % lag. Eine kleine Zahl blieb länger als ein Jahr in Behandlung, darunter eine Frau, die nach Umstellung auf Pembrolizumab allein in Remission verblieb.
Wie das Tumormilieu verändert wurde
Um zu untersuchen, was die Wirkstoffkombination innerhalb der Tumoren bewirkte, entnahmen die Forschenden Gewebeproben vor Beginn der Therapie und erneut etwa sechs Wochen nach Therapiebeginn. Sie maßeten die Aktivität von Hunderten immunbezogener Gene und sequenzierten die Tumor‑RNA, um umfassendere Veränderungen zu erfassen. Unter Therapie zeigten die Tumoren eine höhere Aktivität von Genen, die mit Entzündung, Interferon‑Signalen und der Maschinerie verbunden sind, die Tumorfragmente den Immunzellen präsentiert. Signalwege, die Immunzellen das Eindringen in und Verweilen in Tumoren erleichtern, waren ebenfalls stärker aktiv. Gleichzeitig nahm die relative Zahl tumorinfiltrierender T‑Zellen, besonders der zytotoxischen Untergruppe, zu. Diese Muster deuten darauf hin, dass sich das Tumorumfeld von einem ruhigen Zustand hin zu einem stärker entzündeten, immunbewussten Zustand verschob.
Hinweise aus den Ansprechern und Signaturen von Immunzellen
Die Untersuchenden analysierten auch Muster bei Patientinnen, die Anzeichen eines Nutzens zeigten, etwa durch Abnahmen des Blutmarkers CA‑125 oder länger anhaltende Krankheitskontrolle. Tumoren dieser Frauen wiesen tendenziell höhere Ausgangsaktivität in inflammatorischen Genprogrammen auf und zeigten nach Therapiebeginn stärkere Verstärkungen adaptiver Immunantworten—jene, die von T‑ und B‑Zellen getragen werden, die spezifische Ziele erkennen. Durch Rekonstruktion der umgestellten T‑Zell‑Rezeptoren aus Tumor‑RNA stellte das Team fest, dass sich T‑Zell‑Populationen innerhalb der Tumoren unter Therapie häufig veränderten, wobei bestimmte Klone expandierten oder schrumpften. Diese Umgestaltung der T‑Zell‑Landschaft ist ein weiteres Indiz dafür, dass die Wirkstoffkombination aktiv die immunologische Auseinandersetzung in den Tumoren neu gestaltete.
Was das für Patientinnen bedeutet
Für Frauen mit platinresistentem Ovarialkarzinom erhöhte diese spezifische Kombination aus Pembrolizumab und oralem Azacitidin nicht deutlich die Anzahl der sichtbaren Tumorverkleinerungen im Vergleich zur Immuntherapie allein. Sie kontrollierte jedoch bei rund der Hälfte der Teilnehmenden die Erkrankung und hinterließ klare molekulare Spuren, dass Tumoren entzündlicher wurden und dichter von Immunzellen besiedelt waren. Für eine breite Leserschaft lautet die Schlussfolgerung, dass die Medikamente offenbar in der Lage sind, das Immunsystem innerhalb dieser ansonsten stillen Tumoren zu „wecken“, auch wenn sich dies in dieser kleinen, stark vorbehandelten Gruppe nicht stets in großem Tumorschwund niederschlug. Die Autoren argumentieren, dass eine Verfeinerung der Dosierung, bessere Verabreichungsformen von Azacitidin und der Einsatz molekularer Marker zur Auswahl wahrscheinlich ansprechender Patientinnen diese Strategie des Immun‑Aufwärmens zu einem wichtigen Baustein künftiger Ovarialkarzinom‑Therapien machen könnte.
Zitation: Landon, B.V., Boland, J.L., Wahner Hendrickson, A.E. et al. Pembrolizumab and epigenetic modification with azacitidine reshapes the tumor microenvironment of platinum-resistant epithelial ovarian cancer: a phase 2 non-randomized clinical trial. Commun Med 6, 142 (2026). https://doi.org/10.1038/s43856-026-01404-0
Schlüsselwörter: Eierstockkrebs, Immuntherapie, epigenetische Therapie, Tumormikroumgebung, Checkpoint-Inhibitoren