Clear Sky Science · de
Genomische Charakterisierung und Sub-Clustering des Escherichia-coli-Klonkomplexes 38 enthüllen wirtsspezifische genetische Marker
Warum das im Alltag wichtig ist
Antibiotikaresistente Infektionen sind längst kein reines Krankenhausproblem mehr – sie betreffen zunehmend Lebensmittel, Tiere, Reisen und das gesellschaftliche Leben. Diese Studie konzentriert sich auf eine bestimmte Gruppe von Escherichia-coli-Bakterien, den Klonkomplex 38 (CC38), der schwere Blutstrom- und Harnwegsinfektionen verursachen kann und oft gegenüber wichtigen Antibiotika resistent ist. Indem die Forscher die Herkunft dieser Bakterien und ihre Bewegungen zwischen Menschen, Tieren und Umwelt nachvollziehen, liefern sie Hinweise, die Gesundheitsbehörden dabei helfen könnten, gefährliche Stämme zu stoppen, bevor sie sich weit verbreiten.
Ein genauerer Blick auf eine problematische Bakterienfamilie
Nicht alle E. coli sind schädlich, aber einige Linien stechen als wiederkehrende Verursacher schwerer Erkrankungen hervor. CC38 hat sich jüngst als eine dieser problematischen Gruppen etabliert und rangiert in dänischen Blutstrominfektionen nur hinter einer bekannten Hochrisiko‑Linie (ST131). Das Team untersuchte 242 resistente E.-coli-CC38-Isolate aus dänischen Patienten, 83 aus Lebensmitteln und Nutztieren sowie mehr als 2.300 verwandte Genome aus aller Welt. Mit Ganzgenomsequenzierung – also dem Auslesen der gesamten DNA jedes Bakteriums – kartierten sie, wie die Zweige dieser Familie verwandt sind, welche Resistenzgene sie tragen und in welchen Wirten sie bevorzugt vorkommen.
Der Weg von Krankenhäusern zu Höfen und Lebensmitteln
Beim Vergleich dänischer E.-coli-CC38-Isolate aus Patienten mit solchen aus Geflügel, Nutztieren und Lebensmitteln identifizierten die Forscher zwei Hauptgruppen in Dänemark. Eine Gruppe bestand überwiegend aus menschlichen Infekten, die andere enthielt Bakterien aus Geflügel, anderen Nutztieren und Lebensmitteln. Wichtig ist, dass es keine nahezu identischen DNA‑Übereinstimmungen zwischen menschlichen und tierischen Isolaten gab, was darauf hindeutet, dass es im Untersuchungszeitraum in Dänemark keine eindeutigen lebensmittelbedingten Ausbrüche gab. Statistische Modelle, die sich Neben-DNA‑Segmente (accessory genome) ansehen, deuteten jedoch darauf hin, dass einige menschlich assoziierte Untergruppen wahrscheinlich einen Geflügelursprung haben — was auf frühere oder indirekte Übertragungen von Hühnern auf Menschen hinweist.
Ein globaler Stammbaum mit zwei großen Ästen
Erweiterten die Forschenden die Analyse auf einen weltweiten Datensatz von 2.638 Genomen, konnten sie einen globalen "Stammbaum" für CC38 erstellen. Zwei große Äste fielen auf. Einer war stark mit Geflügel verknüpft und trug mäßige Resistenzniveaus zusammen mit zahlreichen Eigenschaften, die mit schweren Erkrankungen einhergehen. Der andere wurde von menschlich geprägten Untergruppen dominiert, die sich hinsichtlich Resistenz, Krankheitspotenzial und bevorzugten Wirten unterschieden. Einige Untergruppen waren klar menschenorientiert und stark resistent, andere zeigten gemischte Muster und traten in Menschen, Geflügel, Wildtieren, Wasser und Haustieren auf. Dieses Mosaik spiegelt die Fähigkeit von CC38 wider, sich an unterschiedliche Umgebungen und Wirtsarten anzupassen, was die Bekämpfung erschwert.
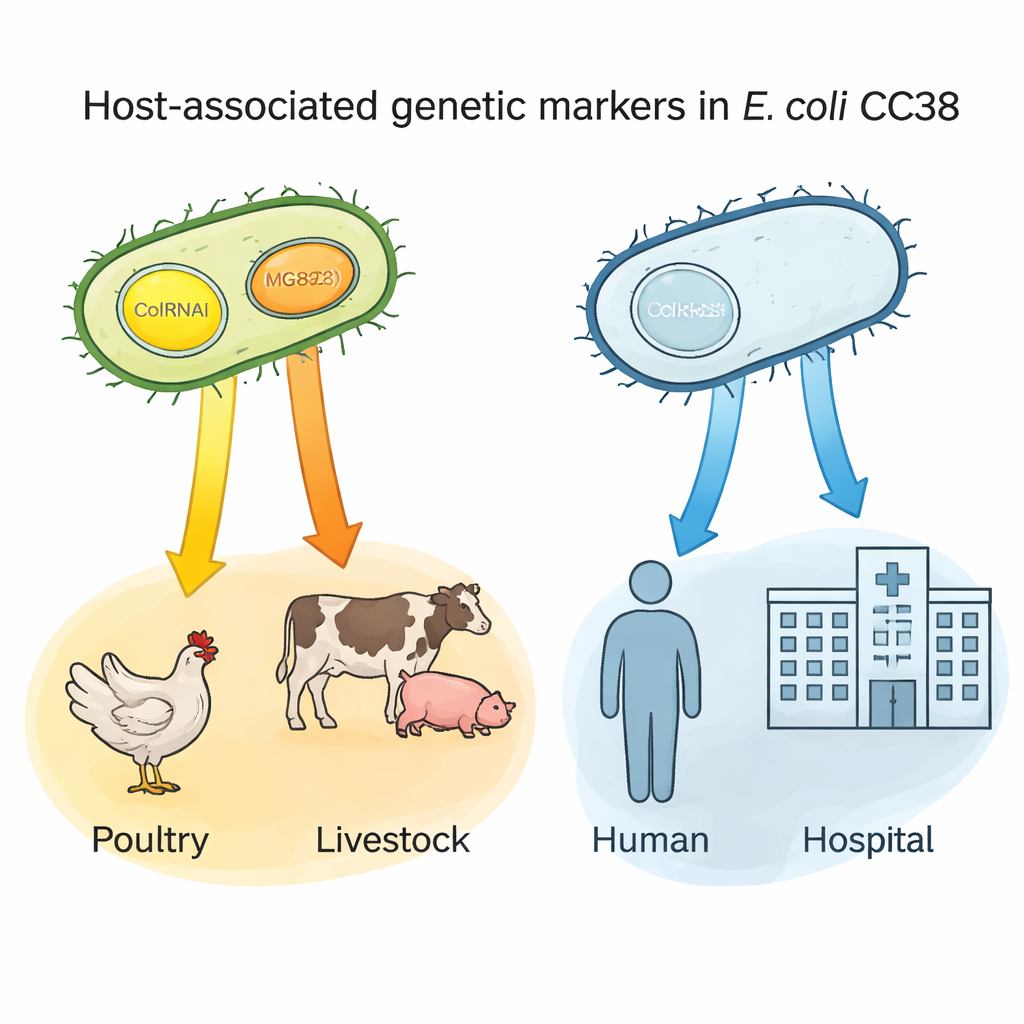
Kleine DNA‑Kreise als wirtsspezifische „Namensschilder"
Eine zentrale Entdeckung betraf zwei winzige DNA‑Stücke — Plasmide mit den Bezeichnungen ColRNAI und Col(MG828) —, die sich zwischen Bakterien bewegen können. Diese Plasmide waren in CC38‑Isolaten aus Geflügel und anderen Nutztieren häufig, in den menschenzentrierten Untergruppen jedoch selten. Mittels statistischer Analysen zeigten die Autorinnen und Autoren, dass das Tragen eines der beiden Plasmide stark für einen Geflügelursprung vorhersagte; das gemeinsame Vorkommen beider Plasmide war besonders charakteristisch für Linien, die mit Nutztieren und bestimmten Lebensmittelquellen verbunden sind. Da diese Plasmide oft auch Resistenzmerkmale tragen, können sie als genetische „Namensschilder“ dienen, die Bakterien kennzeichnen, die wahrscheinlich aus tierischen Reservoiren stammen, und so helfen nachzuvollziehen, wie resistente Stämme in die Nahrungskette und zu Menschen gelangen.
Was das für den Gesundheitsschutz bedeutet
Für Nichtfachleute ist die Kernaussage: Schädliche, medikamentenresistente E. coli sind nicht auf Krankenhäuser oder Patientinnen und Patienten beschränkt; sie bilden vernetzte Populationen, die Menschen, Geflügel, Nutztiere, Wildtiere, Lebensmittel und Umwelt übergreifen. Diese Studie zeigt, dass innerhalb einer wichtigen Linie, CC38, einige Zweige stark mit Tieren verbunden sind und andere mit Menschen, und dass spezifische mobile DNA‑Elemente Aufschluss über die wahrscheinliche Herkunft eines Stamms geben können. Die Nutzung dieser genetischen Marker in der routinemäßigen Überwachung könnte frühzeitig warnen, wenn tierassoziierte resistente Bakterien vermehrt bei Menschen auftauchen. Das unterstützt einen "One Health"-Ansatz — der menschliche, tierische und ökologische Gesundheit als ein zusammenhängendes System betrachtet — und ermöglicht gezieltere Strategien zur Verhinderung von Infektionen und zur Verlangsamung der Ausbreitung von Antibiotikaresistenzen.
Zitation: Roer, L., Rasmussen, A., Hansen, F. et al. Genomic characterization and sub-clustering of Escherichia coli clonal complex 38 reveal host associated genetic markers. Commun Med 6, 126 (2026). https://doi.org/10.1038/s43856-026-01402-2
Schlüsselwörter: antimikrobielle Resistenz, Escherichia coli, zoonotische Übertragung, Geflügel und Nutztiere, genomische Überwachung