Clear Sky Science · de
Vorhersage des Verlaufs aus räumlichem Proteinprofiling von triple-negativen Mammakarzinomen
Warum die Anordnung von Krebszellen zählt
Wenn Ärzte ein aggressives Mammakarzinom unter dem Mikroskop betrachten, sehen sie eine dichte Landschaft aus Tumorzellen, Immunzellen und Stützgewebe. Bis vor Kurzem konzentrierten sich die meisten Tests jedoch darauf, wie viel einer bestimmten Molekülart vorhanden ist, nicht darauf, wo sie sich befindet. Diese Studie zeigt, dass die physische Anordnung von Proteinen und Zellen in triple-negativen Brustkrebserkrankungen vorhersagen kann, wie Patientinnen und Patienten abschneiden, und führt eine neue Methode ein, um diese räumlichen Muster direkt aus hochauflösenden Bildern zu lesen.
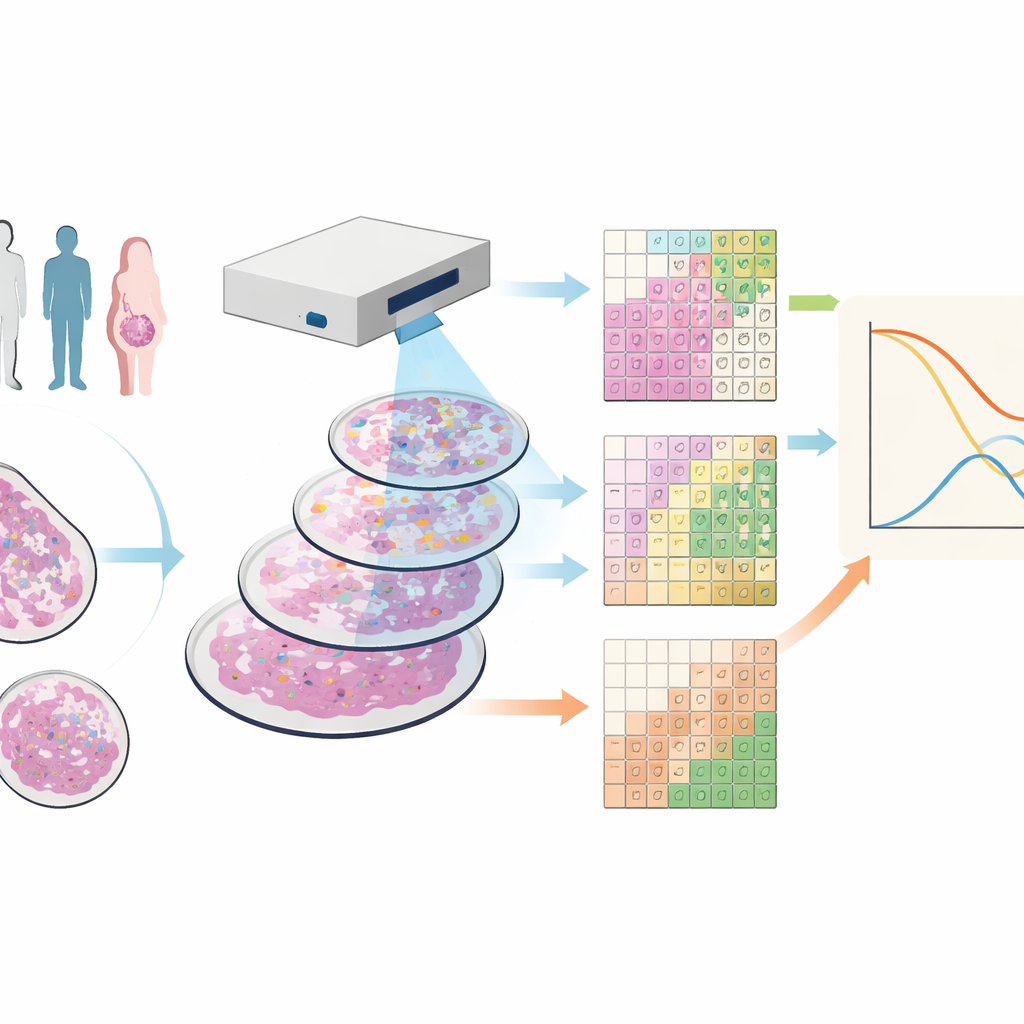
Krebsgewebe in vielen Farben sehen
Die Forschenden arbeiteten mit Gewebeproben von 88 Personen mit triple-negativem Brustkrebs, einer Form der Erkrankung, die gängige Wirkstoffziele nicht aufweist und oft eine ungünstige Prognose hat. Sie verwendeten eine Technik namens imaging mass cytometry, bei der jede Probe mit Dutzenden metallmarkierter Antikörper gefärbt wird. Unter einem spezialisierten Scanner entstehen dadurch Bilder, in denen jeder Punkt im Gewebe einen detaillierten Fingerabdruck vieler verschiedener Proteine trägt und gleichzeitig Tumorzellen, verschiedene Immunzellen, Blutgefäße und Strukturfasern sichtbar macht.
Das Bild in Kacheln statt in Zellen zerlegen
Die meisten aktuellen Werkzeuge versuchen, die Umrisse jeder einzelnen Zelle zu zeichnen und sie dann nach Typ zu klassifizieren — ein Vorgang, der fehleranfällig und langsam sein kann, insbesondere in dünnen Gewebsschnitten, in denen Zellen nur teilweise erfasst werden. Das Team entwickelte stattdessen SparTile, eine Methode, die das Zeichnen individueller Zellgrenzen überspringt. SparTile zerlegt jedes Bild in viele kleine überlappende Quadrate, sogenannte Kacheln, und verwendet mathematische Techniken, um wiederkehrende Muster von Proteinkombinationen innerhalb dieser Kacheln zu erlernen. Zuerst gruppiert es Kacheln in grobe Regionen — Tumor, Stroma (stützendes Gewebe) oder immunreiche Zonen — und teilt dann jede Region weiter in spezifischere „Mikroumgebungen“ auf, die jeweils ihre eigene Mischung aus Proteinen und benachbarten Zelltypen aufweisen.
Versteckte Nachbarschaften, die mit dem Verlauf verknüpft sind
Mit diesen kartierten Mikroumgebungen quantifizierten die Wissenschaftlerinnen und Wissenschaftler, wie häufig jedes Muster in den Proben der einzelnen Patientinnen und Patienten vorkam, und verglichen dies mit der Langzeitüberlebenszeit. Mehrere auffällige Zusammenhänge traten zutage. Eine tumorzentrierte Mikroumgebung, die reich an einem Protein namens MX1 und an Markern myeloider Immunzellen war, war mit einem deutlich höheren Sterberisiko verbunden. Ein weiteres Tumormuster, gekennzeichnet durch Vimentin — ein Hinweis darauf, dass Tumorzellen in einen beweglicheren, invasiveren Zustand übergegangen sind —, korrelierte ebenfalls stark mit schlechtem Überleben. Im Gegensatz dazu standen Bereiche, die von bestimmten T‑Zellen dominiert wurden, mit besseren Ergebnissen in Verbindung, während B-Zell-reiche Regionen schwächere Effekte zeigten, möglicherweise weil sie in den kleinen Gewebekernen, die analysiert wurden, selten waren.
Abstand zwischen Tumor- und Immunzellen als Warnsignal
Über das Vorhandensein bestimmter Nachbarschaften hinaus spielten auch ihre räumlichen Beziehungen eine Rolle. Das Team untersuchte, wie eng Tumorregionen und myeloide Immunregionen nebeneinander lagen, indem es ein statistisches Maß berechnete, wie stark sich ihre Protein‑Signale räumlich überlappten. Patientinnen und Patienten, deren Tumoren myeloidreiche Bereiche hatten, die dicht zwischen Tumorzellen eingebettet waren, tendierten zu schlechteren Verläufen als solche, bei denen die beiden Populationen weiter getrennt waren. Dieses „Abstands“-Maß blieb ein starker Risikoprädiktor, selbst nachdem standardmäßige klinische Faktoren berücksichtigt wurden, und seine Bedeutung bestätigte sich bei Tests an zwei unabhängigen Brustkrebs-Bilddatensätzen anderer Forschungsgruppen.
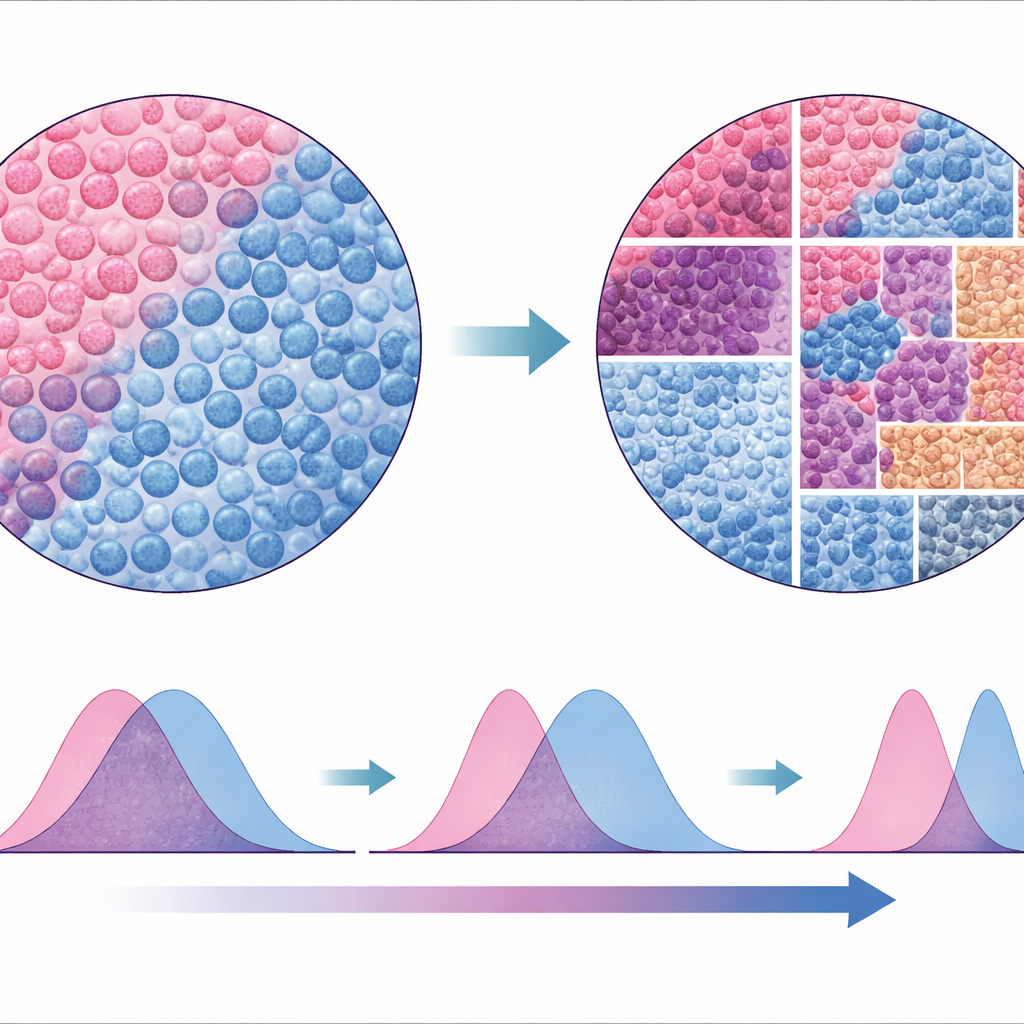
Eine neue Art, die Tumorlandschaft zu lesen
Um die Robustheit ihres Ansatzes zu prüfen, verglichen die Autorinnen und Autoren SparTile mit traditionellen Methoden, die auf Segmentierung und Klassifikation einzelner Zellen aufbauen und dann Nachbarschaften um diese Zellen herum bilden. Während die zellbasierten Analysen einige der gleichen Muster wiederfanden, waren sie über Datensätze hinweg weniger konsistent und weniger zuverlässig beim Erkennen bestimmter riskanter Mikroumgebungen, etwa jener mit MX1 und myeloiden Zellen. Da SparTile direkt auf den Rohproteinbildern arbeitet, umgeht es viele der Annahmen und technischen Fallstricke zell‑für‑zell‑Ansätze, kann aber später dennoch mit ihnen kombiniert werden, wenn detaillierte Zelltypen für die Planung von Experimenten oder Therapien benötigt werden.
Was das für Patientinnen und Patienten und die zukünftige Versorgung bedeutet
Diese Arbeit zeigt, dass nicht nur die Bestandteile, sondern auch die räumliche Anordnung eines Tumors wichtig ist, um vorherzusagen, wie sich eine Patientin oder ein Patient mit triple-negativem Brustkrebs entwickelt. Indem komplexe Multi‑Protein‑Bilder in interpretierbare räumliche Muster und einfache Abstandsmaße übersetzt werden, bietet SparTile eine Möglichkeit, Hochrisiko‑Patientinnen und -Patienten aus kleinen Gewebeproben zu identifizieren und biologische Anordnungen aufzudecken, die möglicherweise durch künftige Behandlungen adressiert werden können. Obwohl vor einer routinemäßigen klinischen Anwendung noch weitere Validierungen nötig sind, weist der Ansatz auf eine Zukunft hin, in der die „Karte“ eines Tumors genauso wichtig wird wie seine molekulare Teileliste.
Zitation: Foroughi pour, A., Wu, TC., Noorbakhsh, J. et al. Prediction of outcome from spatial Protein profiling of triple-negative breast cancers. Commun Med 6, 133 (2026). https://doi.org/10.1038/s43856-026-01400-4
Schlüsselwörter: triple-negativer Brustkrebs, Tumormikroumgebung, räumliche Proteomik, imaging mass cytometry, prognostische Biomarker