Clear Sky Science · de
Defizienz der homologen Rekombination bei primärem ER-positivem und HER2-negativem Brustkrebs
Warum das für Brustkrebspatientinnen und -patienten wichtig ist
Die meisten Brustkrebserkrankungen gehören zu einer großen Gruppe, die als Östrogenrezeptor-positiv und HER2-negativ klassifiziert wird. Diese Tumoren werden in der Regel mit hormonsperrenden Medikamenten behandelt, teils in Kombination mit Chemotherapie. Dennoch treten bei vielen Patientinnen und Patienten Rückfälle auf, und Ärztinnen und Ärzte verfügen nicht über präzise Werkzeuge, um zu entscheiden, wer wirklich eine intensive Behandlung benötigt oder von neuen zielgerichteten Medikamenten profitieren könnte. Diese Studie untersucht eine spezifische Schwachstelle mancher Tumoren – die Defizienz der homologen Rekombination (HRD) – bei der Krebszellen schlecht darin sind, gebrochene DNA zu reparieren, was möglicherweise personalisierte Behandlungsoptionen eröffnet.
Eine verborgene Schwäche nur in manchen Tumoren
Die homologe Rekombination ist eines der wichtigsten zellulären Systeme zur Reparatur gefährlicher DNA-Brüche. Versagt dieses System – oft durch Defekte in bekannten Genen wie BRCA1, BRCA2, PALB2 oder RAD51C – sammeln Zellen Mutationen an und können besonders sensitiv gegenüber bestimmten Medikamenten werden, darunter Platin-basierte Chemotherapien und PARP-Inhibitoren. HRD ist bei einer aggressiveren Form von Brustkrebs, dem triple-negativen Tumor, häufig, doch ihre Bedeutung in der häufiger vorkommenden ER-positiven, HER2-negativen Gruppe war unklar. Zur Klärung analysierten Forschende 502 solcher Tumoren aus der schwedischen SCAN-B-Studie mittels Ganzgenomsequenzierung sowie zugehöriger Daten zu Genaktivität, DNA-Methylierung, erhaltenen Therapien und Langzeitverläufen.
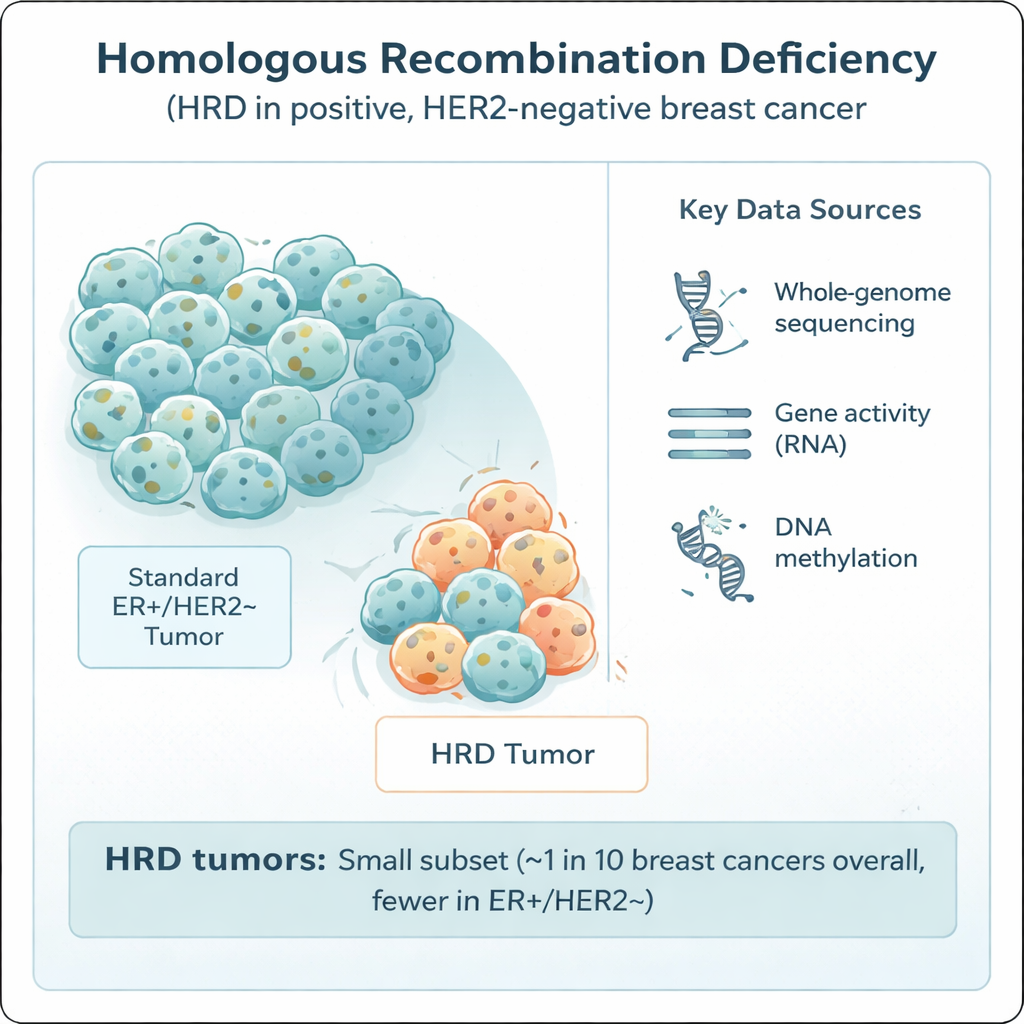
Wie die Studie durchgeführt wurde
Alle Tumoren wurden zum Zeitpunkt der Operation gesammelt, vor jeglicher medikamentöser Behandlung, wodurch ein klares Bild ihrer ursprünglichen Biologie entstand. Das Team nutzte ein ausgefeiltes Mustererkennungswerkzeug, HRDetect, um die „mutationalen Signaturen“ zu lesen, die in der Krebs-DNA zurückbleiben, wenn die homologe Rekombination gestört ist. Tumoren wurden als HRD klassifiziert, wenn sie eine strenge Wahrscheinlichkeitsgrenze überschritten. Die Wissenschaftlerinnen und Wissenschaftler verglichen außerdem verschiedene Methoden zur Detektion von HRD – von anderen DNA-basierten Scores bis hin zu einem RNA-basierten Genexpressions-Test –, um zu prüfen, wie zuverlässig die Verfahren übereinstimmen. Zusätzlich untersuchten sie weiter gefasste Merkmale wie die Gesamtmutationslast, Muster von chromosomalen Gewinnen und Verlusten, immunbezogene Genaktivität sowie chemische Markierungen der DNA (Methylierung), die Gene an- oder ausschalten können.
Wie häufig ist HRD und was verursacht sie?
Die Forschenden stellten fest, dass nur 8,4 % der ER-positiven, HER2-negativen Tumoren in ihrer sequenzierten Kohorte klare Hinweise auf HRD zeigten – deutlich weniger als die etwa 60 %, die in triple-negativen Fällen beobachtet werden. Durch die Kombination dieser Daten mit nationalen Registern und anderen Studien schätzten sie, dass ungefähr 1 von 20 Tumoren in dieser klinischen Untergruppe und etwa 1 von 9 Brustkrebserkrankungen insgesamt in westeuropäischen/nordischen Populationen HRD aufweist. In den HRD-Tumoren konnten sie oft eine wahrscheinliche Ursache identifizieren: Etwa 70 % wiesen eindeutige Schäden in BRCA1, BRCA2, RAD51C oder PALB2 auf, verursacht durch vererbbare Mutationen, tumorspezifische Mutationen oder Deletionen oder durch epigenetische Stilllegung von Promotoren. Auffällig war, dass rund ein Drittel der HRD-Fälle durch Promoter-Hypermethylierung bedingt war – eine chemische Beschichtung, die DNA-Reparaturgene ausschaltet, ohne die Sequenz zu verändern. Etwa 30 % der HRD-Tumoren zeigten hingegen keinen offensichtlichen einzelnen Auslöser, was auf zusätzliche, noch zu entdeckende Wege zu diesem Reparaturversagen hindeutet.
Wie HRD-Tumoren mikroskopisch und klinisch erscheinen
HRD-Tumoren in dieser verbreiteten Gruppe zeigten eher Kennzeichen eines aggressiveren Krankheitsverlaufs: Sie hatten häufig höhere Zellteilungsraten, niedrigere Hormonrezeptor-Färbung und komplexere, mutationsreichere Genome als HR-fähige Tumoren. Sie traten in nahezu allen wichtigen molekularen Subtypen auf, waren jedoch selten in der eher indolenten Luminal-A-Klasse und relativ gehäuft in einer kleineren basal-ähnlichen Untergruppe. Betrachtet man jedoch die globale Genaktivität und DNA-Methylierungsmuster, ließen sich HRD-Tumoren nicht in ein einzelnes, leicht erkennbares Profil einordnen. Ihre Expressionsmuster waren vielfältig, und Unterschiede innerhalb spezifischer Subtypen waren eher mäßig. Einige HRD-Tumoren, insbesondere in den Luminal-B- und basal-ähnlichen Gruppen, zeigten stärkere Hinweise auf Immunaktivität und eine erhöhte Expression von PD-L1, was darauf hindeutet, dass sie für das Immunsystem sichtbarer sein und potenziell besser auf Immuntherapien ansprechen könnten.
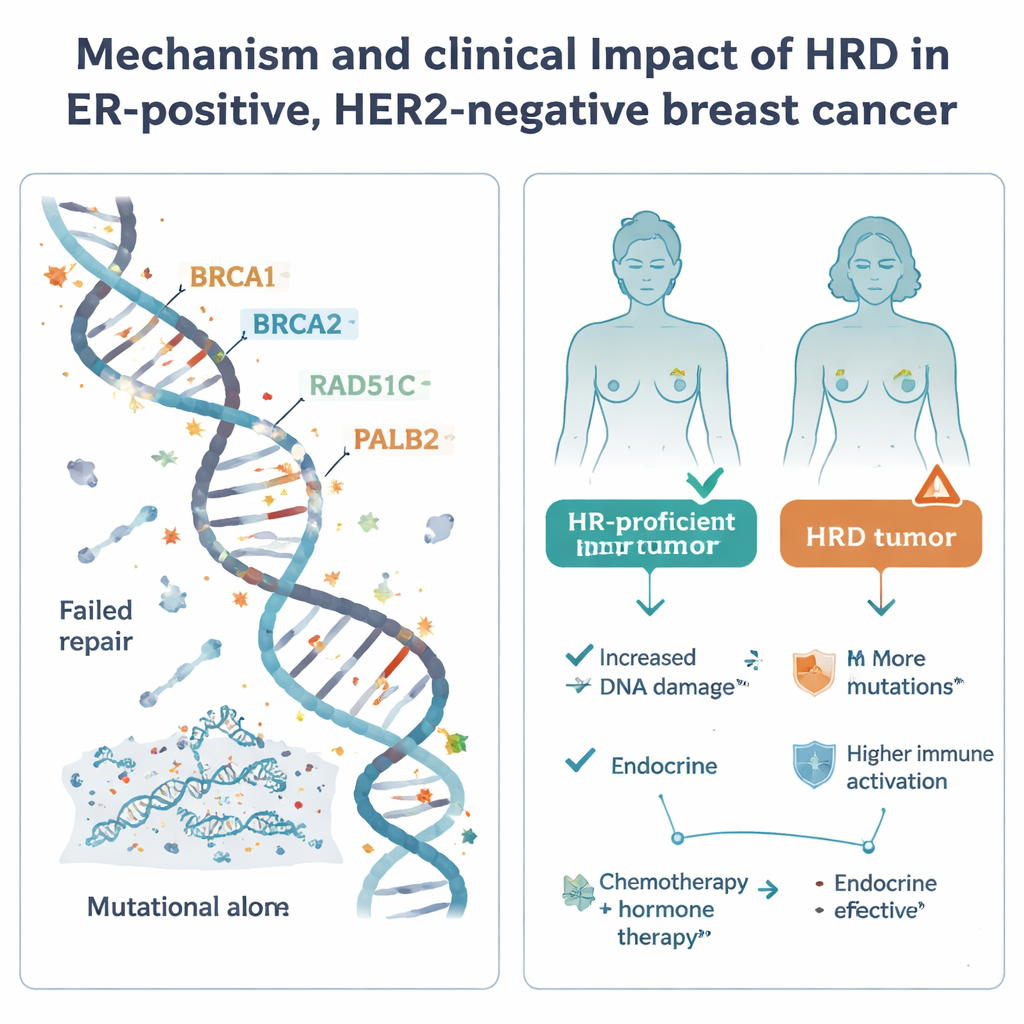
Beeinflusst HRD das Patienten-Outcome?
Die Studie untersuchte anschließend, wie der HRD-Status mit realen Behandlungsergebnissen unter Standardversorgung zusammenhängt. Bei Patientinnen und Patienten, die nach der Operation ausschließlich eine Hormontherapie erhielten, zeigten HRD-Tumoren einen Trend zu schlechterer fernmetastasenfreier Überlebenszeit, wobei die Zahl der HRD-Fälle klein war und das Ergebnis keine formale statistische Signifikanz erreichte. Dieses Muster zusammen mit den aggressiven molekularen Merkmalen legt nahe, dass die ausschließliche Behandlung mit endokriner Therapie für Patientinnen und Patienten mit HRD-Tumoren riskant sein könnte. Im Gegensatz dazu war bei Patientinnen und Patienten, die sowohl Chemotherapie als auch Hormontherapie erhielten, kein klarer Zusammenhang zwischen HRD-Status und besseren oder schlechteren Ergebnissen erkennbar; die Rückfallraten waren in allen Gruppen weitgehend ähnlich, und die Chemotherapie könnte einen Teil des erhöhten Risikos bei HRD-Tumoren abmildern.
Was das für künftige Therapieentscheidungen bedeutet
Für eine interessierte Leserschaft ist die Kernbotschaft: Nur eine Minderheit der ER-positiven, HER2-negativen Brustkrebse trägt diese spezifische DNA-Reparaturschwäche, doch wenn sie vorhanden ist, kennzeichnet sie tendenziell aggressivere Tumoren, die sich allein mit Hormontherapie möglicherweise nicht gut kontrollieren lassen. Die Arbeit stützt die Auffassung, dass Ganzgenomsequenzierung HRD zuverlässig nachweisen und ihre Ursachen klären kann, jenseits des bloßen Testens auf vererbte BRCA1- oder BRCA2-Mutationen. Obwohl die Studie noch nicht beweist, dass eine Therapieanpassung basierend auf HRD das Überleben verbessert, liefert sie frühe Hinweise darauf, dass Patientinnen und Patienten mit HRD-Tumoren von Chemotherapie und in künftigen Studien möglicherweise von PARP-Inhibitoren oder Immuntherapien profitieren könnten. Kurz gesagt: HRD-Tests könnten ein Baustein in einem verfeinerten Instrumentarium werden, um Therapiedosis und neue zielgerichtete Optionen an die Biologie jedes einzelnen Brustkrebses anzupassen.
Zitation: Davies, H.R., Black, D., Kvist, A. et al. Homologous recombination deficiency in primary ER-positive and HER2-negative breast cancer. Commun Med 6, 118 (2026). https://doi.org/10.1038/s43856-026-01385-0
Schlüsselwörter: Brustkrebs, DNA-Reparatur, BRCA-Gene, Genomsequenzierung, zielgerichtete Therapie