Clear Sky Science · de
Oberflächenmodifizierte, doppelt beladene, tumorgezielte liposomale Nanopartikel zur Überwindung der Therapieresistenz beim Glioblastoma multiforme
Warum diese Forschung zu Hirntumoren wichtig ist
Das Glioblastom ist eine der tödlichsten Formen von Hirntumoren. Selbst mit Operation, Bestrahlung und Chemotherapie überleben die meisten Patienten nach der Diagnose kaum mehr als ein Jahr. Ein zentrales Problem ist, dass Standardmedikamente oft den Tumor im Gehirn nicht erreichen können, und selbst wenn sie es tun, passt sich der Tumor schnell an und entwickelt Resistenzen. Diese Studie untersucht einen neuen Ansatz, mehrere Wirkstoffe an den natürlichen Schutzbarrieren des Gehirns vorbei in den Tumor zu schleusen und dort zu konzentrieren, mit dem Ziel, bestehende Therapien wie die Strahlentherapie deutlich wirksamer zu machen.
Ein winziger Lieferwagen für Krebsmedikamente
Die Forschenden entwickelten ultrakleine Wirkstoffträger, so genannte tumorgezielte Liposomen. Dabei handelt es sich um weiche, fettbasierte Bläschen im Nanometerbereich, die Arzneistoffe im Inneren aufnehmen können. Das Team modifizierte die Oberfläche dieser Bläschen mit einem speziellen Peptid, das Glioblastomzellen erkennt und an ihnen haftet, wodurch die Partikel Tumoren anstelle von gesundem Gewebe gezielt ansteuern. Jedes Bläschen wurde so gestaltet, dass es gleichzeitig zwei Krebsmedikamente transportieren kann: entweder Everolimus zusammen mit Vinorelbin oder Rapamycin zusammen mit Vinorelbin. Die Idee ist, dass die beiden Wirkstoffe die Tumorzellen auf komplementäre Weise angreifen, während die schützende Hülle die Medikamente im Blutstrom stabilisiert und ihr Eindringen ins Gehirn erleichtert.
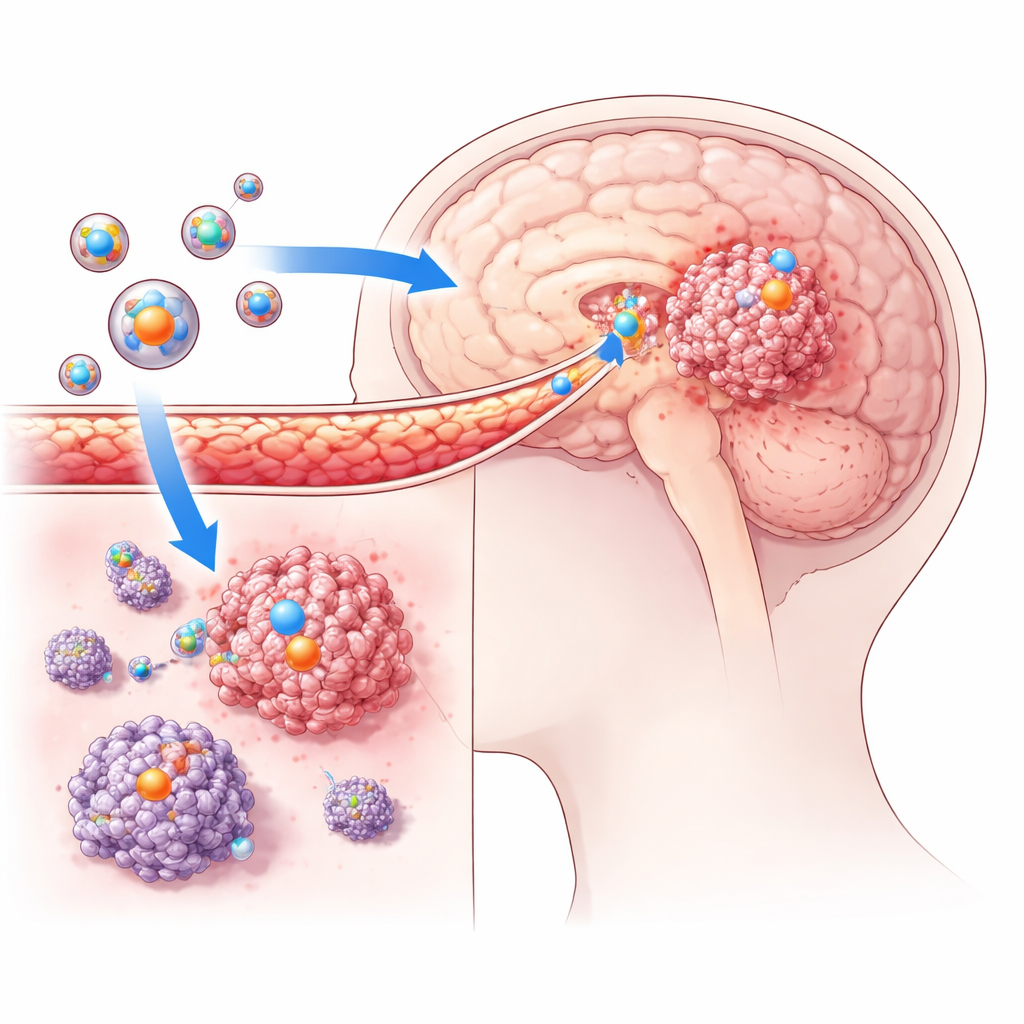
Die Schutzmauer des Gehirns überwinden
Mithilfe von Mausmodellen, die mit menschlichen Glioblastomzellen beimpft waren, prüfte das Team, ob diese Liposomen tatsächlich Tumoren im Gehirn erreichen können. Sie markierten die Partikel mit fluoreszierenden Farbstoffen und verfolgten ihren Weg mit fortschrittlichen bildgebenden Verfahren. Im Vergleich zu nicht gezielten Liposomen zeigten die tumorgezielten Varianten deutlich stärkere Signale im Hirntumor und nur geringe Signale in normalen Hirnregionen. Das bestätigte, dass die konstruierten Partikel die Blut‑Hirn-Schranke überwinden und sich gezielt dort anreichern konnten, wo die Krebszellen wuchsen. In Zellkulturversuchen nahmen Glioblastomzellen auch deutlich mehr der gezielten Liposomen auf als die Kontrollpartikel, was die Annahme stützt, dass das Oberflächenpeptid die Tumoranziehung und das Eindringen stark verbessert.
Den Tumor stärker treffen und dabei den Rest des Körpers schonen
Die Wissenschaftler verglichen zunächst, wie gut Ein-Wirkstoff- und Zwei-Wirkstoff-Liposomen Krebszellen in Zellkulturen abtöteten. Die Zwei-Wirkstoff-Varianten, insbesondere die Kombination Everolimus–Vinorelbin, waren wirksamer als jeder Wirkstoff allein und wirkten besser als dieselben Medikamente ohne liposomalen Träger. In Kombination mit Bestrahlung verstärkte sich der Effekt noch: Krebszellen bildeten deutlich weniger Kolonien, bewegten sich weniger und zeigten vermehrt Anzeichen von Schäden. In Maus-Hirntumoren wuchsen Tumoren bei Tieren, die mit Zwei‑Wirkstoff‑Liposomen plus Bestrahlung behandelt wurden, langsamer und die Tiere lebten länger als solche, die nur Bestrahlung, nur Liposomen oder die Standardchemotherapie mit Temozolomid erhielten. Wichtig ist, dass die Forschenden keine offensichtlichen Schädigungen anderer Organe beobachteten, was darauf hindeutet, dass die gezielte Konzentration der Behandlung im Tumor Nebenwirkungen verringern kann.
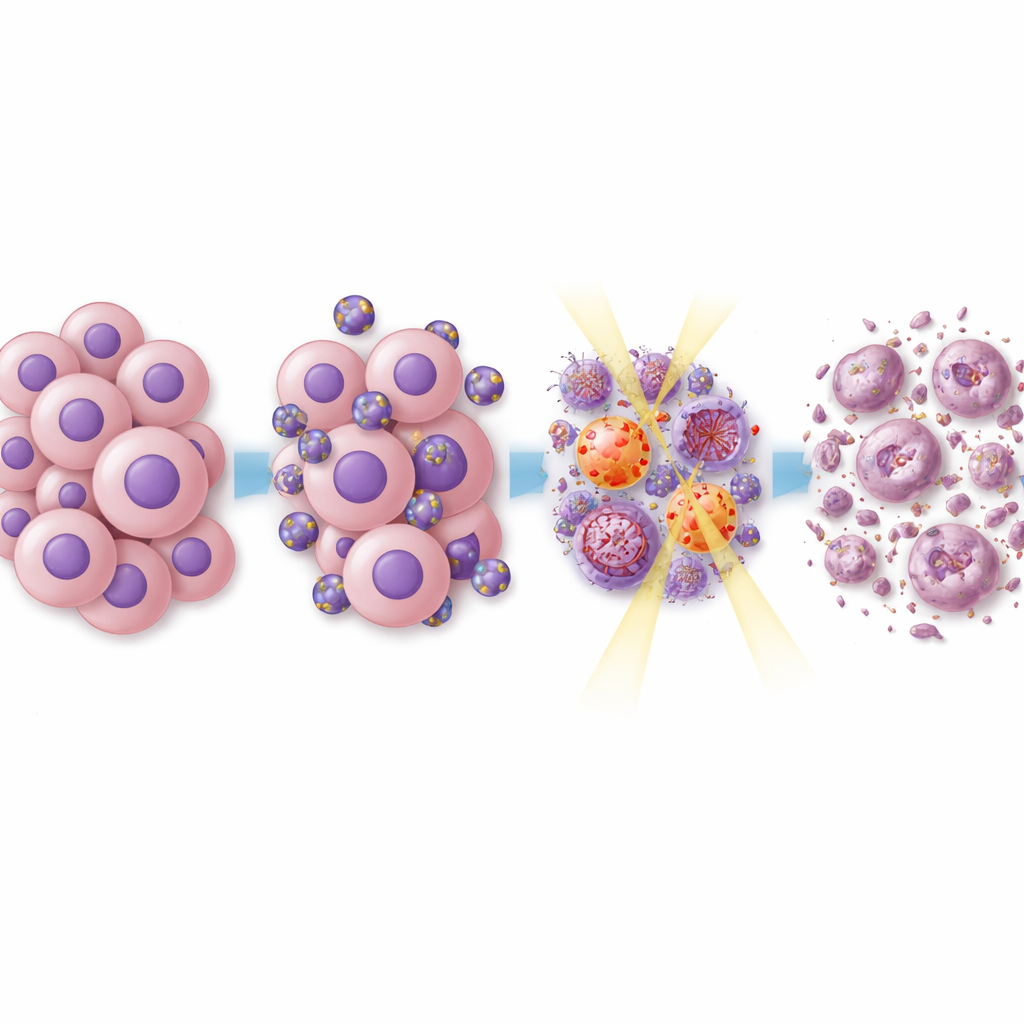
Was sich in den Krebszellen abspielt
Um zu verstehen, warum dieser Ansatz Tumore empfindlicher gegenüber Therapien machte, untersuchte das Team zentrale Signalwege in den Krebszellen. Everolimus und Rapamycin blockieren bekanntermaßen einen als mTOR bezeichneten Weg, der Zellen beim Wachstum und bei der Stressresistenz unterstützt. Die Zwei‑Wirkstoff‑Liposomen unterdrückten mTOR‑bezogene Signale sowie andere Wachstumswege, die die Teilung und Bewegung von Glioblastomzellen antreiben. Wurde zusätzlich bestrahlt, waren auch Proteine, die an der DNA‑Schadensreparatur beteiligt sind, gedämpft. Das bedeutet, dass die Tumorzellen weniger in der Lage waren, die durch Strahlung verursachten genetischen Schäden zu reparieren, wodurch sie eher in Richtung Zelltod statt Erholung gedrängt wurden. Detaillierte Analysen der Genaktivität in behandelten Tumoren zeigten weitreichende Veränderungen in Netzwerken, die mit Zellzykluskontrolle, DNA‑Reparatur und der Interaktion des Tumors mit dem Immunsystem verknüpft sind; viele Gene, die mit Therapieresistenz assoziiert sind, wurden herunterreguliert.
Was das für zukünftige Patientinnen und Patienten bedeuten könnte
Diese Arbeit zeigt, dass sorgfältig entwickelte, tumoranziehende Nanopartikel zwei kooperierende Wirkstoffe über die Schutzbarriere des Gehirns transportieren, sie im Glioblastom konzentrieren und die Wirkung der Strahlentherapie verbessern können. Bei Mäusen verlangsamte diese Strategie das Tumorwachstum und verlängerte das Überleben, ohne offensichtliche zusätzliche Toxizität. Obwohl diese Ergebnisse noch präklinisch sind und vor einer Anwendung am Menschen deutlich mehr Tests erforderlich sind, weist die Studie auf einen praktikablen Weg hin, gezielte Wirkstoffabgabe mit bestehenden Therapien zu kombinieren, um einen hochresistenten Krebs zu überlisten. Sollten sich vergleichbare Vorteile beim Menschen zeigen, könnten solche doppelt beladenen Liposomen eines Tages Glioblastompatientinnen und -patienten zu längeren und lebenswerteren Zeiten verhelfen.
Zitation: Angom, R.S., Rachamala, H.K., Nakka, N.M.R. et al. Surface-engineered dual drug-loaded tumor-targeted liposomal nanoparticles to overcome the therapeutic resistance in glioblastoma multiforme. Commun Med 6, 152 (2026). https://doi.org/10.1038/s43856-025-01279-7
Schlüsselwörter: Glioblastom, Nanopartikel, Liposomen, Behandlung von Hirntumoren, Strahlungssensibilisierung