Clear Sky Science · de
Untertypen der Alzheimer- und Parkinson-Krankheit mithilfe longitudinaler elektronischer Patientenakten
Warum das für Familien und Patienten wichtig ist
Über Alzheimer und Parkinson wird häufig gesprochen, als seien es jeweils einzelne, einheitliche Erkrankungen. Doch wer einen geliebten Menschen hat dahinschwinden sehen, weiß: Kein Krankheitsverlauf gleicht dem anderen. Diese Studie stellt eine einfache, aber wichtige Frage: Können die medizinischen Aufzeichnungen, die wir über Jahre hinweg sammeln, verborgene „Ausprägungen" dieser Hirnerkrankungen offenlegen, die schließlich eine gezieltere Versorgung ermöglichen könnten? Anhand moderner Mustererkennungswerkzeuge und der Krankengeschichten von über 100.000 Menschen im Vereinigten Königreich zeigen die Autorinnen und Autoren, dass sich Alzheimer und Parkinson jeweils in fünf unterschiedliche Subtypen aufspalten lassen, mit verschiedenen Risiken, Symptomen und wahrscheinlichen Verläufen.
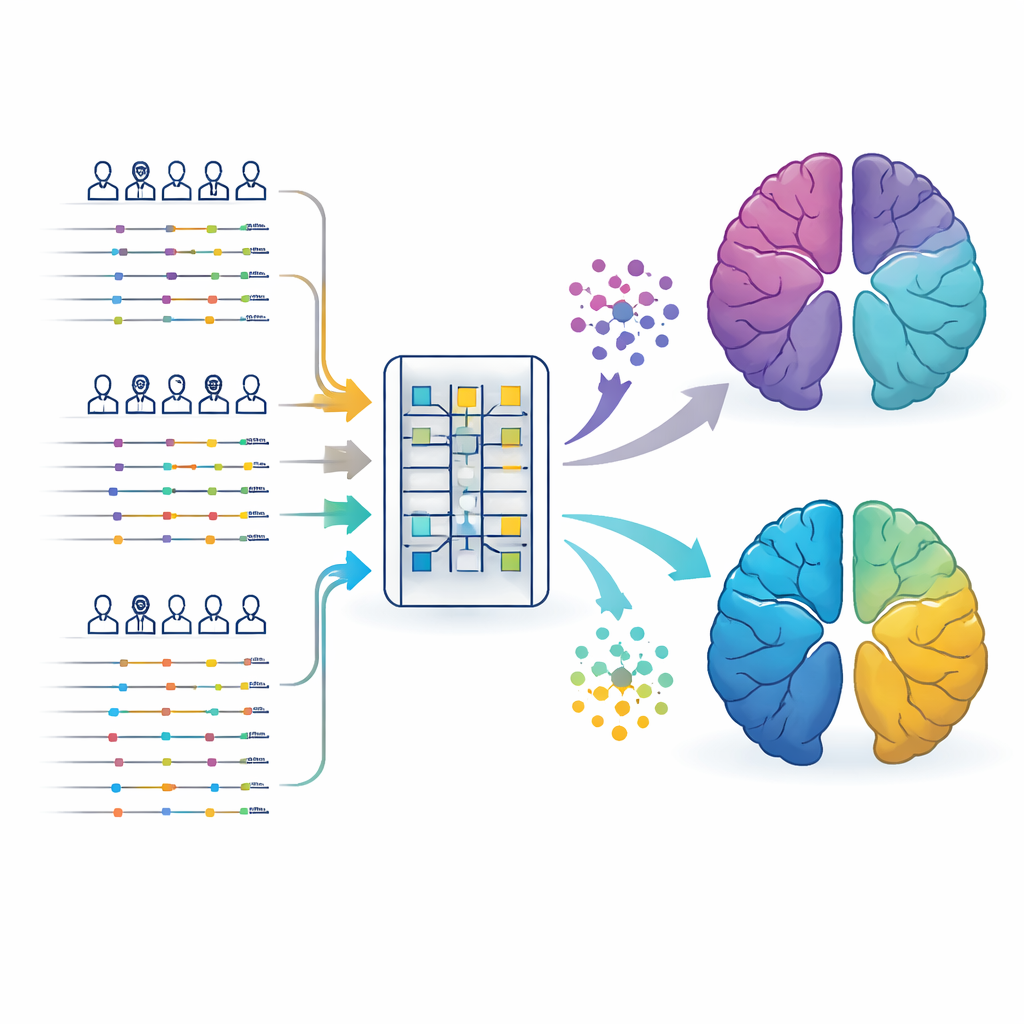
Menschen über Jahrzehnte hinweg in ihrer Gesundheitsgeschichte folgen
Die Forschenden nutzten anonymisierte elektronische Patientenakten aus zwei großen britischen Datensätzen: dem Clinical Practice Research Datalink, das Informationen aus der hausärztlichen Versorgung enthält, und dem UK Biobank, einem Langzeitforschungsprojekt, das Klinikbesuche, Krankenhausaufenthalte, Verschreibungen und genetische Daten verknüpft. Im Fokus standen mehr als 113.000 Menschen mit Alzheimer und über 45.000 mit Parkinson, jeweils mit rund zwei bis drei Jahrzehnten medizinischer Vorgeschichte vor der Diagnose. Anstatt nur Testergebnisse nach der Erkennung der Hirnerkrankung zu betrachten, fütterte das Team diese langen, zeitgestempelten Gesundheits"geschichten" in einen Transformer — eine Form künstlicher Intelligenz, die gut darin ist, Sequenzen wie Sprache oder hier eine zeitliche Abfolge von Arztkontakten zu verstehen.
Die Daten Patienten in verborgene Gruppen sortieren lassen
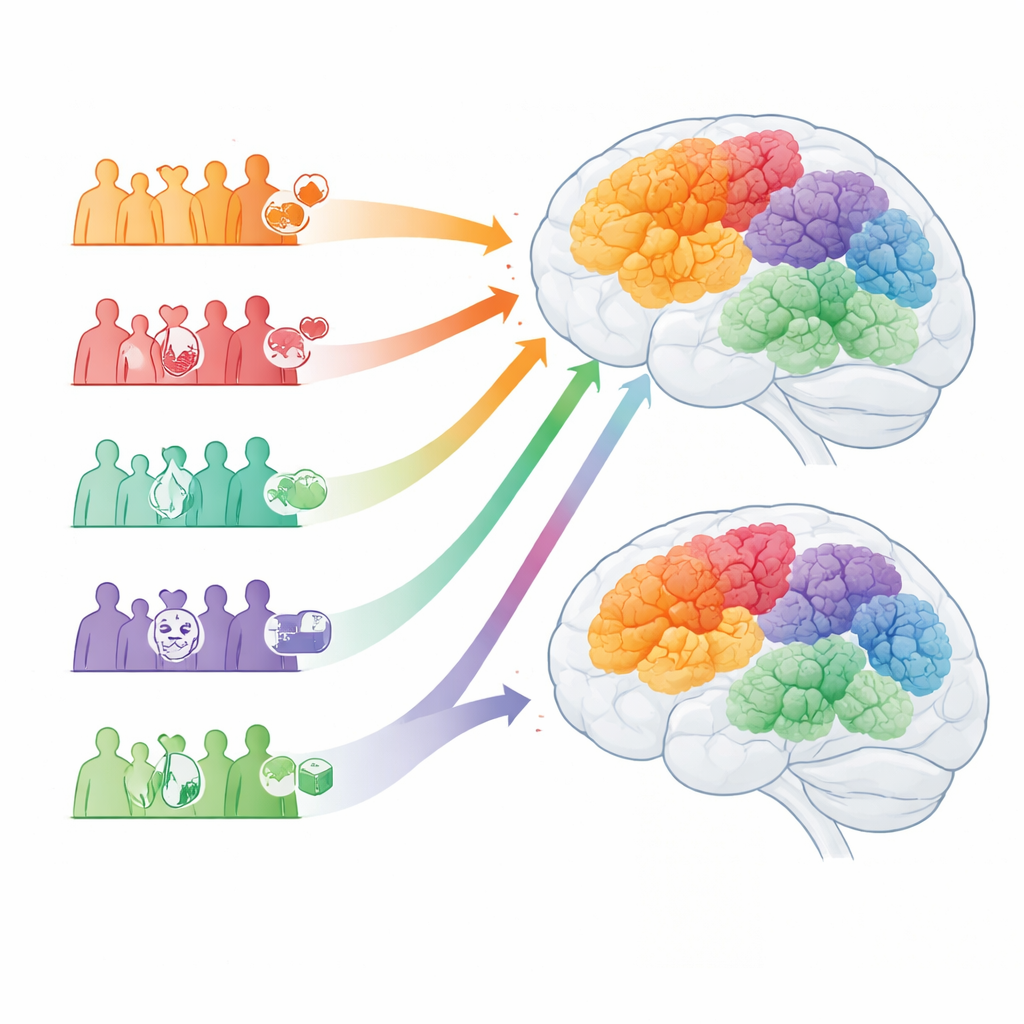
Aus jedem Datensatz erzeugte das Modell einen kompakten numerischen „Fingerabdruck“, der Muster von Erkrankungen, Verschreibungen und deren zeitlichem Ablauf einfing. Ein Clustering-Verfahren ordnete diese Fingerabdrücke dann in Gruppen, ohne dass ein vorgegebener Suchauftrag existierte. Für Alzheimer wie für Parkinson ergab sich jeweils die stabilste und reproduzierbarste Lösung mit fünf Subtypen. In jeder Erkrankung gab es eine Gruppe, die einem klassischen, weitgehend „reinen" Hirnleiden entsprach: Diese Personen hatten höhere genetische Risikowerte, relativ wenige andere medizinische Probleme und entwickelten sich nach der Diagnose besser. Andere Gruppen wurden von Mustern geprägt, die Jahre zuvor erkennbar waren, etwa ausgeprägter Gefäßkrankheit, metabolischen Problemen wie Diabetes und Adipositas oder einer langen Vorgeschichte von Angst und Depression.
Unterschiedliche Wege, unterschiedliche Ergebnisse
Die fünf Alzheimer-Subtypen reichten von einer häufigen spätbeginnenden Form mit weniger Begleiterkrankungen bis zu einem vaskulär dominierten Muster mit weit verbreitetem Bluthochdruck, sowie zu einer „psychischen Gesundheits"-Form, die durch ausgeprägte Depressionen, Ängste und schnellerem kognitiven Abbau gekennzeichnet war. Ein weiterer Subtyp stand in engem Zusammenhang mit Diabetes, Nierenerkrankungen und Hinweisen auf chronische Entzündung, obwohl er geringeres vererbtes Risiko zeigte; diese Patientinnen und Patienten erkrankten tendenziell früher und hatten eine kürzere Überlebenszeit. Eine letzte Alzheimer-Gruppe zeigte mehr Herzkrankheiten und Bewegungsprobleme und wies die höchsten Raten von Krankenhausaufenthalten und Sterblichkeit auf. Die Parkinson-Subtypen spiegelten diese Themen: eine Gruppe mit relativ „sauberer" Krankengeschichte und höherem genetischen Risiko, eine von Bluthochdruck und Gefäßkrankheit dominierte, eine mit schweren Stimmungsschwankungen und Bewegungsstörungen, eine mit ausgeprägten metabolischen und entzündlichen Merkmalen sowie eine, die schwere Herz- und Bewegungsprobleme kombinierte und besonders schlechte Überlebensraten hatte.
Gene und gemeinsame Risikofaktoren über Hirnerkrankungen hinweg
Da die UK Biobank DNA-Daten enthält, konnten die Autorinnen und Autoren prüfen, ob sich diese klinisch definierten Subtypen auch biologisch unterscheiden. In beiden Krankheitsbildern wiesen alle Patientengruppen höhere krankheitsbezogene genetische Risiko-Scores auf als Menschen ohne Diagnose — wie zu erwarten. Dennoch zeigten einige Cluster besonders starke oder schwache genetische Signale. Beispielsweise hatte ein „metabolisch‑entzündlicher" Alzheimer-Subtyp niedrigere Werte für klassische Alzheimer-Risikogene und war relativ angereichert mit einer schützenden Variante des APOE-Gens. Das deutet darauf hin, dass lebenslange Erkrankungen wie Diabetes und Adipositas ein demenzähnliches Bild hervorrufen können, selbst wenn das vererbte Risiko gering ist. Bei Alzheimer und Parkinson tauchten Subtypen, die von Bluthochdruck, Schlaganfallrisiko oder Stimmungserkrankungen geprägt sind, auf ähnliche Weise wieder auf — ein Hinweis darauf, dass Gefäßgesundheit, Stoffwechsel und psychische Gesundheit das Gehirn eher in unterschiedliche Degenerationsmuster lenken können, statt nur Begleiterscheinungen des Alterns zu sein.
Was das für die künftige Versorgung bedeuten könnte
Diese Arbeit verändert noch nicht die Art und Weise, wie Ärztinnen und Ärzte Patienten am Krankenbett diagnostizieren, und die Autorinnen und Autoren betonen, dass medizinische Aufzeichnungen allein nicht die genauen biologischen Ursachen jedes Subtyps beweisen können. Indem sie jedoch zeigen, dass routinemäßige Langzeitdaten sich natürlicherweise in konsistente, sinnvolle Gruppen einordnen, die Unterschiede in Symptomen, Überleben und Genetik widerspiegeln, liefert die Studie eine Blaupause für präzisere, frühere Risikoprofile. Künftig könnten Menschen mit bestimmten Kombinationen aus Gefäßkrankheit, Diabetes oder psychischen Problemen gezielter überwacht werden, um spezifische Muster von Alzheimer oder Parkinson früher zu erkennen, und klinische Studien ließen sich auf jene Subtypen ausrichten, die am ehesten profitieren. Kurz gesagt unterstützen die Ergebnisse einen Wandel weg von der Behandlung dieser Erkrankungen als monolithische Einheiten hin zu einer Sicht als Familien verwandter, aber unterschiedlicher Verläufe — und eröffnen damit Möglichkeiten für individuellere Prävention und Therapie.
Zitation: Lian, J., Fan, Z., Petrazzini, B.O. et al. Subtyping Alzheimer’s disease and Parkinson’s disease using longitudinal electronic health records. Nat Aging 6, 612–625 (2026). https://doi.org/10.1038/s43587-026-01085-3
Schlüsselwörter: Alzheimer-Krankheit Untertypen, Parkinson-Krankheit Untertypen, elektronische Patientenakten, Maschinelles Lernen in der Neurologie, Risikofaktoren für Neurodegeneration