Clear Sky Science · de
Strukturelles Signaturmuster von Plasmaproteinen klassifiziert den Status der Alzheimer-Krankheit
Warum ein Bluttest für Gedächtnisverlust wichtig ist
Die Alzheimer-Krankheit ist oft bereits weit fortgeschritten, bevor Gedächtnisprobleme deutlich werden. Die heute verfügbaren Tests, um sie früh zu erkennen, können jedoch invasiv, teuer oder schwer zugänglich sein. Diese Studie untersucht einen anderen Ansatz: Ob winzige Veränderungen in den dreidimensionalen Formen von Proteinen im Blut Auskunft darüber geben können, wo sich eine Person auf dem Kontinuum von gesundem Altern über leichte Vergesslichkeit bis hin zur manifesten Alzheimer-Erkrankung befindet. Gelingt das, könnte ein solcher Bluttest das Screening vereinfachen, frühere Behandlungen ermöglichen und Forschern helfen nachzuverfolgen, wer von neuen Therapien profitiert.
Auf die Proteinstruktur schauen, nicht nur auf die Menge
Die meisten Bluttests messen, wie viel eines bestimmten Moleküls vorhanden ist. Die Forscher konzentrierten sich stattdessen auf die Proteinstruktur. Innerhalb unserer Zellen sorgt ein Qualitätskontrollsystem dafür, dass Proteine korrekt gefaltet bleiben; versagt dieses System mit dem Alter, können fehlgefaltete Proteine sich ansammeln und Nervenzellen schädigen. Das Team fragte sich, ob dieser Zusammenbruch der „Proteinhaushaltsführung“ einen strukturellen Fingerabdruck in Blutproteinen hinterlässt. Von 520 Freiwilligen, die entweder kognitiv gesund, leicht kognitiv beeinträchtigt (MCI) oder an Alzheimer erkrankt waren, wurde Blut entnommen und eine chemische Methode namens kovalente Proteinprofilierung verwendet, um exponierte Proteinstellen zu markieren. Je stärker eine Stelle exponiert ist, desto leichter wird sie markiert, was eine numerische Messung der Proteinstruktur liefert, die weitgehend unabhängig von der Proteinkonzentration ist.
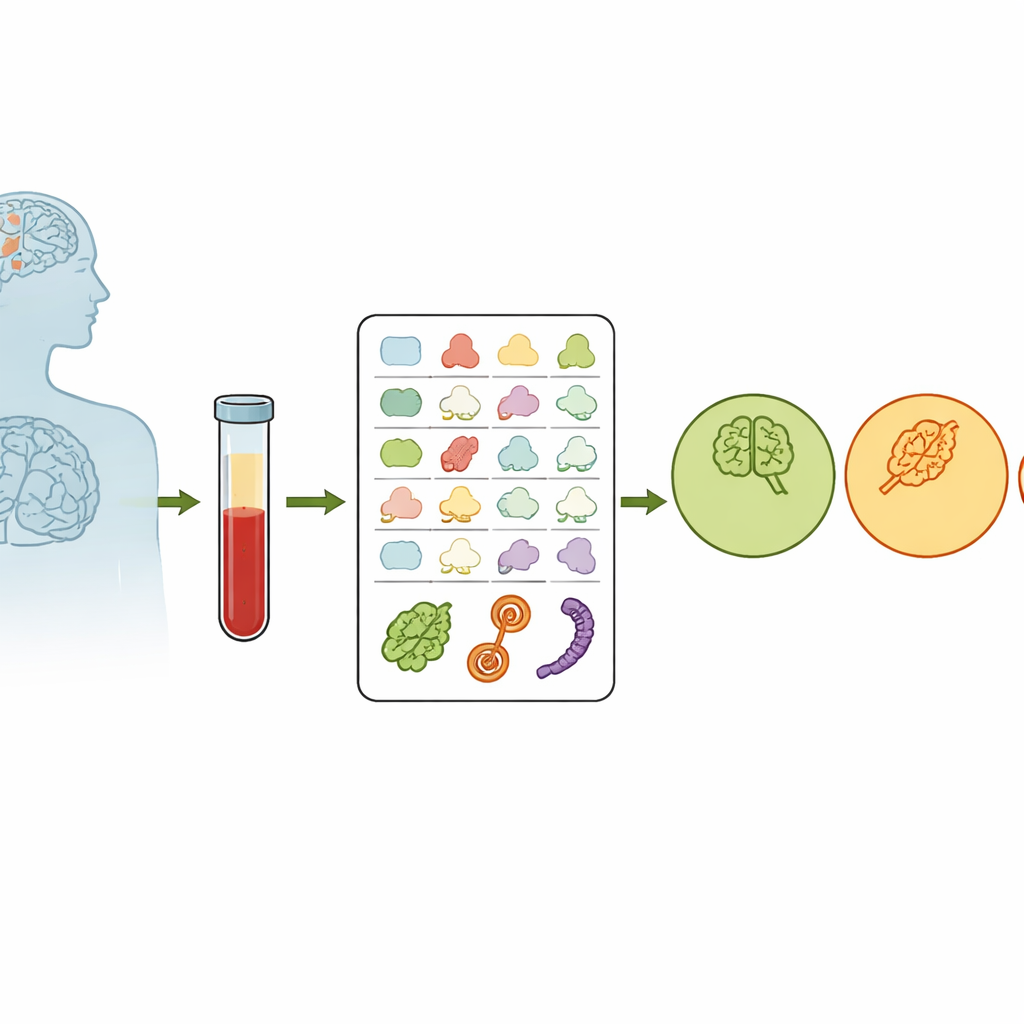
Strukturelle Fingerabdrücke im Blut finden
Bei fast 900 markierten Proteinfragmenten beobachteten die Forschenden einen subtilen, aber konstanten Trend: Mit dem Übergang von gesund zu MCI zu Alzheimer wurden bestimmte Proteinoberflächen weniger exponiert und zeigten größere Variabilität zwischen den Personen. Dieses Muster passt zur Vorstellung, dass die Kontrolle der Proteinfaltung im Körper mit dem Fortschreiten der Krankheit abnimmt. Das Team untersuchte außerdem, wie ein wichtiger genetischer Risikofaktor für Alzheimer, die APOE ε4-Variante, die Proteinstruktur beeinflusst. Sie fanden, dass Personen mit zwei Kopien von ε4 charakteristische strukturelle Veränderungen in mehreren Proteinen zeigten, die mit dem APOE-Protein interagieren, was darauf hindeutet, dass dieses Risikogen nicht nur die Anwesenheit bestimmter Proteine verändert, sondern auch deren Faltung und Anordnung.
Verknüpfung von Blutproteinen mit Stimmung und Verhalten
Alzheimer betrifft weit mehr als das Gedächtnis; Symptome wie Unruhe, Depression und Halluzinationen sind häufig und unterscheiden sich oft zwischen Männern und Frauen. Die Forscher kombinierten klinische Bewertungen von 12 Arten neuropsychiatrischer Symptome mit ihren Messungen der Proteinstruktur. Bei beiden Geschlechtern gingen schwerere Symptome tendenziell mit einer stärkeren strukturellen „Verschlossenheit“ der Proteine einher. Einige Proteine, darunter Clusterin und mehrere weitere, die mit Amyloidablagerungen verknüpft sind, korrelierten bei Männern und Frauen ähnlich mit der Symptomschwere, während andere geschlechtsspezifische Muster zeigten. Diese Ergebnisse deuten darauf hin, dass die Struktur von Blutproteinen nicht nur das Vorhandensein der Krankheit widerspiegeln könnte, sondern auch, wie sie sich in Verhalten und Stimmung äußert.
Ein Drei-Protein-Panel zur Klassifizierung des Krankheitsstadiums
Um diese komplexen Messwerte in etwas Klinisch Nützliches zu überführen, speiste das Team die Strukturdaten in 18 verschiedene maschinelle Lernverfahren. Das leistungsstärkste Modell, basierend auf Deep Learning, stützte sich auf nur drei Proteinfragmente aus C1QA, Clusterin (auch CLUS genannt) und Apolipoprotein B (ApoB). Mithilfe nur der strukturellen Messwerte dieser drei Fragmente sortierte das Modell Personen in unabhängigen Tests etwa 83 % der Zeit korrekt in die Gruppen gesund, MCI oder Alzheimer ein. Bei leichteren Zweierunterscheidungen – etwa gesund versus MCI oder MCI versus Alzheimer – war die Leistung des Panels noch stärker, mit Genauigkeitsmaßen, die mit vielen derzeitigen blutbasierten Ansätzen, die sich auf Proteinmengen statt auf Struktur konzentrieren, vergleichbar oder besser sind.
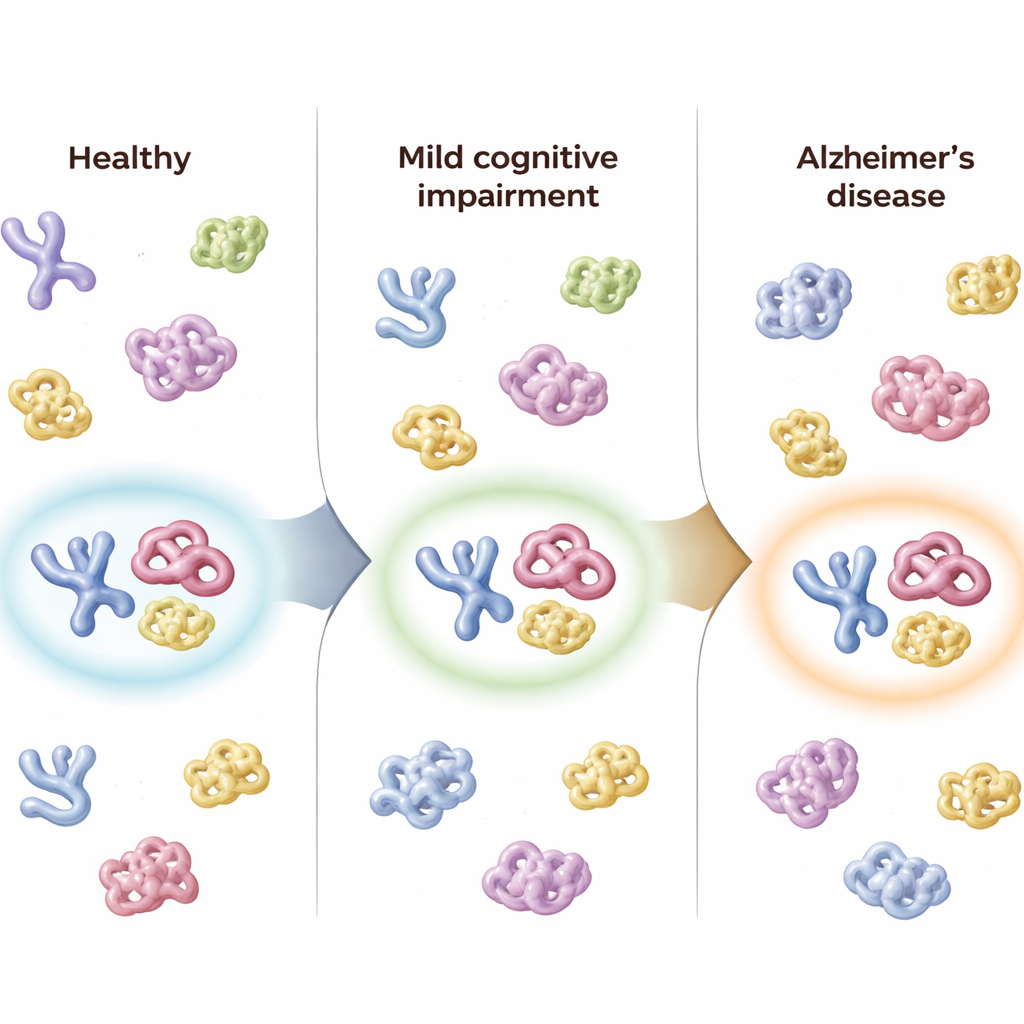
Betreuung von Personen über die Zeit
Die Forschenden verfügten außerdem über Nachproben von 50 Teilnehmern, die bis zu etwa acht Monate später entnommen wurden. Bei Personen, deren Diagnose sich verschlechterte – etwa von gesund zu MCI oder von MCI zu Alzheimer – verschob sich der kombinierte Score des Drei-Protein-Panels in dieselbe Richtung und reflektierte so den Krankheitsverlauf. Im Gegensatz dazu zeigten Personen mit unverändertem klinischem Status kaum Veränderung ihrer Panel-Werte. Der Gesamt-„Alzheimer-Confidence“-Score des Panels korrelierte stark mit standardisierten kognitiven Tests, mit Maßen der Alltagsfunktion, mit der im MRT sichtbaren Hirnatrophie und mit etablierten Rückenmarksflüssigkeitsmarkern für Amyloid und Tau, was darauf hindeutet, dass das blutbasierte Struktur-Signal den zugrunde liegenden Hirnveränderungen entspricht.
Was das für Patientinnen und Patienten bedeuten könnte
In der Summe zeigen die Ergebnisse, dass kleine, koordinierte Veränderungen in der Form nur weniger häufiger Blutproteine zuverlässig anzeigen können, ob jemand kognitiv gesund, leicht beeinträchtigt oder an Alzheimer erkrankt ist. Da der Test Blut statt Rückenmarksflüssigkeit oder Hirnbildgebung verwendet, ließe er sich prinzipiell für routinemäßiges Screening oder zur Auswahl und Überwachung von Teilnehmern in klinischen Studien skalieren. Die Autoren mahnen, dass größere und längerfristige Studien erforderlich sind und die zugrundeliegende Chemie noch spezialisiert ist. Dennoch deuten ihre Befunde darauf hin, dass die Proteinstruktur – nicht nur die Proteinmengen – eine vielversprechende neue Informationsquelle für das frühere und präzisere Erkennen sowie die Nachverfolgung der Alzheimer-Krankheit darstellt.
Zitation: Son, A., Kim, H., Diedrich, J.K. et al. Structural signature of plasma proteins classifies the status of Alzheimer’s disease. Nat Aging 6, 597–611 (2026). https://doi.org/10.1038/s43587-026-01078-2
Schlüsselwörter: Biomarker der Alzheimer-Krankheit, Bluttest für Demenz, Veränderungen der Proteinfaltung, Maschinelles Lernen zur Diagnose, Clusterin und C1QA