Clear Sky Science · de
Resistenz gegen platinbasierte Chemotherapie bei Lungen- und Ovarialkarzinom wird durch ein therapierbares TGFβ‑seneszenz‑Sekretom angetrieben
Wenn Krebsbehandlung nach hinten losgeht
Platinbasierte Chemotherapie gehört zu den Arbeitspferden der modernen Krebsbehandlung, besonders bei Lungen‑ und Eierstockkrebs. Sie zielt darauf ab, die Tumor‑DNA so schwer zu schädigen, dass Krebszellen sich nicht mehr teilen können. Viele Patientinnen und Patienten erleben zwar zunächst ein Schrumpfen der Tumoren, doch die Krankheit kehrt oft zurück — und ist dann widerstandsfähiger. Diese Studie stellt eine einfache, aber beunruhigende Frage: Können gerade die Medikamente, die Leben retten, den überlebenden Krebszellen auch beim Wiederaufbau helfen? Die Antwort, so zeigen die Autorinnen und Autoren, liegt in einer speziellen Gruppe geschädigter, altern‑ähnlicher Zellen und den starken chemischen Signalen, die sie aussenden.
Das Doppelleben gealterter Krebszellen
Chemotherapie trifft nicht alle Tumorzellen gleich. Manche werden sofort abgetötet, andere treten in einen Zustand ein, der als zelluläre Seneszenz bezeichnet wird — dauerhaft teilungsunfähig, aber noch lebendig. Diese seneszenten Zellen schwellen an und beginnen, ein Cocktail aus Proteinen und Signalen auszuschütten, bekannt als seneszenzassoziiertes sekretorisches Phänotyp (SASP). An humanen Lungen‑ und Eierstockkrebszellen im Labor sowie in Mausmodellen zeigten die Forschenden, dass Platinpräparate wie Cisplatin und Carboplatin besonders potente seneszente Zellen erzeugen. Wenn frische Krebszellen mit dem Medium aus diesen seneszenten Kulturen behandelt wurden, wuchsen sie schneller, wanderten leichter und bildeten größere, aggressivere Cluster und Kugeln als Kontrollzellen.
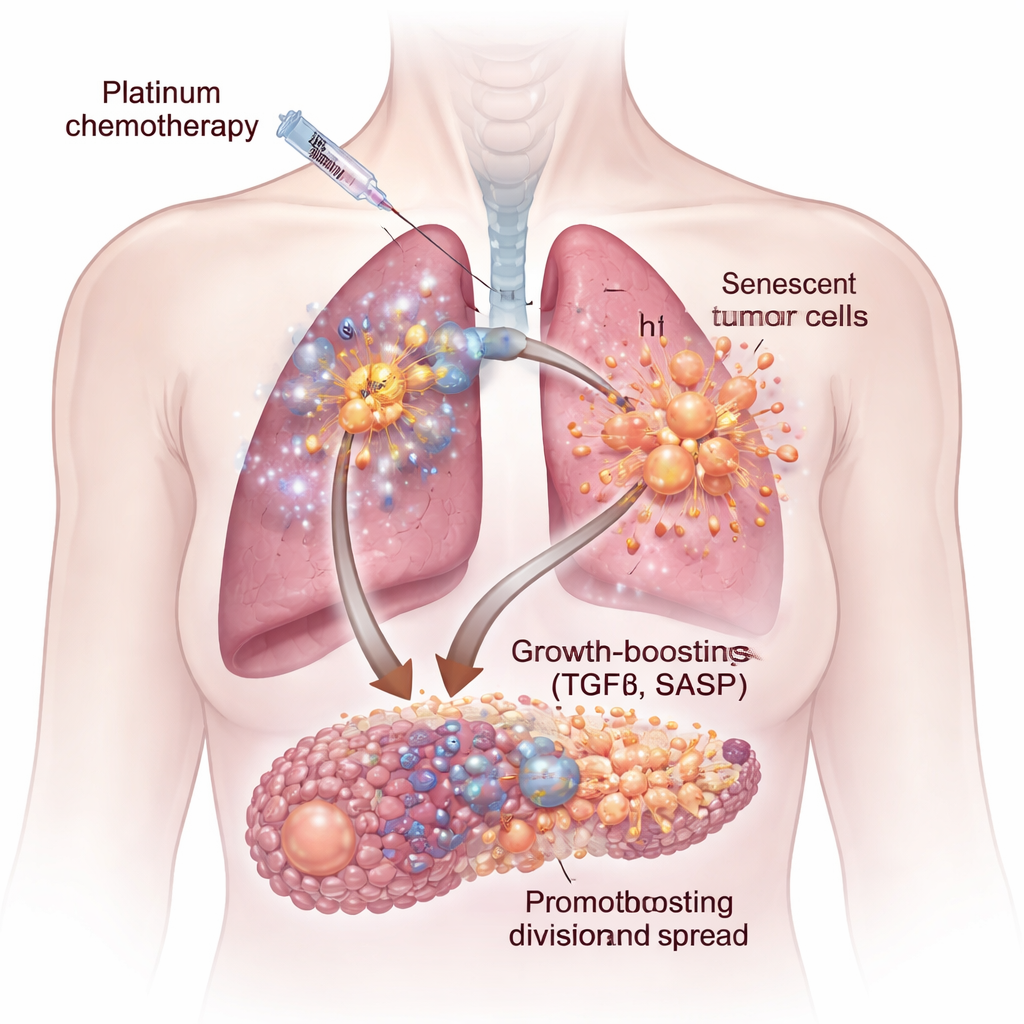
Ein verborgenes Wachstumssignal: TGFβ
Nicht alle Chemotherapeutika lösten die gleichen schädlichen Sekrete aus. Verglich das Team Platinpräparate mit zwei anderen verbreiteten Wirkstoffen, Docetaxel und Palbociclib, produzierte nur die Platinbehandlung ein SASP, das das Tumorwachstum stark förderte. Mithilfe von Genexpressionsstudien, Proteinanalyse und einem Hochdurchsatz‑Mikroumgebungs‑Microarray identifizierten sie einen zentralen Schuldigen: das Signalmolekül Transforming Growth Factor‑beta, kurz TGFβ. Seneszente Zellen, die durch Cisplatin induziert wurden, zeigten eine Anreicherung mehrerer TGFβ‑Formen und verwandter Signalwege. Die Zugabe von gereinigtem TGFβ an Krebszellen ahmte den mit seneszenten Zellen beobachteten Wachstumsboost nach und hebt diese Zytokin‑Familie als zentralen Treiber des pro‑tumoralen Sekretoms hervor.
Wie das Signal Krebszellen umprogrammiert
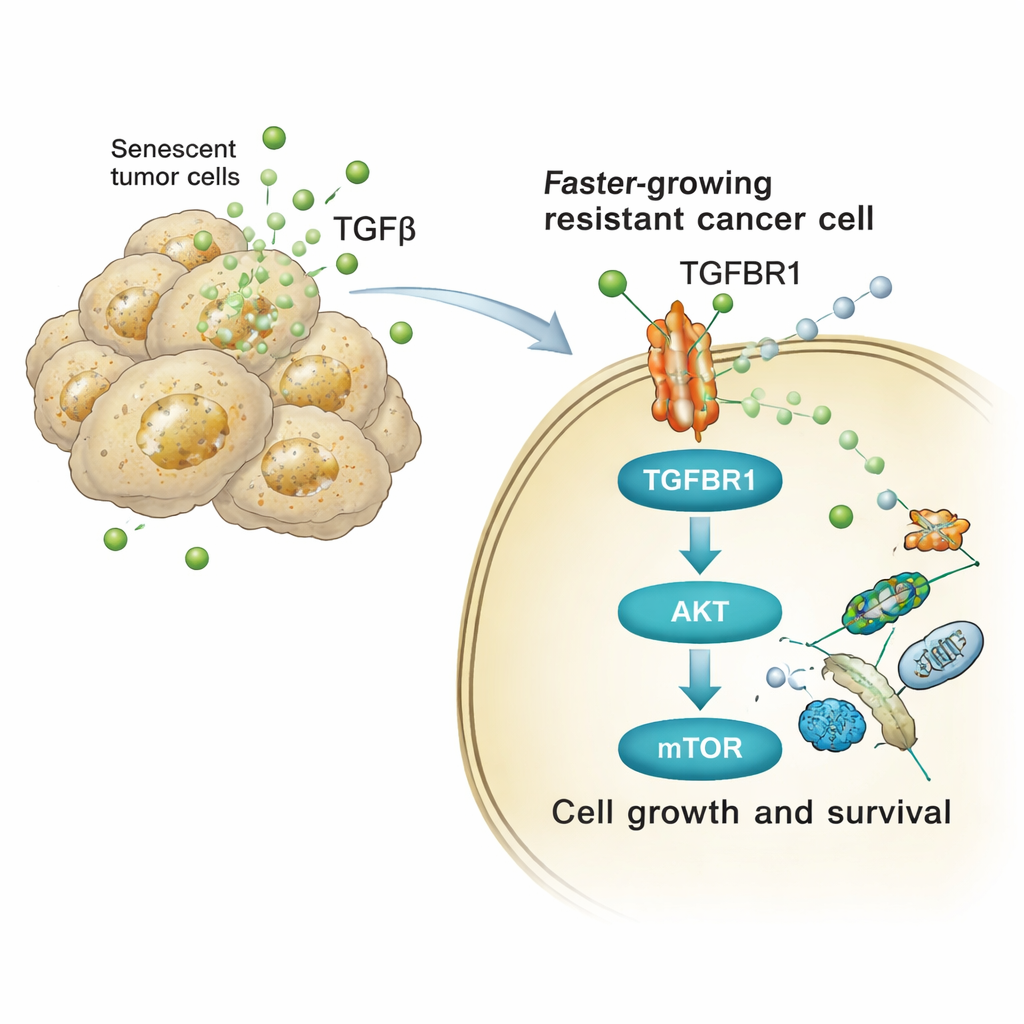
Die Studie verfolgte anschließend, wie diese TGFβ‑reichen Signale das Verhalten benachbarter Tumorzellen verändern. Auf der Oberfläche empfangender Zellen bindet TGFβ an einen Rezeptor namens TGFBR1. Dieser schaltet eine interne Kaskade von Proteinen ein — insbesondere die AKT‑ und mTOR‑Signalwege —, die bekannt sind für ihre Kontrolle von Zellwachstum, Stoffwechsel und Überleben. In humanen und Maus‑Lungenkrebszellen erhöhte die Exposition gegenüber Cisplatin‑abgeleiteten Sekreten schnell die aktivierten (phosphorylierten) Formen von AKT und dessen Ziel p70S6K und steigerte die Expression von Zellzyklusgenen. Das Blockieren von TGFBR1 mit dem Wirkstoff Galunisertib oder die direkte Hemmung von mTOR bremste diese Signalkaskade weitgehend und reduzierte die erhöhte Proliferation, Kolonie‑Bildung und das invasive Kugelwachstum, das durch das seneszente Sekretom ausgelöst wurde.
Von Mäusen zu Patienten: Eine gemeinsame Schwachstelle
Diese Mechanismen beschränkten sich nicht auf Petrischalen. In Mäusen mit Lungentumoren führten Mischungen aus seneszenten und nicht‑seneszenten Krebszellen zu schneller wachsenden Tumoren und kürzerem Überleben, während die Eliminierung seneszenter Zellen oder das Blockieren von TGFBR1 diesen Effekt abschwächte. Bei genetisch veränderten Mäusen mit Lungentumoren akkumulierten nach Standardbehandlung mit Cisplatin Tumoren seneszente Marker zusammen mit hoher AKT/mTOR‑Aktivität in benachbarten, noch teilenden Zellen. Die Kombination von Cisplatin mit einer TGFBR1‑Hemmung oder senolytischen Wirkstoffen (die selektiv seneszente Zellen abtöten) verringerte die Tumorlast und verlängerte das Überleben im Vergleich zur alleinigen Chemotherapie. Entscheidend zeigen Analysen humaner Lungen‑ und hochgradig seröser Ovarialkarzinomproben nach platinbasierter Therapie ähnliche Muster: vermehrte Seneszenzmarker und verstärkte AKT/mTOR‑Signalgebung in der Tumormikroumgebung, besonders in Regionen mit vielen seneszenten Zellen.
Aus einer Schwäche einen Vorteil machen
Für Laien lautet die Kernaussage: Platinchemotherapie kann eine Population geschädigter, aber gefährlicher „Zombie“‑Zellen zurücklassen. Diese seneszenten Tumorzellen teilen sich zwar nicht mehr, senden jedoch TGFβ‑reiche Signale aus, die benachbarte Krebszellen reaktivieren und Tumoren beim Nachwachsen und bei der Resistenzbildung helfen. Die ermutigende Nachricht ist, dass sich diese Verwundbarkeit gezielt angreifen lässt. In präklinischen Modellen für Lungen‑ und Eierstockkrebs machten Wirkstoffe, die den TGFβ‑Rezeptor TGFBR1 blockieren, oder senolytische Substanzen in Kombination mit Platinchemotherapie diese wirksamer und verbesserten das Überleben ohne offensichtliche zusätzliche Toxizität. Die Arbeit weist auf zukünftige klinische Studien hin, die Standard‑Platintherapie mit senolytischen oder anti‑TGFβ‑Strategien kombinieren, mit dem Ziel, die Vorteile der Chemotherapie zu erhalten und gleichzeitig ihre verborgenen, seneszenzgetriebenen Nebenwirkungen zu entschärfen.
Zitation: González-Gualda, E., Reinius, M.A.V., Macias, D. et al. Treatment resistance to platinum-based chemotherapy in lung and ovarian cancer is driven by a targetable TGFβ senescent secretome. Nat Aging 6, 368–392 (2026). https://doi.org/10.1038/s43587-025-01054-2
Schlüsselwörter: Chemotherapie‑Resistenz, zelluläre Seneszenz, TGFβ‑Signalgebung, Lungenkrebs, Eierstockkrebs