Clear Sky Science · de
DNA-Schäden in Makrophagen treiben Immun-Autoreaktivität durch Präsentation nuklearer Antigene voran
Wenn zellulärer Verschleiß das Immunsystem gegen uns wendet
Mit dem Alter steigt das Risiko für Autoimmunerkrankungen, bei denen das Immunsystem beginnt, den eigenen Körper anzugreifen. Diese Studie untersucht einen überraschenden Übeltäter: alltägliche DNA-Schäden in Immunzellen, den Makrophagen. Indem die Forschenden nachverfolgten, wie diese Schäden verändern, was Makrophagen anderen Immunzellen präsentieren, offenbaren sie eine mögliche fehlende Verbindung zwischen dem Altern und der Entstehung von Erkrankungen wie Lupus.
Wächter des Körpers außer Kontrolle
Makrophagen sind Frontkämpfer, die Mikroben und Zelltrümmer aufnehmen und dann Proteinfragmente T-Zellen präsentieren, wodurch das Immunsystem entscheidet, was angegriffen wird. Das Team erzeugte Mäuse, deren Makrophagen in einem wichtigen DNA-Reparaturprotein, ERCC1-XPF, defekt waren, sodass diese Zellen anhaltende DNA-Schäden aufwiesen. Mit zunehmendem Alter entwickelten diese Mäuse Kennzeichen von Autoimmunität: entzündliche Herde in den Nieren, Ablagerungen von Immunkomplexen und Komplementproteinen, vergrößerte Milz und hohe Spiegel an antinukleären Antikörpern, ähnlich denen, die bei natürlich alten Tieren beobachtet werden. Detaillierte Immunprofilierungen zeigten eine Expansion von Plasmazellen, aktivierten T-Zellen und natürlichen Killerzellen — alles Zeichen eines chronisch stimulierten Immunsystems.
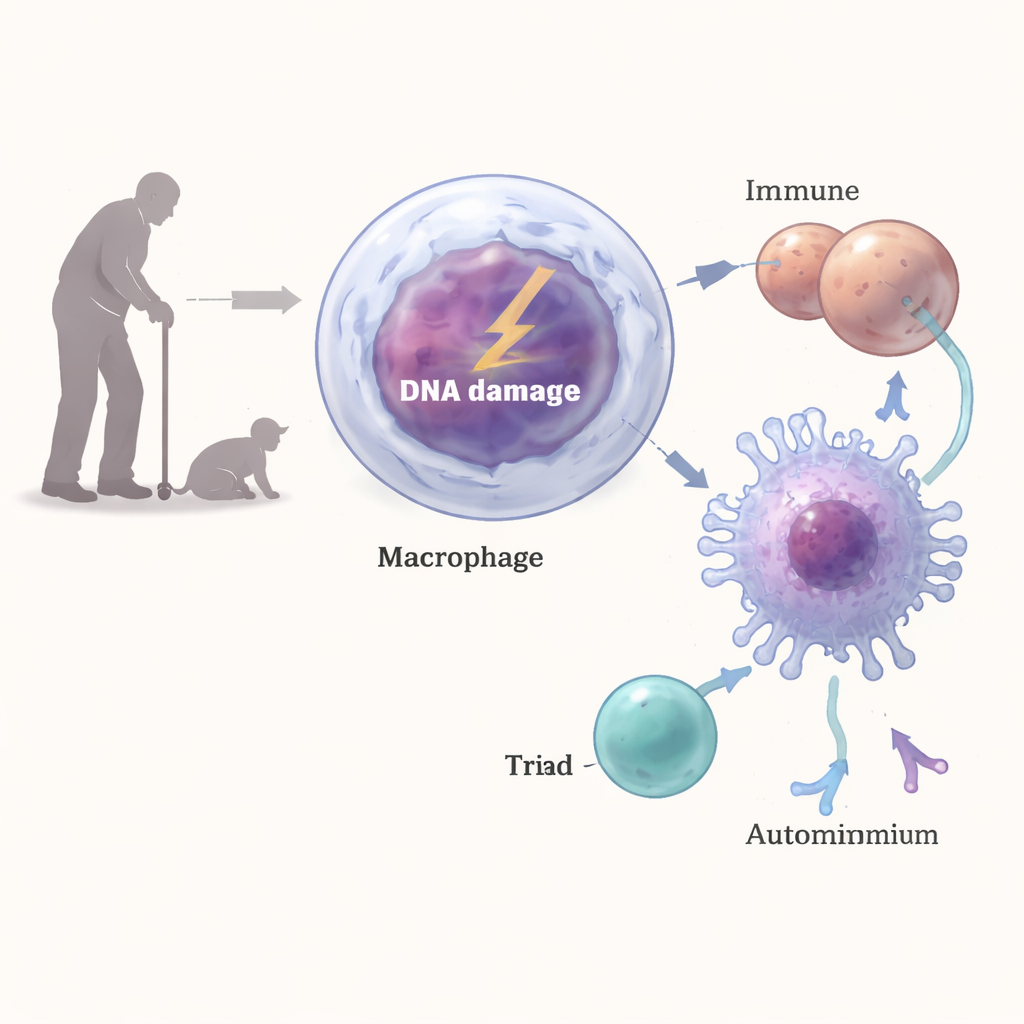
Von gebrochener DNA zu selbstzielenden T-Zellen
Wie konnten DNA-Schäden in Makrophagen eine so starke autoimmunähnliche Reaktion auslösen? Die Forschenden stellten fest, dass DNA-Brüche in diesen Zellen eine klassische Schadenserkennungs-Kaskade aktivierten, an der Enzyme wie ATM, ATR und DNA-PK beteiligt sind. Diese Signalgebung erhöhte die Oberflächenexpression von MHC Klasse II, den molekularen Vitrinen, mit denen Proteinfragmente CD4-T-Zellen präsentiert werden. Wenn DNA-geschädigte Makrophagen mit T-Zellen zusammengebracht wurden, führten sie zu stärkerer T-Zell-Aktivierung und Interferon-gamma-Produktion als normale Makrophagen. Die Blockade von MHC-II oder das Eingreifen in die DNA-Schadensantwort kehrte einen Großteil dieses Effekts um, und in lebenden Tieren reduzierten Antikörper gegen MHC-II oder die Depletion von CD4-T-Zellen Nierenentzündungen und Autoantikörperspiegel.
Selbstproteine aus dem Zellkern werden ausgestellt
Um genau zu sehen, was geschädigte Makrophagen den T-Zellen zeigten, isolierte das Team die an MHC-II gebundenen Peptide und analysierte sie mittels Massenspektrometrie. Im Vergleich zu normalen oder mit Lipopolysaccharid stimulierten Zellen präsentierten DNA-geschädigte Makrophagen ein auffallend anderes Peptidrepertoire. Anstatt überwiegend Membran- und extrazellulärer Proteine enthielten ihre MHC-II-Moleküle vermehrt Fragmente, die von nukleären und ribosomalen Proteinen stammten, darunter Histone und andere eng mit DNA assoziierte Komponenten. Als einige dieser nukleären Peptide synthetisch hergestellt und zur Re-Stimulation von Immunzellen der genetisch veränderten Mäuse verwendet wurden, lösten sie starke T-Zell-Antworten aus, was darauf hindeutet, dass diese selbststammenden Fragmente tatsächlich immunogen sind.
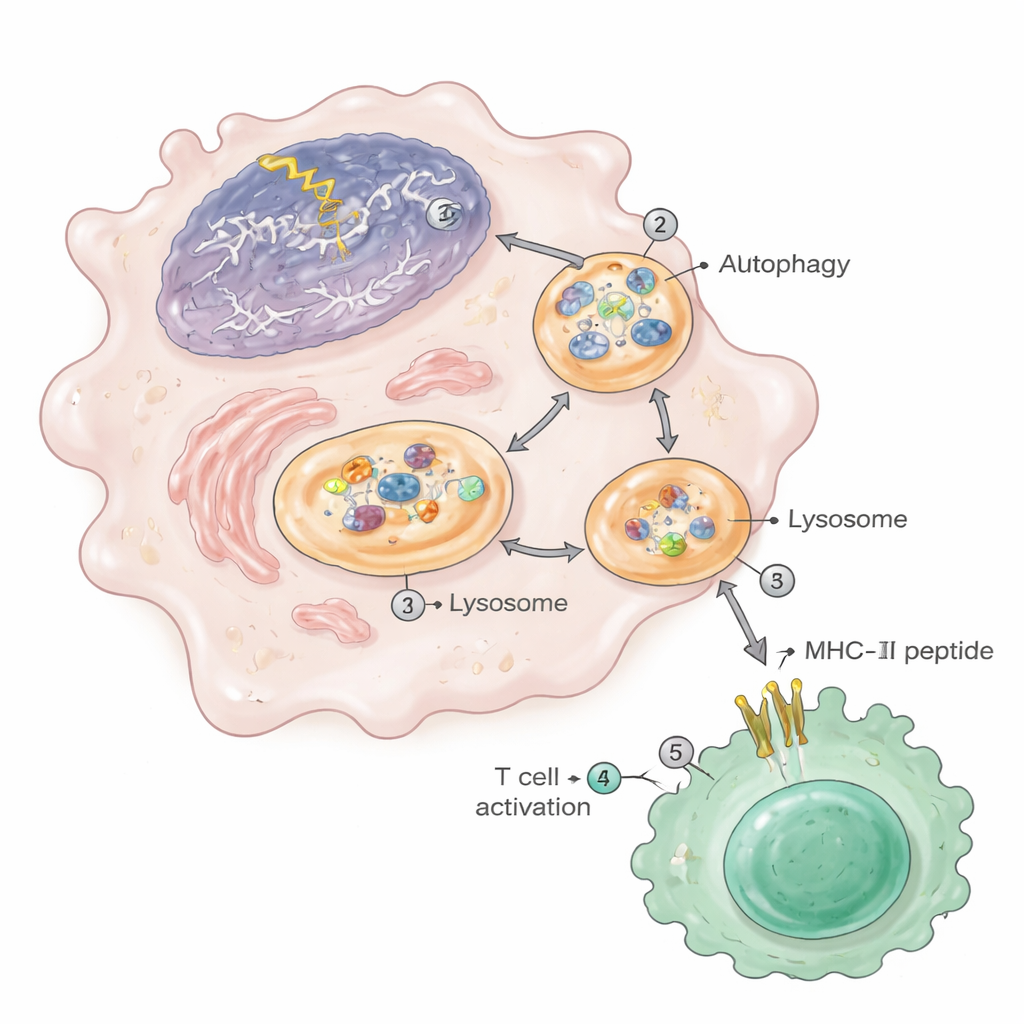
Autophagie: Der Aufräumweg, der Autoimmunität antreibt
Der Weg nuklearer Materialien zur MHC-II-Präsentation hing stark von der Autophagie ab, dem zellulären Recycling-System. Unter DNA-Schaden wurde die Autophagie hochreguliert und transportierte Chromatinfragmente — aus dem eigenen Zellkern — in Autophagosomen, die dann mit Lysosomen verschmolzen, wo Proteine in Peptide zerlegt werden. Diese Lysosomen in geschädigten Makrophagen enthielten erhöhte Mengen an nuklearen und ribosomalen Proteinen. Als die Forschenden die Autophagie pharmakologisch blockierten oder genetisch ein essentielles Autophagie-Gen (Atg5) in denselben myeloiden Zellen entfernten, zeigten die Tiere weniger Nierenläsionen, weniger aktivierte T-Zellen und Plasmazellen sowie eine dramatische Reduktion nukleärer Peptide auf MHC-II. Ähnliche Chromatinfragmente und eine erhöhte Antigenpräsentation fanden sich in Makrophagen von lupusanfälligen Mäusen, in humanen Monozytenzelllinien nach Exposition gegenüber DNA-schädigenden Wirkstoffen und in Makrophagen sehr alter Mäuse.
Warum das für Altern und Autoimmunerkrankungen wichtig ist
Zusammengefasst sprechen die Befunde für eine einfache, aber kraftvolle Idee: Mit dem Alter sammeln sich DNA-Schäden in Makrophagen an, die wiederum über Autophagie nukleare Trümmer entsorgen. Dabei zerlegen sie unbeabsichtigt nukleares Material in Peptide, die auf MHC-II geladen und den T-Zellen präsentiert werden, als wären sie fremd. Im Verlauf der Zeit kann diese chronische Exposition gegenüber nuklearen Selbstantigenen das Immunsystem darauf trainieren, gegen den eigenen Körper zu reagieren und so Autoimmunität zu fördern. Indem die Studie diesen Weg — von DNA-Schaden über Autophagie zur Präsentation nuklearer Antigene — präzisiert, eröffnet sie neue Ansätze, altersbedingte Autoimmunität zu dämpfen, etwa durch Verbesserung der DNA-Reparatur, gezielte Modulation der Autophagie oder selektive Blockade der Präsentation nuklearer Selbstpeptide, ohne die lebenswichtigen Abwehrfunktionen des Immunsystems abzuschalten.
Zitation: Niotis, G., Arvanitaki, E.S., Theodorakis, E. et al. DNA damage in macrophages drives immune autoreactivity via nuclear antigen presentation. Nat Aging 6, 393–413 (2026). https://doi.org/10.1038/s43587-025-01053-3
Schlüsselwörter: Altern und Autoimmunität, DNA-Schäden, Makrophagen, Autophagie, antinukleäre Antikörper