Clear Sky Science · de
Senotoxine zielen auf Seneszenz über lipidspezifische Bindung, Ionenungleichgewicht und Umbau des Lipidoms
Warum das Töten von „Zombie“-Zellen die Krebstherapie schärfen könnte
Wenn wir altern – oder harte Behandlungen wie Chemotherapie durchlaufen – hören manche Zellen auf, sich zu teilen, sterben aber nicht. Diese „Zombie“-Zellen, bekannt als seneszente Zellen, schütten entzündungsfördernde Moleküle aus, die Gewebe schädigen und Tumoren ein Wiederauftreten erleichtern können. Die vorliegende Studie untersucht eine überraschende neue Möglichkeit, solche problematischen Zellen gezielt mit einem aus Giftstoffen stammenden Protein zu eliminieren, was Krebsbehandlungen potenziell wirksamer und sicherer machen könnte.
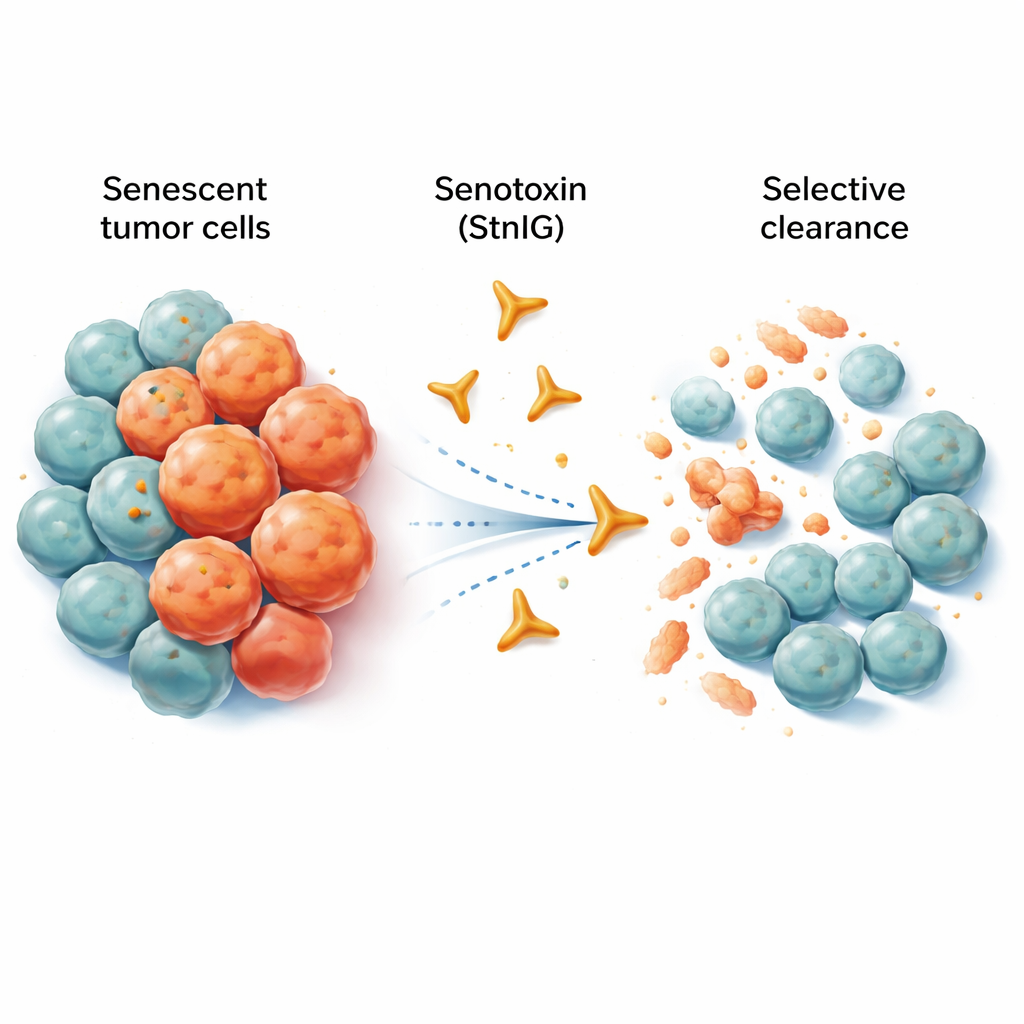
Alte Zellen, die nicht aufgeben
Seneszente Zellen sind wie pensionierte Mitarbeiter, die ihre Schreibtische weiter belegen und das Büro stören. Sie vermehren sich nicht mehr, geben aber einen Cocktail entzündlicher Signale ab, der umliegendes Gewebe schwächen, das Altern fördern und sogar Tumorwachstum und -ausbreitung unterstützen kann. Die Chemotherapie tötet zwar viele Krebszellen, hinterlässt aber häufig einen Bestand seneszenter Zellen in und um den Tumor. Diese Verweiler können chronische Entzündungen, Nebenwirkungen und schließlich Rückfälle antreiben. Experimentelle Medikamente, sogenannte Senolytika, zielen darauf ab, seneszente Zellen zu entfernen, viele treffen jedoch auch gesunde Zellen, wirken nur in engen Dosisbereichen oder sind für den Körper schwer aufzunehmen.
Meeranemonengift als Präzisionswerkzeug
Die Forschenden wandten sich den Spezialisten des natürlichen Zelltötens zu: Tiergiften. Sie konzentrierten sich auf ein porenbildendes Protein namens Sticholysin I (StnI), das in einer karibischen Seeanemone vorkommt. Dieses Protein kann winzige Löcher in Zellmembranen stechen. Das Team entdeckte, dass StnI und eine verfeinerte, von ihnen entwickelte Version namens StnIG seneszente Krebszellen deutlich besser töten als ihre nicht-seneszenten Nachbarn. Über mehrere menschliche Krebszelltypen hinweg (Melanom, Leber-, Lungen- und nervenabgeleitete Tumoren), die durch Chemotherapie in Seneszenz versetzt wurden, vernichteten StnI und besonders StnIG die gealterten Zellen bei deutlich niedrigeren Dosen als nötig, um aktiv wachsende Zellen zu beeinträchtigen. StnIG war selektiver als ein führendes experimentelles Senolytikum, Navitoclax, was nahelegt, dass sorgfältig abgestimmte Toxine aktuelle Ansätze übertreffen können.
Wie veränderte Zellmembranen zur Achillesferse werden
Seneszente Zellen ändern sich nicht nur innerlich; ihre Außenmembran – die fetthaltige Hülle jeder Zelle – wird ebenfalls umgebaut. In gesunden Zellen liegen bestimmte Lipide vorwiegend auf der Innenseite der Membran, für die Außenwelt verborgen. In seneszenten Zellen bricht dieses Gleichgewicht zusammen und diese Lipide werden exponiert. Mithilfe detaillierter chemischer Analysen und Computersimulationen zeigte das Team, dass StnIG diese veränderte Lipidlandschaft erkennt und daran haftet. Seine Struktur ist besonders gut darauf ausgelegt, an spezifische Lipide anzudocken, die seneszente Zellen an ihrer Oberfläche freilegen. Einmal angeheftet, bildet StnIG Poren, die es geladenen Atomen, also Ionen, ermöglichen, sehr unausgeglichen hinein- und herauszufließen.
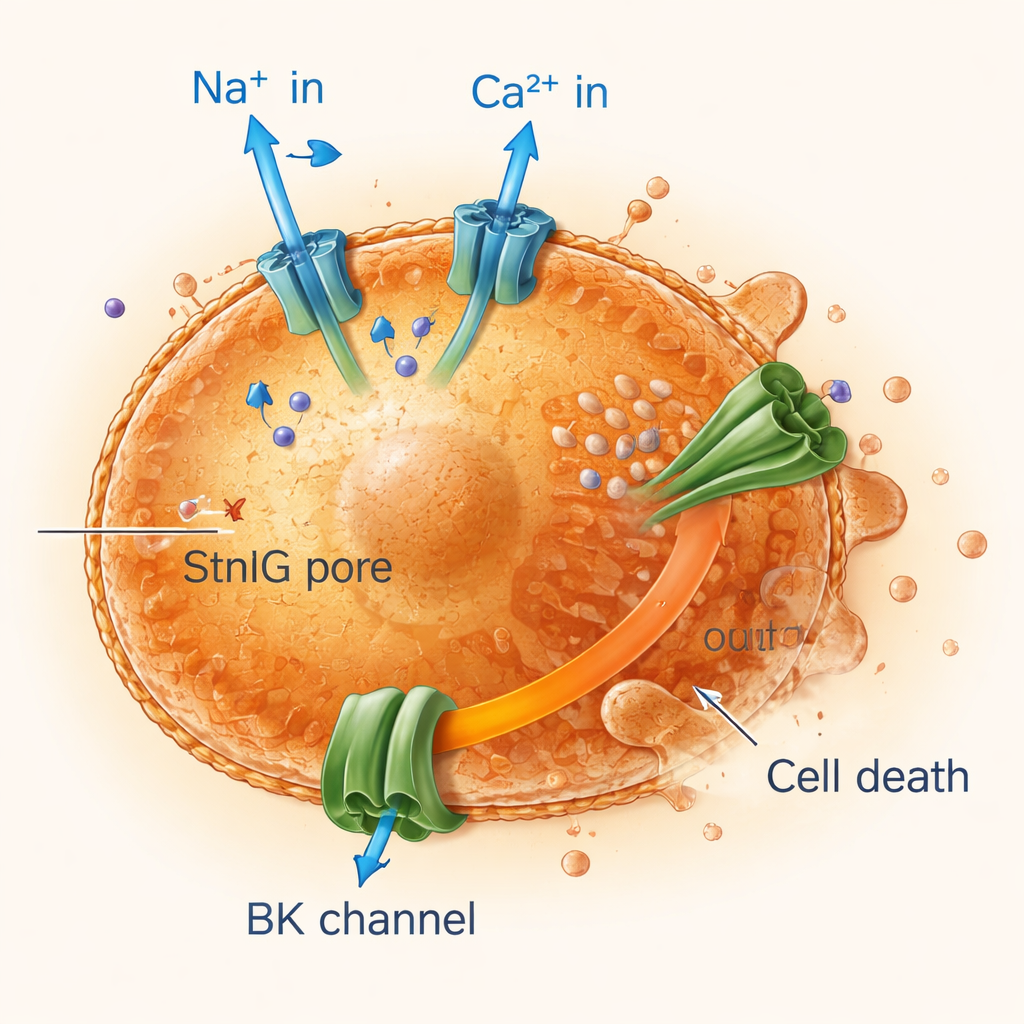
Alte Zellen durch Ionenungleichgewicht kurzschließen
Durch die Messung von Elektrizität und Ionenbewegungen über Zellmembranen stellten die Forschenden fest, dass StnIG-Poren Natrium- und Calciumionen schnell in seneszente Zellen strömen lassen, während Kalium kontinuierlich ausläuft. Der Calciumanstieg aktiviert große Kaliumkanäle, was den Kaliumverlust weiter verstärkt – Kalium ist entscheidend für die Aufrechterhaltung des Zellvolumens und des Überlebens. Seneszente Zellen, die bereits weniger flexibel und fragiler sind als gesunde, können mit dieser anhaltenden Ionenstörung nicht umgehen. Ihre Mitochondrien – die Kraftwerke der Zelle – verlieren ihr elektrisches Potenzial, die Energieproduktion bricht ein und die Zellen durchlaufen programmierte Todesformen, darunter Apoptose und ein feuriger, entzündlicher Tod namens Pyroptose. Das Blockieren des Calcium-Einstroms oder von Kaliumkanälen schützte seneszente Zellen und bestätigte, dass diese Ionenstörung zentral für die Wirkung des Toxins ist.
Von Zellkulturen zu lebenden Tieren
Das Team prüfte anschließend, ob die Strategie auch in lebenden Organismen funktioniert. In Zebrafisch-Embryonen, die humane seneszente Melanomzellen trugen, reduzierte eine niedrige Dosis StnIG die Zahl dieser Zellen ebenso effektiv wie Navitoclax, ohne offensichtliche Toxizität. In Mausmodellen für Melanom und Leberkrebs verlangsamte eine Chemotherapie mit einem Zellzyklushemmer (Palbociclib) das Tumorwachstum, indem viele Krebszellen in Seneszenz getrieben wurden. Als die Forschenden StnIG intermittierend hinzufügten, schrumpften die Tumoren oder gingen wirksamer in Remission als mit Chemotherapie allein und ähnlich effektiv wie die Kombination aus Chemotherapie und Navitoclax. Wichtig ist, dass StnIG-behandelte Mäuse nur begrenzte Nebenwirkungen und keinen klaren Schaden in wichtigen Organen zeigten, obwohl das Blutkalium bei Tieren mit seneszenten Tumoren anstieg – vermutlich ein Spiegelbild der massiven Kaliumfreisetzung, als Tumorzellen zerstört wurden.
Was das für die künftige Krebsbehandlung bedeutet
Diese Arbeit führt den Begriff „Senotoxine" ein: gentechnisch optimierte, von Giften inspirierte Proteine, die die einzigartigen Membran- und Ionenhandhabungs-Eigenheiten seneszenter Zellen ausnutzen. Indem sie sich auf veränderte Lipide fokussieren und tödliche Ionenungleichgewichte erzwingen, können StnIG und ähnliche Moleküle schädliche seneszente Zellen selektiv beseitigen und dabei das meiste gesunde Gewebe verschonen. Zusammen mit Chemotherapie eingesetzt, könnten solche Senotoxine eines Tages helfen, die Zombie-Zellen zu beseitigen, die Rückfälle und chronische Entzündungen antreiben, Krebsbehandlungen dauerhafter machen und einige langfristige Nebenwirkungen lindern.
Zitation: Moral-Sanz, J., Fernández-Carrasco, I., Ramponi, V. et al. Senotoxins target senescence via lipid binding specificity, ion imbalance and lipidome remodeling. Nat Aging 6, 349–367 (2026). https://doi.org/10.1038/s43587-025-01030-w
Schlüsselwörter: zelluläre Seneszenz, Senolytika, Krebstherapie, aus Gift stammende Medikamente, Ionenkanäle