Clear Sky Science · de
Axicabtagene ciloleucel in Kombination mit Rituximab bei refraktärem großzelligem B‑Zell‑Lymphom: die Phase‑2‑Einarmstudie ZUMA‑14
Warum diese neue Lymphom‑Behandlung wichtig ist
Bei Menschen mit einem aggressiven Blutkrebs namens großzelliges B‑Zell‑Lymphom reicht die Standardchemotherapie nicht immer aus, und selbst leistungsfähige zellbasierte Therapien können mit der Zeit an Wirkung verlieren. In dieser Studie wurde eine neue Strategie geprüft: die Kombination einer maßgeschneiderten Immunzelltherapie mit einem lange etablierten Antikörper, um zu testen, ob ein gleichzeitiger Angriff auf zwei Fronten Rückfälle verhindern kann, ohne zusätzliche gefährliche Nebenwirkungen zu verursachen.
Zwei Medikamente im Team gegen einen Krebs
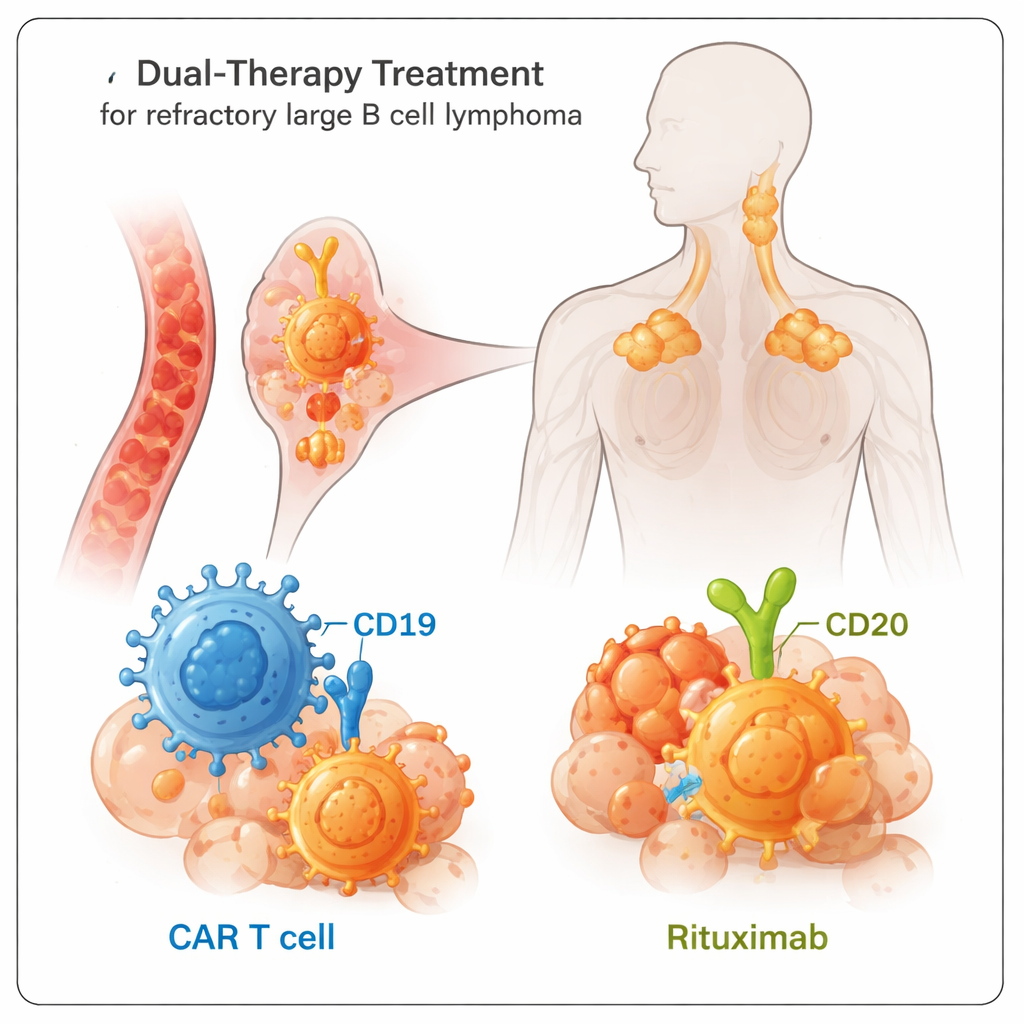
Die Studie konzentrierte sich auf Erwachsene, deren Lymphom auf frühere Behandlungen nicht angesprochen hatte — eine Gruppe mit meist schlechten Prognosen. Alle Teilnehmenden erhielten Axicabtagene ciloleucel, kurz axi‑cel, eine Form der CAR‑T‑Zelltherapie, die aus ihren eigenen T‑Zellen hergestellt und so modifiziert wurde, dass sie Zellen mit dem Marker CD19 angreift. Zusätzlich bekamen sie Rituximab, einen Antikörper, der an einen anderen Marker derselben Krebszellen bindet, CD20. Die Idee war einfach, aber wirkungsvoll: Durch das gleichzeitige Treffen zweier Ziele auf den Lymphomzellen sollte es dem Tumor schwerer fallen, „zu entkommen“, indem er einen dieser Marker verliert.
Stärkere und länger anhaltende Ansprechen
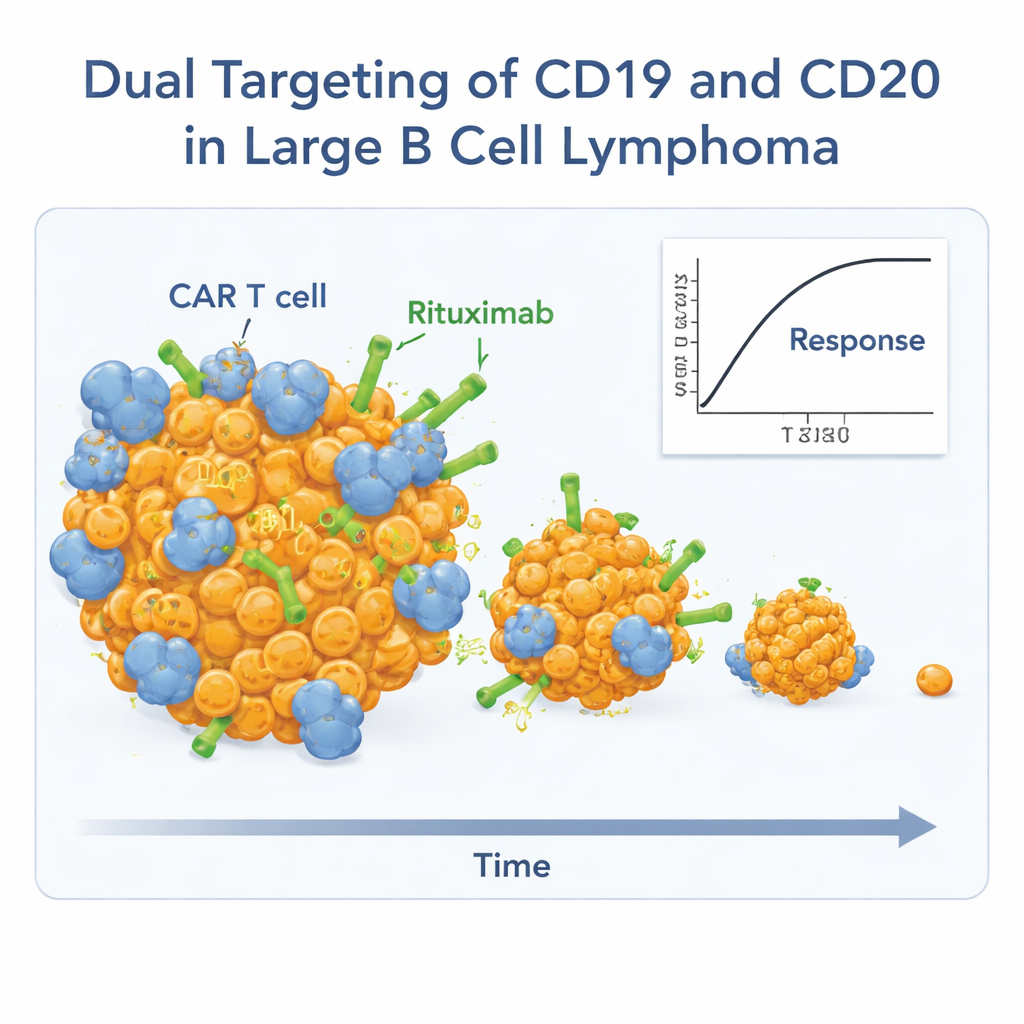
Unter den 26 Personen, die beide Behandlungen erhielten, sahen fast 9 von 10 eine Tumorverkleinerung, und fast drei Viertel hatten bei Bildgebungen keine nachweisbaren Krebszeichen mehr, also ein komplettes Ansprechen. Viele dieser tiefen Ansprechen waren nicht nur kurzlebige Erfolge. Bei etwas mehr als zwei Jahren Nachbeobachtung hatten fast die Hälfte der Teilnehmenden noch anhaltende Ansprechen. Die mediane Ansprechdauer lag bei etwa 26 Monaten, und die typische Zeit bis zum Fortschreiten der Erkrankung betrug knapp zwei Jahre. Das Gesamtüberleben war zum Zeitpunkt der Analyse noch nicht erreicht, was bedeutet, dass mehr als die Hälfte der Patienten noch lebte.
Nebenwirkungen bleiben schwerwiegend, aber beherrschbar
Da CAR‑T‑Therapien das Immunsystem stark aktivieren, können sie intensive Nebenwirkungen hervorrufen, insbesondere das sogenannte Zytokinfreisetzungssyndrom und vorübergehende neurologische Symptome. In dieser Studie hatte nahezu jeder Teilnehmende eine Form von Immunreaktion, doch wichtig ist: Es trat kein schwerstes Stadium des Zytokinfreisetzungssyndroms auf, und schwere neurologische Probleme traten bei etwa 15 % der Patienten auf; alle diese Episoden bildeten sich schließlich zurück. Niedrige Blutwerte und Infektionen waren, wie zu erwarten, häufig, doch die Zugabe von Rituximab schien diese Komplikationen im Vergleich zu früheren Studien mit nur axi‑cel nicht eindeutig zu verschlimmern. Zwei Patienten entwickelten eine zweite Blutkrebserkrankung, ein seltenes, aber bekanntes Langzeitrisiko bei starken Immuntherapien.
Anhaltspunkte dafür, wer am meisten profitiert
Die Forschenden untersuchten auch die zugrunde liegende Biologie des Ansprechens und des Versagens der Kombination. Personen, deren Blut höhere Spiegel an CAR‑T‑Zellen und höhere Rituximab‑Exposition zeigte, neigten dazu, die stärksten und nachhaltigsten Ansprechen zu haben. Nur sehr wenige Patienten hatten über ein ganzes Jahr normale B‑Zellen — die Zellen, die bei dieser Erkrankung entarten —, was zeigt, dass die Therapie weiterhin aktiv war. Tumorproben vor der Behandlung deuteten darauf hin, dass Tumore, die bereits reich an bestimmten Immunzellen wie natürlichen Killerzellen und Gedächtnis‑T‑Zellen waren, eher in langfristiger Remission blieben. Bluttests auf Tumor‑DNA‑Fragmente deuteten ebenfalls darauf hin, dass die frühzeitige Erkennung selbst sehr kleiner Restsignale späteren Rückfall vorhersagen könnte.
Was das für die Zukunft bedeutet
Für Patientinnen und Patienten, deren Lymphom gegen mehrere Behandlungsrunden resistent war, erzielte die Kombination aus axi‑cel und Rituximab hohe Ansprechraten und viele langanhaltende Remissionen, ohne unerwartete Sicherheitsprobleme einzuführen. Obwohl die Studie klein war und keine direkte Vergleichsgruppe hatte, stützen die Ergebnisse die Idee, dass ein gleichzeitiges Anpeilen von CD19 und CD20 das Entkommen des Tumors vor einer Einzelzieltherapie erschweren kann. Dieser Zwei‑Ziel‑Ansatz inspiriert nun die Entwicklung von Next‑Generation‑Zelltherapien, die denselben zweigleisigen Angriff direkt in ein einziges Produkt integrieren sollen, in der Hoffnung, leistungsfähige, dauerhafte Behandlungen bequemer und breiter verfügbar zu machen.
Zitation: Strati, P., Leslie, L., Shiraz, P. et al. Axicabtagene ciloleucel in combination with rituximab for refractory large B cell lymphoma: the phase 2, single-arm ZUMA-14 trial. Nat Cancer 7, 304–315 (2026). https://doi.org/10.1038/s43018-025-01102-1
Schlüsselwörter: CAR‑T‑Zelltherapie, großzelliges B‑Zell‑Lymphom, Rituximab, zwei‑faches Antigen‑Targeting, Resistenz gegen Immuntherapie