Clear Sky Science · de
CAR-adaptierte PIK3CD-Basenbearbeitung erhöht die Anti-Tumor-Wirksamkeit von T‑Zellen
Umschaltung krebsbekämpfender Zellen
Die Therapie mit chimären Antigenrezeptor-(CAR-)T‑Zellen hat die Behandlung mancher Blutkrebserkrankungen revolutioniert, doch viele Patientinnen und Patienten fallen zurück oder sprechen nie an. Ein zentrales Problem ist, dass diese gentechnisch veränderten Immunzellen erschöpfen oder nicht lange genug im Körper verbleiben. Diese Studie stellt eine einfache, aber wirkungsvolle Frage: Statt CARs komplett neu zu entwerfen — was, wenn man die interne Verkabelung der T‑Zellen dezent »neu abstimmen« könnte, damit sie länger leistungsfähig bleiben und das sicher geschieht?
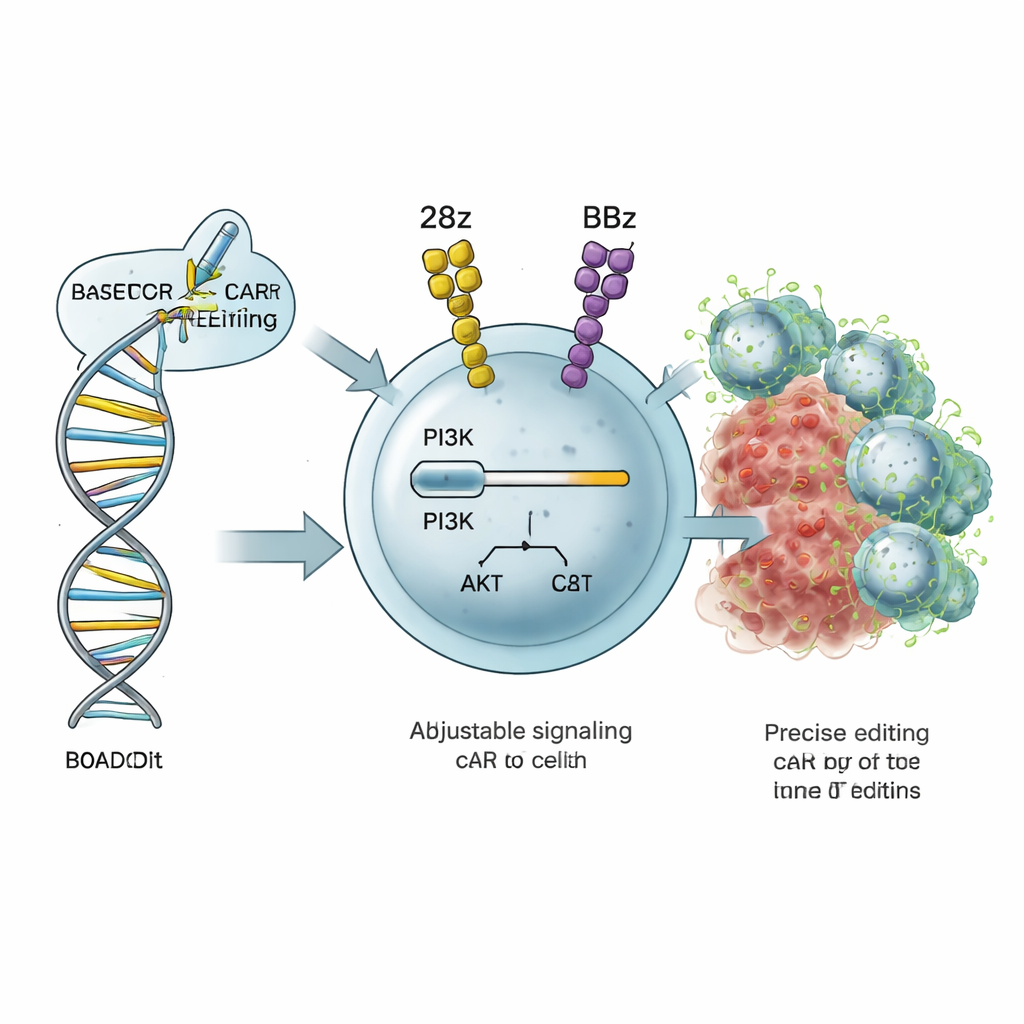
Den Lautstärkeregler der T‑Zelle anpeilen
Krebsvernichtende T‑Zellen sind auf interne Signalnetzwerke angewiesen, die ihnen sagen, wie stark sie aktiviert werden, wie schnell sie sich teilen und ob sie kurzlebige Effektorzellen oder langlebige Gedächtniszellen werden. Ein wichtiger Schaltkreis ist der PI3K–AKT‑Weg, in dem das Protein PI3Kδ — kodiert vom Gen PIK3CD — wie ein Lautstärkeregler für Aktivierung und Stoffwechsel wirkt. Die Autoren entwickelten eine Strategie namens ROADSTAR, die Basenbearbeitung einsetzt, eine hochpräzise Form der CRISPR‑Genomtechnik, um einzelne »Buchstaben« in PIK3CD zu verändern. Anstatt den Weg vollständig an- oder auszuschalten, sucht ROADSTAR nach winzigen Mutationen, die die Signalstärke behutsam erhöhen oder verringern, sodass sie am besten zur jeweiligen CAR‑Architektur in der T‑Zelle passt.
Nützliche Mutationen entdecken
Das Team erstellte eine Bibliothek von 34 verschiedenen Einzelbuchstabenänderungen in der regulatorischen Region von PIK3CD und brachte diese in humane T‑Zellen ein, die bereits eine von zwei gebräuchlichen CAR‑Ausführungen trugen: 28z (basierend auf CD28) und BBz (basierend auf 4‑1BB). Diese CARs unterscheiden sich in ihrer Stimulation der T‑Zellen: 28z neigt zu starker, schneller Attacke, geht aber auch mit Erschöpfung einher, während BBz bessere Überlebensfähigkeit und Gedächtnis fördert, aber weniger aggressiv sein kann. Die bearbeiteten CAR‑T‑Zellen wurden einem »Stresstest« unterzogen, indem sie wiederholt Leukämiezellen ausgesetzt wurden. Mittels Deep Sequencing verfolgten die Forschenden, welche Mutationen es den CAR‑T‑Zellen erlaubten, ihre unbearbeiteten Pendants über mehrere Wochen zu übertreffen.
Zwei Mutationen stachen klar hervor. In BBz‑CAR‑T‑Zellen steigerte eine Veränderung namens E81K leicht die PI3Kδ‑Aktivität und erhöhte die Signale entlang des PI3K–AKT‑Wegs. In 28z‑CAR‑T‑Zellen dämpfte eine andere Veränderung, L32P, die PI3Kδ‑Aktivität. Strukturmodelle legten nahe, dass beide Änderungen die Interaktion von PI3Kδ mit seinem regulatorischen Partner subtil verändern und so die Signalstärke feinjustieren, anstatt sie vollständig an- oder auszuschalten. Wichtig ist, dass die vorteilhafte Mutation für eine CAR‑Architektur nicht dieselbe war wie für die andere — ein Hinweis darauf, dass jede CAR‑Struktur ihre eigene optimale interne Abstimmung benötigt.
Stärkere, robustere und länger anhaltende CAR‑T‑Zellen
Wurden die vielversprechenden Edits einzeln getestet, machte E81K BBz‑CAR‑T‑Zellen bei Kontakt mit Tumorzellen stärker aktiviert, verbesserte ihre Proliferation und erhöhte die Effizienz beim Abtöten von Krebszielen deutlich, auch bei Zielen mit niedrigen Antigenmengen. Diese Zellen differenzierten sich in Effektorgedächtnis‑T‑Zellen, die starke zytotoxische Aktivität mit Persistenz verbanden. In Mausmodellen für Leukämie und metastasiertes Neuroblastom kontrollierten E81K‑editierte BBz‑CAR‑T‑Zellen Tumore vollständiger und wesentlich länger als unbearbeitete BBz‑Zellen und überstanden sogar mehrere Tumor‑Wiederherausforderungen. Detaillierte Einzelzell‑RNA‑ und Stoffwechselprofile zeigten, dass E81K‑Zellen verbesserte mitochondriale Funktion, höhere Reservekapazitäten in Atmung und Glykolyse sowie weniger Erschöpfungszeichen aufwiesen — im Grunde waren sie energiereicher und widerstandsfähiger.
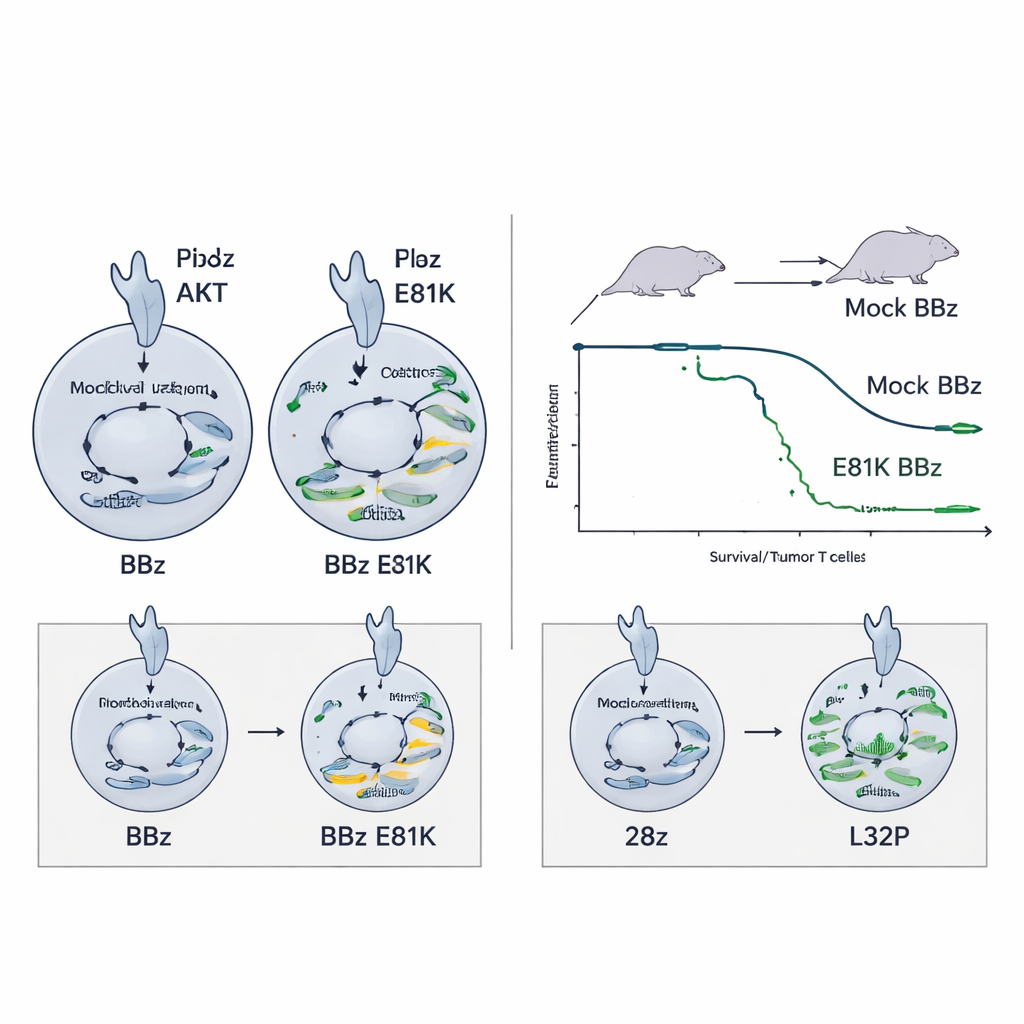
Erschöpfung bei hochaktiven CARs verhindern
Die gleiche E81K‑Steigerung half bei 28z‑CAR‑T‑Zellen nicht — sie konnte sogar schaden, da diese bereits stark signalisieren. In diesem Fall erhöhte zusätzliche PI3K‑Aktivität Marker der Erschöpfung, ohne die Funktion zu verbessern. Hier erwies sich die L32P‑Mutation als besser geeignet: Durch eine moderate Absenkung der PI3K–AKT‑Signalgebung zeigten L32P‑editierte 28z‑CAR‑T‑Zellen reduzierte Grundaktivierung bei gleichzeitig erhalten hoher Tötungskapazität und proliferierten im Laufe der Zeit stärker. Sie behielten außerdem einen weniger differenzierten, gedächtnisähnlichen Zustand bei, einschließlich eines stem‑cell‑like Gedächtnispools, der vermutlich langfristige Antworten trägt. In einem anspruchsvollen Neuroblastom‑Modell verbesserten L32P‑modifizierte 28z‑CAR‑T‑Zellen das Überleben gegenüber ihren unbearbeiteten Gegenstücken.
Sicherheit und zukünftiges Potenzial
Ein zentrales Anliegen bei dauerhafter Veränderung der Immun‑Signalgebung ist das Risiko unkontrollierten Wachstums oder sekundärer Tumoren. Die Autoren führten daher umfassende Sicherheitsprüfungen durch. E81K‑editierte BBz‑CAR‑T‑Zellen wuchsen nicht abnormal in Kultur, verursachten bei Mäusen keine Organschäden oder entzündliche Krisen und zeigten Monate nach Infusion keine Anzeichen von Lymphom oder Gewebeinvasion. Klinische Datenbanken zeigen ebenfalls keine Anreicherung dieser spezifischen PIK3CD‑Mutationen in T‑Zell‑Leukämien. Insgesamt demonstriert die Arbeit, dass sorgfältig ausgewählte Einzelbuchstaben‑Genomeditierungen als präzise Einstellräder für T‑Zell‑Verhalten dienen können — sie erhöhen Anti‑Tumor‑Kraft und Persistenz und berücksichtigen dabei die jeweilige CAR‑Biologie. Der ROADSTAR‑Ansatz könnte helfen, die nächste Generation von CAR‑T‑Therapien zu entwickeln, die sowohl wirksamer als auch verlässlicher bei Blutkrebserkrankungen und möglicherweise auch soliden Tumoren sind.
Zitation: Bucher, P., Brückner, N., Kortendieck, J. et al. CAR-adapted PIK3CD base editing enhances T cell anti-tumor potency. Nat Cancer 7, 368–383 (2026). https://doi.org/10.1038/s43018-025-01099-7
Schlüsselwörter: CAR-T-Zellen, PI3K-Signalgebung, Basenbearbeitung, Krebsimmuntherapie, T‑Zell‑Stoffwechsel