Clear Sky Science · de
De novo H3.3K27M-verändertes diffuses Mittellinien-Gliom in humanen Hirnstamm-Organoiden zur Entschlüsselung der GD2-CAR-T-Zell-Funktion
Warum diese Studie zu kindlichen Hirntumoren wichtig ist
Diffuses Mittellinien-Gliom ist einer der tödlichsten kindlichen Hirntumoren: Er trifft sehr junge Kinder im Hirnstamm und lässt Familien kaum wirksame Behandlungsoptionen. Da die Tumoren tief im Gehirn liegen und selten operativ entfernt werden, steht Forschenden nur wenig Gewebe zur Verfügung und es gibt wenige sichere Möglichkeiten, neue Therapien zu testen. Diese Studie konstruiert ein realistisches „Mini‑Hirnstamm‑Modell in der Schale“ und nutzt es, um über Wochen zu beobachten, wie eine vielversprechende Immuntherapie — GD2-CAR-T-Zellen — reagiert und warum sie manchmal versagt.
Ein Mini‑Hirnstamm im Labor aufbauen
Das Team begann mit menschlichen Stammzellen und leitete sie schrittweise dazu an, dreidimensionale Hirnorganoide auszubilden, die dem Hirnstamm‑Bereich Pons ähneln, wo diese Tumoren typischerweise entstehen. Durch das präzise Timing von Wachstums‑Signalen erzeugten sie Organoide, die reich an den gleichen Arten von Stützzellen, also Gliazellen, sind, die in diesem Bereich vorkommen. Detaillierte genetische Analysen zeigten, dass die Zelltypen und ihre Reifung Mustern folgten, die in der frühen menschlichen Gehirnentwicklung beobachtet werden, insbesondere den glialen Linien, die für Pons und die benachbarte Medulla typisch sind. Das bedeutet, dass die Organoide als realistischer Hintergrund dienen können, um zu untersuchen, wie dieser Krebs entsteht und wächst.
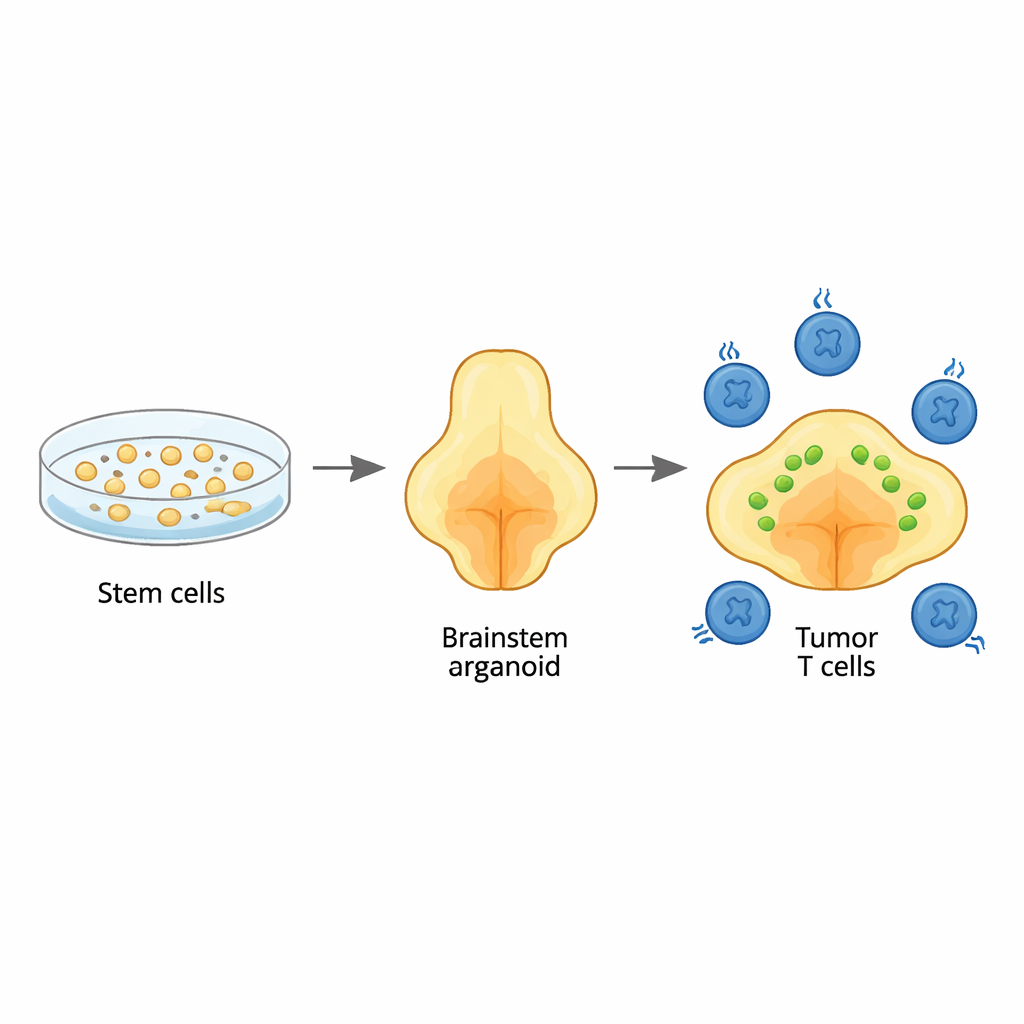
Den kindlichen Tumor im Organoid nachbilden
Um diffuses Mittellinien‑Gliom zu imitieren, führten die Forschenden drei zentrale genetische Veränderungen in junge Organoide ein: eine kennzeichnende Mutation in einem Histonprotein (H3.3K27M), den Verlust des Tumorsuppressors TP53 und eine aktivierende Veränderung im Wachstumsrezeptor PDGFRA. Wurden diese Veränderungen in einem sehr frühen Entwicklungsstadium eingebracht, verwandelten sie ausgewählte gliaähnliche Zellen in Krebszellen. Die entstehenden Tumoren breiteten sich diffus durch die Organoide aus, wie sie auch durch die Hirnstämme von Kindern wachsen, und zeigten dieselben umfassenden DNA‑ und RNA‑Signaturen wie Tumoren von Patientinnen und Patienten. Einzelzellsequenzierungen legten eine Mischung von Krebszell‑Zuständen offen, darunter unreife, pons‑spezifische gliale Zellen, die denen in tatsächlichen pädiatrischen Tumoren entsprechen — ein Beleg dafür, dass das Modell die menschliche Erkrankung getreu nachbildet.
Beobachten, wie Immuntherapien kämpfen — und ermüden — über die Zeit
Mit diesem Tumor‑im‑Hirnstamm‑Modell fügten die Forschenden GD2‑CAR‑T‑Zellen hinzu — patienteneigene T‑Zellen, die so gentechnisch verändert wurden, dass sie ein Molekül namens GD2 auf Tumorzellen erkennen — und verfolgten Tumorgröße und T‑Zell‑Verhalten bis zu einem Monat. Einige Organoide zeigten starke Tumorschrumpfung, andere nur partielle Kontrolle, was die gemischten Ergebnisse klinischer Studien widerspiegelt. Einzelzell‑RNA‑Sequenzierung von mehr als 20.000 CAR‑T‑Zellen, die den Tumoren ausgesetzt waren, offenbarte eine überraschende Vielfalt von T‑Zell‑Zuständen. Einige Zellen waren hochzytotoxische „Vollstrecker“, andere aktiviert, aber nicht vollständig tödlich, und eine eigene Gruppe zeigte Merkmale von Erschöpfung, mit gedämpften krebsbekämpfenden Genen und hoher Expression inhibitorischer „Bremsen“. Die erschöpften Zellen ähnelten stark den ausgebrannten T‑Zellen, die man bei chronischen Infektionen und in menschlichen Tumoren findet, was darauf hinweist, dass das Organoid‑System klinisch relevante T‑Zell‑Erschöpfung abbildet, die durch anhaltenden Kontakt mit dem Krebs getrieben wird.
Kraftvolle, aber kurzlebige T‑Zellen finden
Bei genauerer Betrachtung identifizierten die Forschenden eine Untergruppe von CAR‑T‑Zellen, die durch ein Oberflächenprotein namens NCAM1 gekennzeichnet waren und kurzfristig besonders potente Killer waren. Wurden diese NCAM1‑positiven Zellen isoliert und allein eingesetzt, kontrollierten sie Tumoren anfänglich stärker als ihre NCAM1‑negativen Gegenstücke. Sie mündeten jedoch ebenfalls schneller in Erschöpfung und verringerten sich rascher, was über die Zeit zu einer schwächeren Kontrolle führte. Dieser Kompromiss zwischen unmittelbarer Wirksamkeit und Persistenz erklärt, warum CAR‑T‑Therapien dramatische, aber oft vorübergehende Ansprechraten liefern, und legt nahe, dass die Vorauswahl oder Umgestaltung von T‑Zell‑Subsets die Dauerhaftigkeit der Behandlung optimieren könnte.
Wie hirnansässige Immunzellen die Therapie abschwächen können
Im echten Gehirn sind Tumoren nicht nur von Neuronen und Glia umgeben, sondern auch von Mikroglia, den residenten Immunzellen des Gehirns. Um diese Komplexität abzubilden, fügten die Wissenschaftler mikrogliale Zellen hinzu, die aus Stammzellen abgeleitet wurden. Diese Zellen reiften, nahmen Formen und Genexpressionsmuster an, die für Mikroglia in diffusem Mittellinien‑Gliom charakteristisch sind, und produzierten Moleküle, die mit einer immunsuppressiven Umgebung verbunden sind. Wenn CAR‑T‑Zellen in tumortragende Organoide mit Mikroglia gegeben wurden, verschoben sich die T‑Zellen weiter in Richtung Erschöpfung und niedriger Effektorfunktion, und die Tumorkontrolle verschlechterte sich. Gleichzeitig stiegen entzündliche Faktoren, die mit Nebenwirkungen der Behandlung verknüpft sind, wie IL‑6, was nahelegt, dass das Modell auch dazu beitragen kann, CAR‑T‑assoziierte Toxizitäten zu untersuchen.
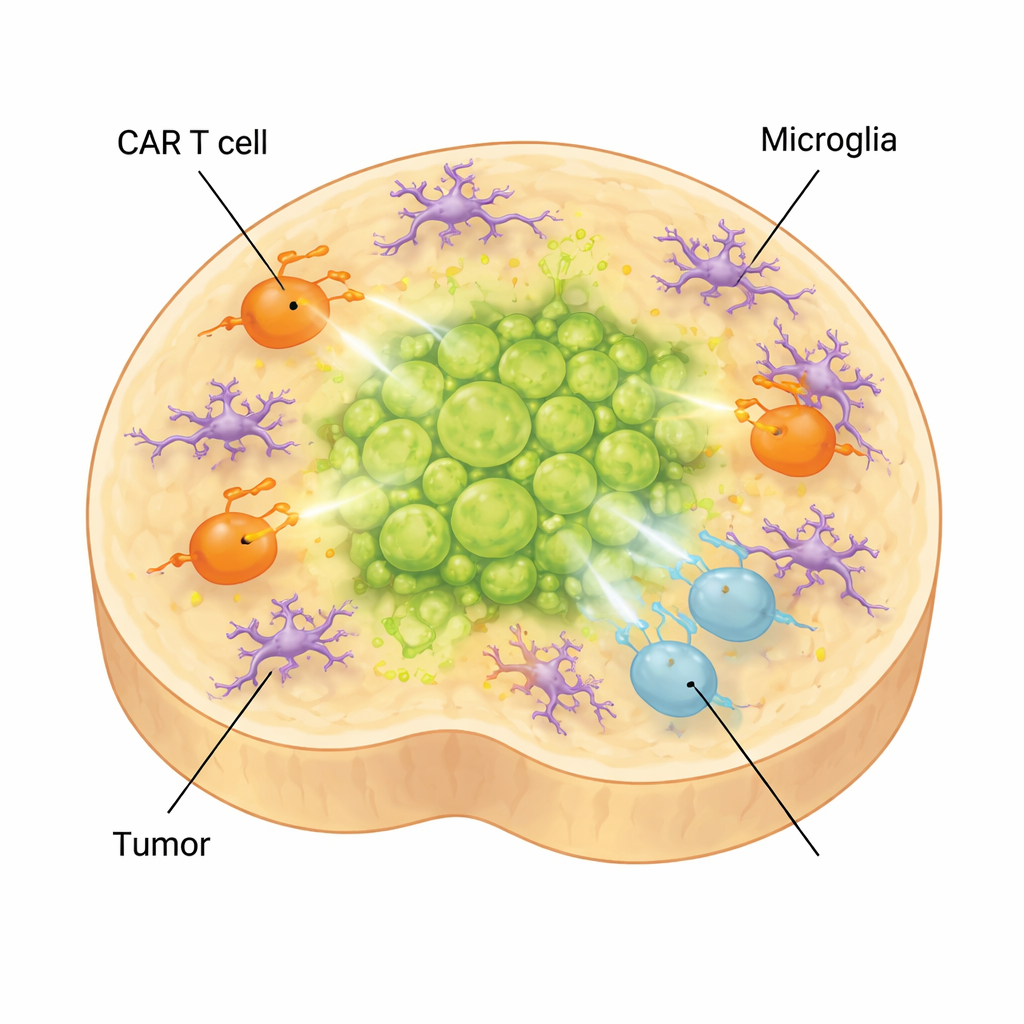
Was das für Kinder mit dieser Erkrankung bedeutet
Für Familien, die mit diffusem Mittellinien‑Gliom konfrontiert sind, bietet diese Arbeit noch keine neue Heilung, aber sie liefert einen kraftvollen Prüfstand, um schneller dorthin zu gelangen. Indem man die Hirnstamm‑Umgebung eines Kindes und den Tumor in einer Schale nachbildet, können Forschende nun in Echtzeit beobachten, wie unterschiedliche Tumorzellen, CAR‑T‑Zelltypen und Mikroglia über Wochen interagieren. So lässt sich identifizieren, welche gentechnisch veränderten T‑Zellen am effektivsten sind, wie und wann sie erschöpfen und wie hirnansässige Immunzellen ihre Wirkung untergraben. Letztlich könnten solche Organoid‑Modelle für einzelne Patientinnen und Patienten personalisiert und verwendet werden, um Immuntherapien vor der Anwendung zu verfeinern — und damit die Chancen zu erhöhen, dass künftige CAR‑T‑Behandlungen für Kinder sowohl sicherer als auch wirksamer sind.
Zitation: Bessler, N., Wezenaar, A.K.L., Ariese, H.C.R. et al. De novo H3.3K27M-altered diffuse midline glioma in human brainstem organoids to dissect GD2 CAR T cell function. Nat Cancer 7, 316–333 (2026). https://doi.org/10.1038/s43018-025-01084-0
Schlüsselwörter: diffuses Mittellinien-Gliom, Hirnorganoide, CAR-T-Zellen, pädiatrischer Hirntumor, Mikroglia