Clear Sky Science · de
Vorhersage und Interpretation zelltypspezifischer Arzneimittelreaktionen im Small-Data-Regime mithilfe induktiver Prioren
Warum diese Forschung für zukünftige Arzneimittel wichtig ist
Wenn ein neues Medikament getestet wird, gehört zu den größten Unbekannten, wie unterschiedlich es die vielen verschiedenen Zelltypen in unserem Körper beeinflussen wird. Eine Verbindung, die einem Zelltyp nützt, kann in einem anderen kaum wirken oder sogar schaden. Solche Informationen experimentell für Tausende von Wirkstoffen und unzählige Zelltypen zu erzeugen, wäre viel zu langsam und teuer. Diese Arbeit stellt einen computerbasierten Ansatz vor, genannt PrePR-CT, der lernt, vorherzusagen, wie einzelne Zelltypen auf Medikamente reagieren, selbst wenn nur begrenzte Daten vorliegen. Die Studie weist auf schnellere, kostengünstigere und präzisere Wege hin, potenzielle Wirkstoffe in silico zu untersuchen, bevor man sich auf teure Labor- und klinische Studien einlässt.
Blick ins Zellinnere statt nur auf die Medikamente
Traditionelle Wirkstoffscreens behandeln Zellen oft so, als seien sie alle gleich, und konzentrieren sich hauptsächlich auf gemittelte Werte. In Wirklichkeit können Immunzellen, Leberzellen und Krebszellen sehr unterschiedlich auf denselben Wirkstoff reagieren. Die Autoren argumentieren, dass ein Modell, um diese Unterschiede vorherzusagen, die interne Vernetzung jedes Zelltyps verstehen muss: welche Gene tendenziell gemeinsam aktiv sind und wie diese Muster die Identität der Zelle definieren. Sie erstellen zelltypspezifische "Karten", indem sie untersuchen, welche Gene in ungestörten (Kontroll-)Zellen gemeinsam an- und abschwellen. Jede Karte wird als Netzwerk dargestellt, in dem Knoten Gene repräsentieren und Kanten starke Koaktivität widerspiegeln. Diese Netzwerke dienen als Vorwissen darüber, wie ein bestimmter Zelltyp organisiert ist, bevor ein Medikament hinzugefügt wird.
Ein netzwerkbewusster Lernmechanismus
PrePR-CT kombiniert drei Zutaten: das Genaktivitätsnetzwerk eines Zelltyps, die Baseline-Genexpression dieses Zelltyps und eine kompakte Beschreibung der chemischen Struktur des Wirkstoffs. Das Modell verwendet eine Klasse von neuronalen Netzen, die für Graphen entwickelt wurden, um das Gen-Netzwerk der Zelle zu verarbeiten und eine Zusammenfassung zu extrahieren, die ihre charakteristischen Muster einfängt. Gleichzeitig wird jedes Medikament in einen numerischen Fingerabdruck überführt, der aus seiner Molekülstruktur abgeleitet wird. Diese Bausteine werden in ein nachgeschaltetes Vorhersagemodul eingespeist, das aus verfügbaren Experimenten lernt, wie ein bestimmter Wirkstoff die Verteilung der Genaktivität in diesem Zelltyp verschieben wird. Anstatt eine einzelne Zahl pro Gen zu liefern, schätzt die Methode sowohl die mittlere Veränderung als auch die Variabilität der Reaktion über einzelne Zellen hinweg, was entscheidend ist, um sowohl subtile als auch starke Effekte zu verstehen.
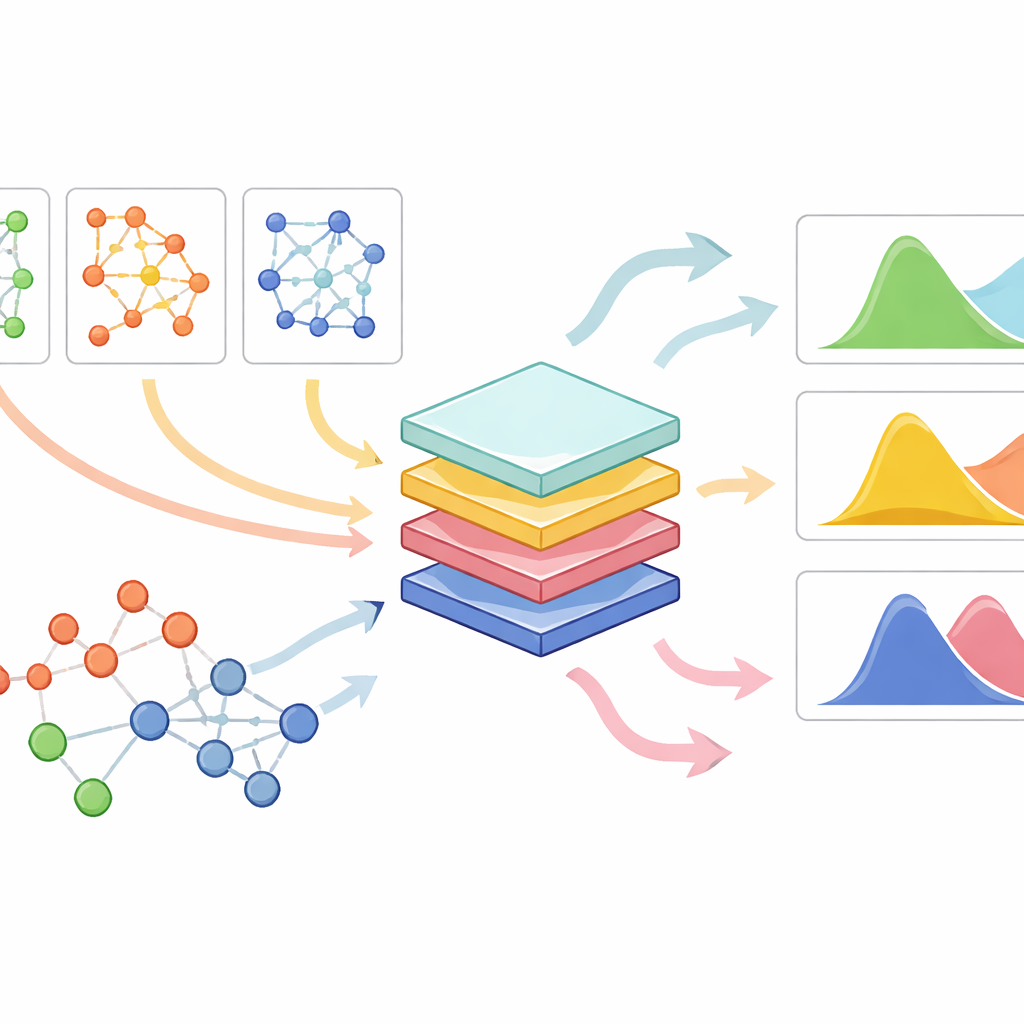
Arbeiten über viele Zelltypen, Wirkstoffe und kleine Datensätze hinweg
Die Forschenden testeten PrePR-CT an einer breiten Sammlung von Datensätzen, darunter humane Blutzellen, die Immunreizen ausgesetzt waren, mehrere Krebszelllinien, die mit verschiedenen Verbindungen behandelt wurden, Maus-Leberzellen, die einem Schadstoff ausgesetzt waren, und großangelegte Wirkstoffscreens aus öffentlichen Ressourcen. In herausfordernden Szenarien, in denen während des Trainings ein ganzer Zelltyp zurückgehalten wurde, konnte das Modell dennoch vorhersagen, wie dieser neue Zelltyp auf ein bekanntes Medikament reagieren würde, oft mit einer Genauigkeit, die frühere generative Modelle übertraf. Ebenso gelang es, wenn ein neues Medikament, aber ein vertrauter Zelltyp zurückgehalten wurde, seine Wirkung allein anhand des chemischen Fingerabdrucks vorherzusagen. Wichtig ist, dass das Modell auch dann wirksam blieb, wenn es auf relativ kleinen Zellzahlen trainiert wurde — einer Situation, in der viele Deep-Learning-Ansätze Probleme haben.
Von der Blackbox zu Hinweisen auf Mechanismen
Über die reine Vorhersage hinaus wollten die Autoren wissen, ob ihr Modell Aufschluss darüber geben kann, welche Gene und Signalwege die Reaktion einer Zelle antreiben. Die graphbasierte Architektur enthält einen Aufmerksamkeitsmechanismus, der Gene hervorhebt, die das Modell in jedem Zelltyp als besonders einflussreich einstuft. Viele dieser "hochaufmerksamen" Gene waren nicht die üblichen Verdächtigen, die durch standardmäßige differentielle Expressionsanalysen identifiziert werden, trotzdem gruppierten sie sich in immunbezogenen Signalwegen, die mit der Biologie der getesteten Wirkstoffe übereinstimmen. Wenn die Forschenden diese einflussreichen Gene in den Modell-Eingaben gezielt störten, sank die Vorhersagequalität, insbesondere für die am stärksten reagierenden Gene, was darauf hindeutet, dass die Aufmerksamkeitswerte auf bedeutsame mechanistische Akteure und nicht auf Rauschen verweisen.
Was das für die Entwicklung besserer Medikamente bedeutet
Einfach gesagt zeigt diese Arbeit, dass es die Fähigkeit künstlicher Intelligenz-Modelle, vorherzusagen, wie Medikamente Zellen umgestalten, deutlich verbessert, wenn man ihnen eine strukturierte Sicht darauf gibt, wie jeder Zelltyp verdrahtet ist — sein internes Gen-Netzwerk — selbst wenn nur begrenzte Daten vorhanden sind. PrePR-CT ersetzt keine Experimente, kann aber helfen einzuschränken, welche Verbindungen und Zelltypen eine nähere Prüfung wert sind, und andeuten, warum bestimmte Zellen so reagieren, wie sie es tun. Mit wachsenden Datensätzen und der Einbeziehung zusätzlicher zellulärer Merkmale könnten solche Ansätze zu wichtigen Werkzeugen werden, um Therapien auf spezifische Gewebe oder Patientenzelltypen zuzuschneiden, Trial-and-Error im Labor zu verringern und präzisere Medikamente näher an die klinische Realität zu bringen.
Zitation: Alsulami, R., Lehmann, R., Khan, S.A. et al. Predicting and interpreting cell-type-specific drug responses in the small-data regime using inductive priors. Nat Mach Intell 8, 461–473 (2026). https://doi.org/10.1038/s42256-026-01202-2
Schlüsselwörter: Vorhersage von Arzneimittelreaktionen, Einzelzell-Transkriptomik, Graph-Neuronale Netze, Arzneimittelentdeckung, Zelltypspezifität