Clear Sky Science · de
Wiederverwendbarkeitsbericht: Bewertung der Leistungsfähigkeit eines Meta-Learning-Foundation-Modells bei der Vorhersage der antibakteriellen Aktivität natürlicher Produkte
Auf der Suche nach neuen Antibiotika — schneller
Die Antibiotikaresistenz nimmt zu, während die Entdeckung neuer Wirkstoffe quälend langsam ist und häufig auf Versuch und Irrtum im Labor beruht. Diese Studie untersucht, ob eine leistungsfähige Art künstlicher Intelligenz, die ursprünglich an großen Sammlungen von Wirkstoffdaten trainiert wurde, schnell angepasst werden kann, um vorherzusagen, welche pflanzlichen Naturstoffe Bakterien bekämpfen könnten — und das nur mit geringen Mengen neuer experimenteller Daten. Gelingt dies, könnten derartige Werkzeuge Forschende dabei unterstützen, die knappe Laborzeit auf die vielversprechendsten Kandidaten zu konzentrieren und die Suche nach der nächsten Antibiotikageneration zu beschleunigen.
Warum Pflanzenstoffe wichtig sind
Viele unserer besten Antibiotika stammen ursprünglich aus natürlichen Produkten von Pflanzen und Mikroorganismen. Diese Moleküle können das Bakterienwachstum stoppen, doch neue Verbindungen in der Natur zu finden ist wie die Suche nach einer Nadel im Heuhaufen. Forschende müssen zahlreiche Verbindungen gegen viele Bakterienstämme testen, und jede Messung ist teuer. Schlimmer noch: Große, sorgfältig gekennzeichnete Datensätze — die moderne Deep-Learning-Methoden benötigen, um gut zu funktionieren — sind in diesem Bereich selten. Das macht die Antibiotikaforschung zu einem wichtigen Prüfstein für sogenannte „Foundation Models“: große, universell einsetzbare KI-Systeme, die sich mit nur wenigen neuen Beispielen auf spezifische Aufgaben feinabstimmen lassen.
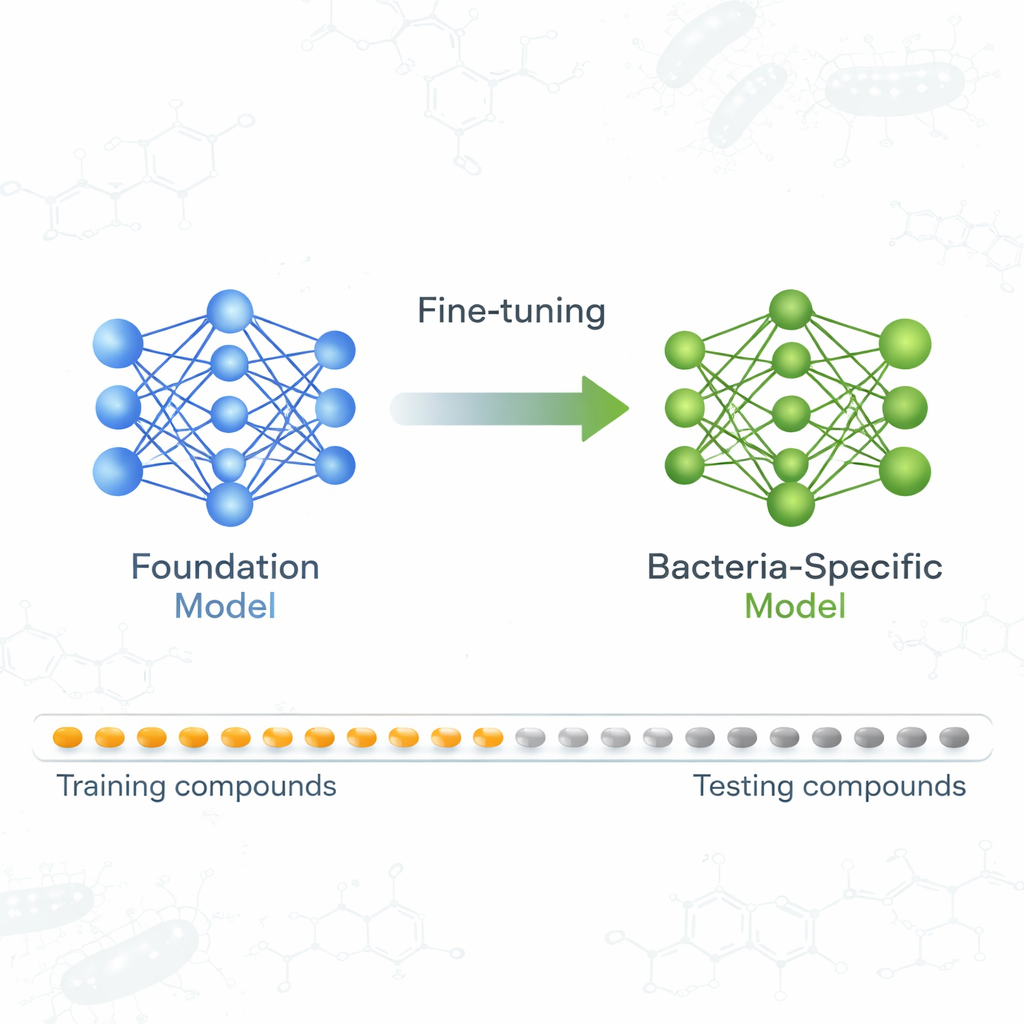
Ein Foundation Model lernt etwas über Keimtöter
Das Team konzentrierte sich auf ein Foundation Model namens ActFound, das ursprünglich darauf trainiert wurde, vorherzusagen, wie stark verschiedene Chemikalien biologische Ziele beeinflussen, unter Verwendung großer Datensätze aus Ressourcen wie ChEMBL und BindingDB. Anstatt für jede Verbindung eine einzelne Zahl vorherzusagen, lernt ActFound, indem es Paare von Verbindungen innerhalb desselben Experiments vergleicht und schätzt, welche aktiver ist. Dieses „paarweise“ Lernen in Kombination mit einer Trainingsstrategie, die als Meta-Learning bekannt ist, soll dem Modell helfen, sich schnell an neue Vorhersageaufgaben anzupassen, wenn nur wenige gelabelte Beispiele verfügbar sind — genau die Situation bei vielen Antibiotikanscreenings.
Test des Modells an realen Pflanzendaten
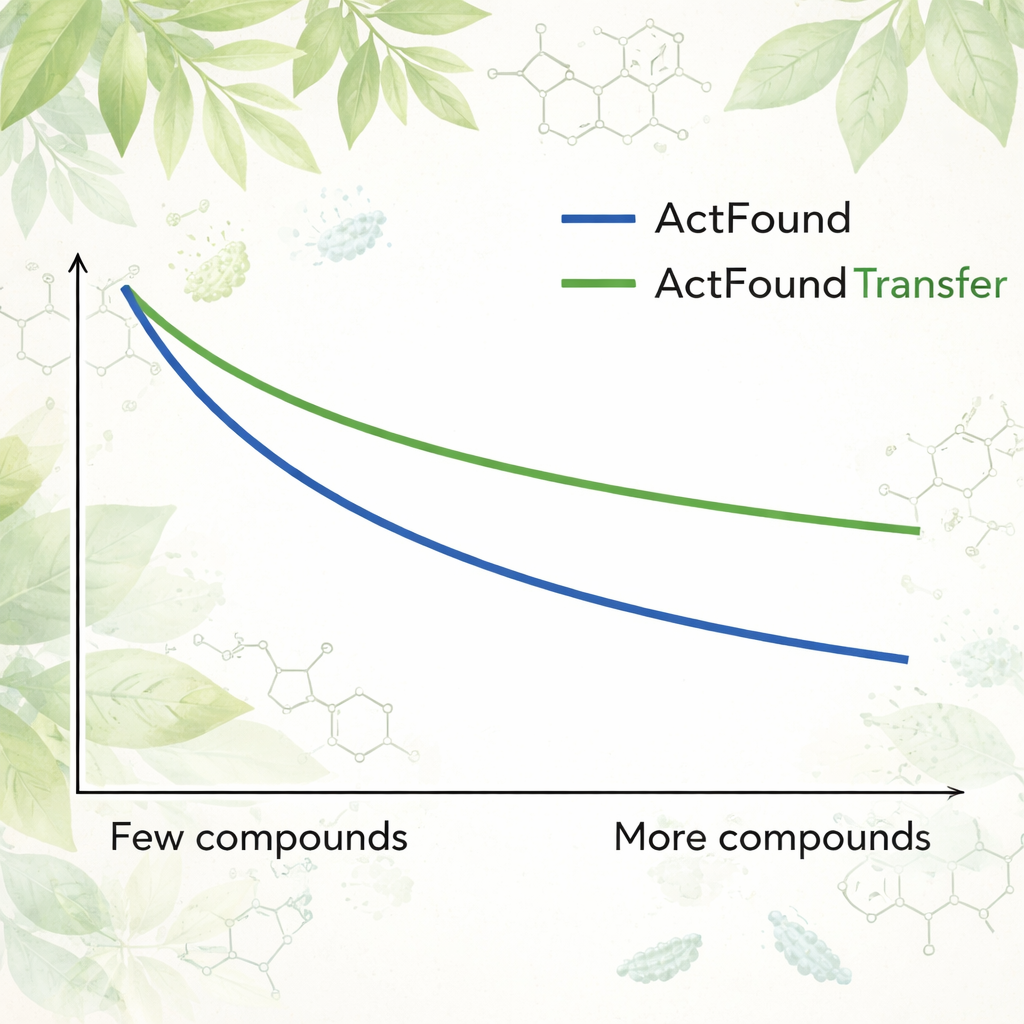
Um die Wiederverwendbarkeit von ActFound zu prüfen, feinabstimmten die Autorinnen und Autoren es an einem kuratierten Datensatz pflanzlicher Naturstoffe, die auf ihre Fähigkeit getestet wurden, das Wachstum verschiedener Bakterien zu hemmen. Jeder Bakterienstamm wurde als eigene Aufgabe behandelt, und das Modell wurde mit nur 8 bis 128 Verbindungen pro Stamm oder festen Prozentsätzen der verfügbaren Daten angepasst. Außerdem verglichen sie ActFound mit einfacheren Meta-Learning- und Transfer-Learning-Modellen, die keine paarweisen Vergleiche verwenden. Über diese Tests hinweg erreichte ActFound nicht die Genauigkeit, die es in früheren Arbeiten an anderen Arten von Wirkstoffdaten gezeigt hatte. Doch bei sehr geringen Datenmengen — ungefähr nur eine Handvoll Verbindungen pro Stamm — lieferten ActFound und seine Transfer-Learning-Variante meist gleichwertige oder bessere Ergebnisse als alternative Methoden.
Wenn Ähnlichkeit hilft — und wann sie schadet
ActFound geht davon aus, dass sich ähnliche Moleküle ähnlich verhalten, was gut funktioniert, wenn Datensätze um Gruppen verwandter Chemikalien herum aufgebaut sind. Der Naturstoffdatensatz jedoch war chemisch vielfältig und wies oft keine eng verwandten „Familien“ von Verbindungen auf. Diese Vielfalt, so wertvoll sie wissenschaftlich ist, untergrub die paarweise Lernstrategie: Wenn Verbindungen innerhalb eines Experiments sehr unterschiedlich sind, hat das Modell Schwierigkeiten, stabile Vergleiche zu erlernen. Die Autorinnen und Autoren stellten außerdem fest, dass eine einfache Diagnostik, die im ursprünglichen ActFound-Paper vorgeschlagen wurde, um im Voraus vorherzusagen, wie gut das Modell bei einer neuen Aufgabe abschneiden würde, für diese Naturstoffdaten nicht standhielt — ein wichtiger Hinweis auf eine Einschränkung beim Übergang in neue chemische Räume.
Was das für die künftige Wirkstoffforschung bedeutet
Für Nichtfachleute lautet die Schlussfolgerung: Foundation Models wie ActFound sind vielversprechende Werkzeuge für die Wirkstoffforschung, wenn Daten knapp sind, aber sie sind keine Allheilmittel. In dieser Studie schnitten ActFound und seine Transfer-Learning-Variante häufig genauso gut oder besser ab als konkurrierende Methoden, wenn nur wenige Pflanzenverbindungen für das Training zur Verfügung standen, doch sie taten sich bei diesem sehr diversen Satz natürlicher Produkte schwer. Die Arbeit legt nahe, dass diese KI-Modelle am nützlichsten sind, wenn die Daten viele chemisch ähnliche Verbindungen enthalten — etwa in fokussierten Studien zu Struktur-Wirkungs-Beziehungen —, während sie weniger zuverlässig bleiben, wenn es darum geht, das Verhalten völlig neuer Molekültypen vorherzusagen. Anders gesagt: KI kann helfen, die Suche einzugrenzen, aber der schwierigste Teil beim Erkunden wirklich neuer chemischer Gebiete liegt weiterhin vor uns.
Zitation: Butt, C.M., Walker, A.S. Reusability Report: Evaluating the performance of a meta-learning foundation model on predicting the antibacterial activity of natural products. Nat Mach Intell 8, 270–275 (2026). https://doi.org/10.1038/s42256-026-01187-y
Schlüsselwörter: Antibiotika-Entdeckung, natürliche Produkte, Deep Learning, Meta-Learning, Wirkstoffscreening