Clear Sky Science · de
Die Phosphorylierung von PLIN5 orchestriert die Kopplung von Mitochondrien und Lipidtröpfchen zur Steuerung des hepatischen Fettflusses und der Steatose
Warum Leberfett wichtig ist
Viele Menschen haben zusätzliches Fett in der Leber, ohne sich krank zu fühlen, doch diese stille Anreicherung kann schließlich zu Entzündungen, Vernarbung und sogar Krebs führen. Diese Studie stellt eine einfache, aber entscheidende Frage: Wenn Wellen von Fett während des Fastens oder durch eine gehaltvolle „westliche“ Ernährung in der Leber eintreffen, wie entscheiden Leberzellen, ob dieses Fett zur Energie verbrannt oder sicher gespeichert wird, und wann beginnt dieses Sicherheitsprogramm zu versagen?
Kleine Kraftwerke und winzige Fettbläschen
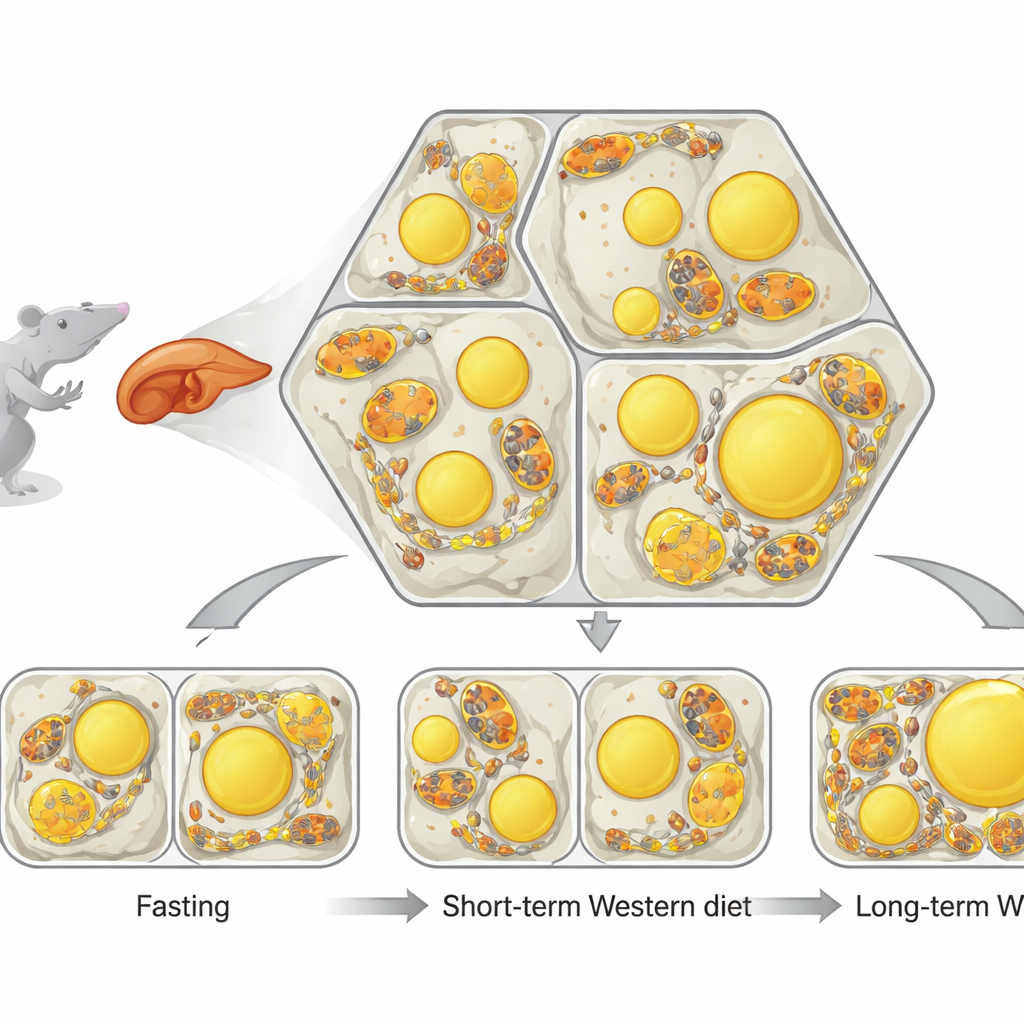
Die Leber ist in sich wiederholende, sechseckähnliche Einheiten organisiert, in denen Blut von einer Seite zur anderen fließt. Entlang dieses Weges spezialisieren sich Leberzellen: Einige verbrennen hauptsächlich Fett zur Energiegewinnung, während andere vorwiegend Fett herstellen und speichern. Innerhalb jeder Zelle sind zwei Strukturen entscheidend. Mitochondrien sind die Kraftwerke der Zelle, und Lipidtröpfchen sind kleine, mit Fett gefüllte Bläschen zur Speicherung. Die Forscher entwickelten eine leistungsstarke Bildgebungs- und Analyse-Pipeline, genannt single-cell phenotypic profiling (scPhenomics), um Größe, Form und Anordnung dieser Strukturen in Tausenden von Zellen direkt in Gewebeschnitten zu kartieren. Sie fanden heraus, dass selbst bei gesunden Tieren die Form der Mitochondrien und der Gehalt an Lipidtröpfchen ausgeprägte räumliche Muster bilden, die widerspiegeln, wo in der Leber normalerweise Verbrennung gegenüber Speicherung stattfindet.
Fasten versus gehaltvolle Ernährung
Als Nächstes untersuchte das Team, was passiert, wenn die Leber plötzlich von Fett überschwemmt wird. Fasten treibt Fett aus den Fettdepots des Körpers in die Leber, während eine kurzzeitige westliche Kost zusätzliches Fett direkt aus der Nahrung zuführt. Bei gefasteten Mäusen nahmen Lipidtröpfchen in der gesamten Leber zu, und Mitochondrien wurden länger und wickelten sich oft eng um diese Fettbläschen, wodurch zahlreiche Kontaktstellen entstanden. Bei Mäusen, die mehrere Wochen lang eine westliche Diät erhielten, füllte sich die Leber ebenfalls mit Fett, doch die Tröpfchen waren anders angeordnet und die Mitochondrien blieben größtenteils getrennt und rundlicher. Dies zeigte, dass die Art und Weise, wie Fett ankommt — durch Fasten oder chronische gehaltvolle Ernährung — sehr unterschiedliche strukturelle Reaktionen innerhalb der Leberzellen auslöst, selbst wenn der Gesamtfettgehalt ähnlich erscheint.
Ein molekularer Schalter für den Umgang mit Fett
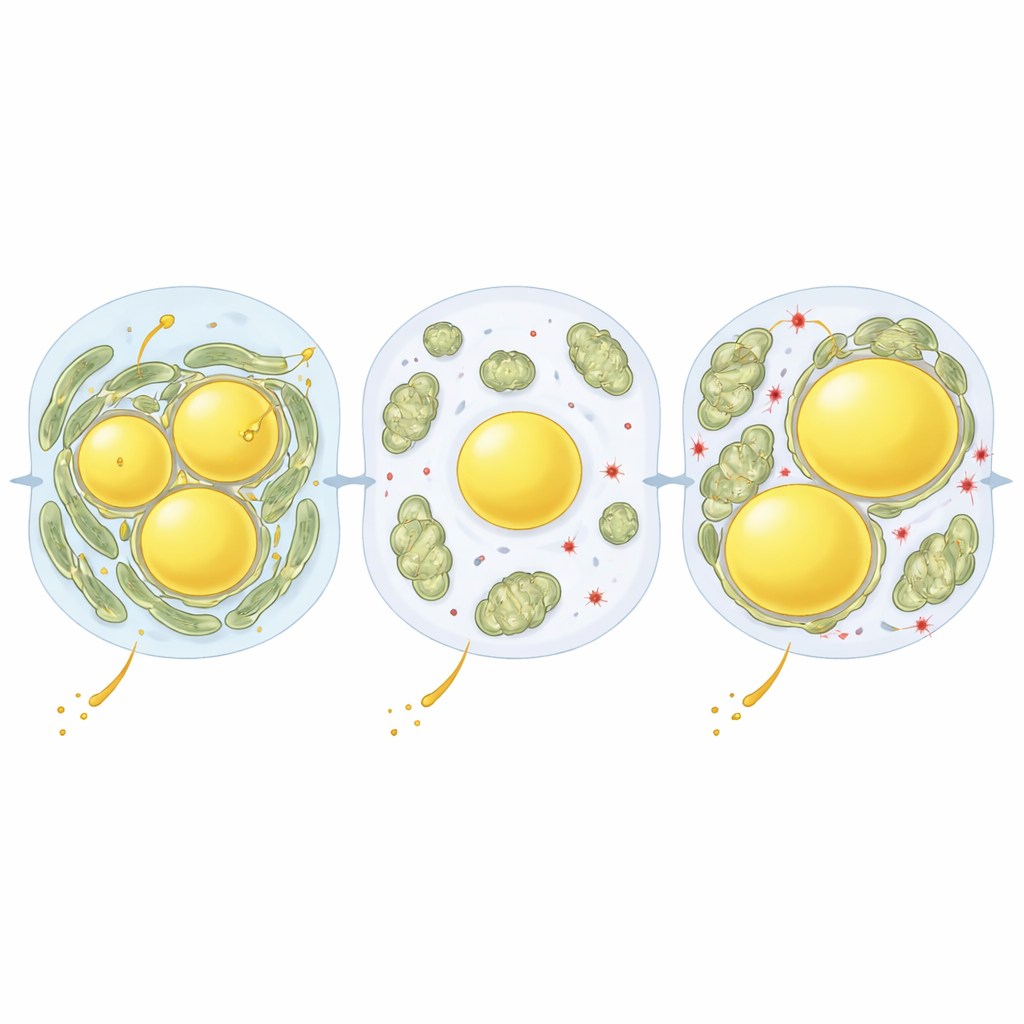
Um zu klären, was diese Organellekontakte steuert, kombinierten die Autoren ihre Bildgebung mit Proteinmessungen in Leberzellen aus verschiedenen Zonen und Ernährungsbedingungen. Ein auffälliges Protein war Perilipin‑5 (PLIN5), das Lipidtröpfchen umhüllt und Mitochondrien an sie binden kann. Fasten erhöhte die PLIN5-Spiegel und platzierte es direkt an der Schnittstelle zwischen Mitochondrien und Tröpfchen. Die Forscher nutzten dann ein leberspezifisches Virus, um PLIN5-Spiegel anzuheben und Versionen des Proteins zu testen, die unterschiedliche Ein-/Ausschaltzustände eines einzelnen chemischen Tags, der Phosphorylierung, nachahmten. Eine Version, die nicht phosphoryliert werden konnte (S155A), verstärkte stark die Kontakte zwischen Mitochondrien und Tröpfchen und vergrößerte Fetttröpfchen, selbst bei normaler Ernährung. Eine Version, die ständige Phosphorylierung imitierte (S155E), bewirkte das Gegenteil: Mitochondrien berührten Tröpfchen selten, die Tröpfchen blieben weniger und kleiner.
Zellen vor fettbedingtem Schaden schützen
Das Team untersuchte dann, was das für die Lebergesundheit unter einer westlichen Diät bedeutete. Als Mäuse mehrere Wochen diese Diät erhielten, förderte die nicht phosphorylierbare PLIN5-Variante (S155A) mehr Fett in Tröpfchen und erhöhte den Triglyzeridgehalt der Leber, doch die Marker für schädlichen oxidativen Stress waren tatsächlich niedriger. Im Gegensatz dazu hinterließ die Phospho-Mimik-Version (S155E) mehr freies Fett und Anzeichen einer stärker oxidierenden, potenziell schädlichen Umgebung mit geringeren antioxidativen Reserven. Effektiv wirkten enge Partnerschaften zwischen Mitochondrien und Lipidtröpfchen wie ein Sicherheitsventil, das überschüssige Fettsäuren in neutrale Speicherkanäle lenkte und die chemischen Kettenreaktionen begrenzte, die Membranen und Proteine schädigen. Bei längerer Fütterung mit westlicher Diät nahmen die Kontakte zwischen Mitochondrien und Tröpfchen jedoch wieder zu und standen in Zusammenhang mit stärkerer Fettbeladung sowohl in Mäusen als auch in menschlichen Lebergewebeproben, was darauf hindeutet, dass dieselbe schützende Vernetzung überlastet werden und zur Krankheitsprogression beitragen kann.
Ein neuer Ansatz für die Fettleberkrankheit
Insgesamt zeigt diese Arbeit, dass Leberzellen aktiv die physischen Beziehungen zwischen ihren Kraftwerken und den Fettdepots umverdrahten, um mit wechselnden Nährstoffbedingungen fertigzuwerden. PLIN5 und insbesondere sein Phosphorylierungszustand an einer einzigen Stelle fungieren wie ein Feinstellrad, das die Kopplung zwischen Mitochondrien und Lipidtröpfchen stärkt oder lockert. Enge Kopplung fördert die Einlagerung potenziell toxischer freier Fette in sicherere Triglyzeridspeicher und hilft, kurzfristige Ernährungsbelastungen wie Fasten oder kurze Exposition gegenüber gehaltvoller Nahrung abzufedern. Wenn dieses adaptive Programm abgeschwächt ist oder wenn eine fettreiche Exposition über Monate oder Jahre anhält, kippt das Gleichgewicht zugunsten von Lipotoxizität und oxidativem Schaden. Indem die Studie diesen strukturellen ‚Schaltkreis‘ innerhalb von Leberzellen offenlegt, legt sie nahe, dass Medikamente, die PLIN5-Aktivität oder Mitochondrien–Tröpfchen-Kontakte modulieren, einen neuen Weg bieten könnten, die Fettlebererkrankung beim Menschen zu verlangsamen oder zu verhindern.
Zitation: Kang, S.W.S., Brown, L.A., Miller, C.B. et al. PLIN5 phosphorylation orchestrates mitochondria lipid-droplet coupling to control hepatic lipid flux and steatosis. Nat Metab 8, 587–603 (2026). https://doi.org/10.1038/s42255-026-01476-1
Schlüsselwörter: fettlebererkrankung, Leberstoffwechsel, Mitochondrien, Lipidtröpfchen, Perilipin 5