Clear Sky Science · de
Fettsäuren fördern entkoppelte Atmung über ATP/ADP-Carrier in weißen Adipozyten
Warum Fettzellen beim Energieverbrennen helfen können
Die meisten Menschen denken bei Körperfett an ein ruhendes Kaloriendepot. Diese Studie zeigt eine überraschend aktive Seite weißer Fettzellen: Unter bestimmten Bedingungen können sie Treibstoff verschwenden und Wärme erzeugen. Indem sie einen neuen Mechanismus offenlegt, durch den Energie in Fettzellen „entweichen“ kann, weist die Arbeit auf frische Ansätze hin, den Kalorienverbrauch des Körpers zu erhöhen und möglicherweise Adipositas zu bekämpfen.
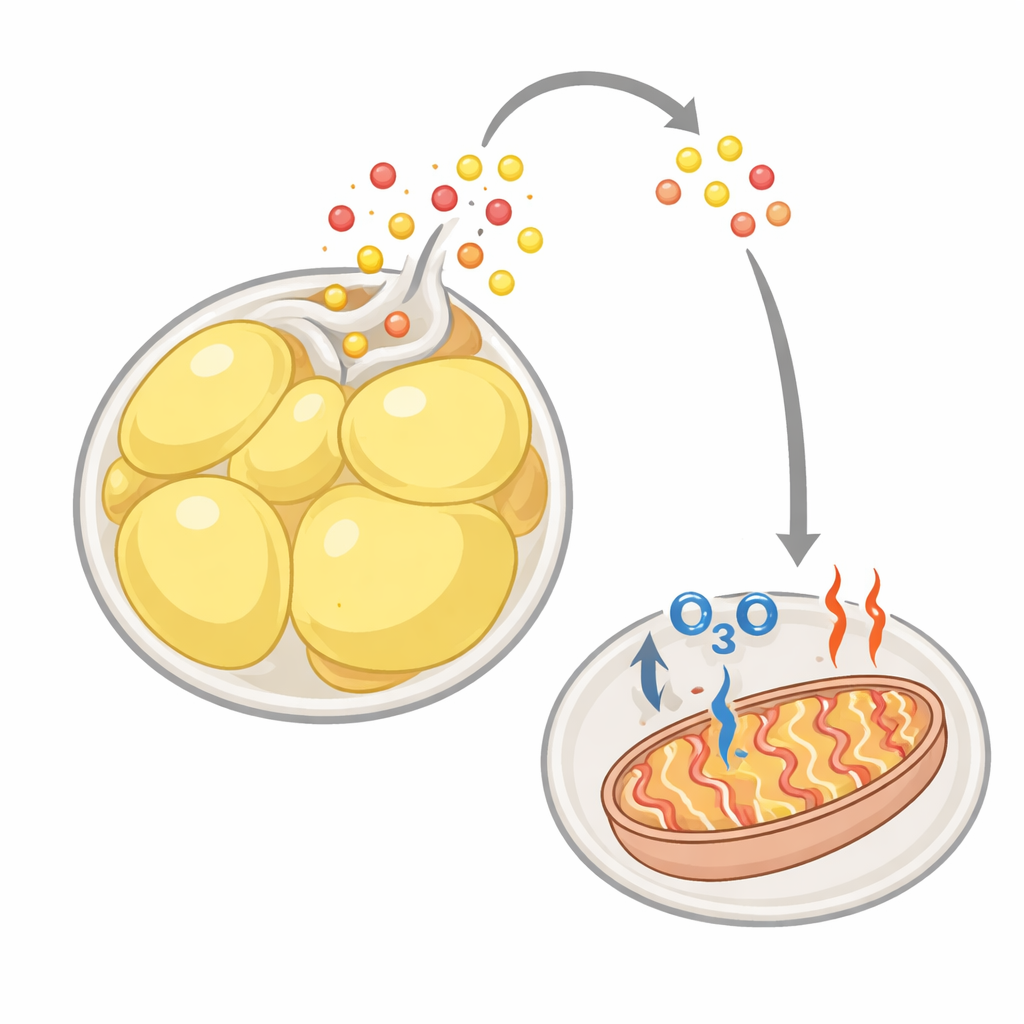
Wenn gespeichertes Fett wieder zu Brennstoff wird
Im Alltag speichern weiße Fettzellen einen Großteil der Zeit Energie als Triglyceride—große Fetttröpfchen. Bei Bewegung, Fasten oder Kälteeinwirkung lösen Stresssignale in diesen Zellen den Abbau von Triglyceriden aus, einen Prozess, der Fettsäuren und Glycerol freisetzt. Die Forschenden bestätigten, dass bei stimuliertem Abbau in im Labor gezüchteten weißen Fettzellen die Zellen ihren Sauerstoffverbrauch deutlich erhöhen, ein Hinweis darauf, dass ihre inneren Kraftwerke, die Mitochondrien, intensiver arbeiten. Die Blockade des ersten Schritts des Fettabbaus stoppte sowohl die Freisetzung von Fettsäuren als auch den Anstieg des Sauerstoffverbrauchs und zeigte damit, dass der Prozess von den Fettsäuren selbst abhängt.
Freie Fettsäuren als Ein-/Ausschalter für Energieverbrennung
Fettsäuren, die die Fettzelle verlassen, treten nicht alle ins Gewebe hinaus; ein Teil verbleibt im Inneren. Das Team zeigte, dass diese verbleibenden freien Fettsäuren entscheidend sind, um die mitochondriale Aktivität hochzufahren. Wenn ein Protein im Kulturmedium verwendet wurde, um Fettsäuren aufzusaugen, schütteten die Zellen insgesamt mehr Fett aus, ihr Sauerstoffverbrauch fiel jedoch — ein Hinweis darauf, dass hohe interne Fettsäurespiegel, nicht nur der allgemeine Fettabbau, die zusätzliche Atmung antreiben. Umgekehrt erhöhte die Blockade der Neubildung von Triglyceriden, eines Wegs, der Fettsäuren normalerweise wieder verpackt, den Sauerstoffverbrauch und verringerte weiter die elektrische Spannung an der mitochondrialen Membran. Zusammengenommen deuten diese Befunde darauf hin, dass freie Fettsäuren die Mitochondrien in einen „leckenden“, energieverschwendenden Zustand treiben.
Ein neuer Akteur in der wärmebildenden Atmung
Im klassischen, wärmebildenden braunen Fett sticht das Protein UCP1 Löcher in die mitochondriale Barriere, sodass die Energie aus der Nahrung als Wärme frei wird statt als nutzbare zelluläre Energie gespeichert zu werden. Weiße Fettzellen haben nur wenig oder gar kein UCP1, daher suchten die Autoren nach einem anderen Weg. Sie konzentrierten sich auf den ATP/ADP-Carrier, ein Transportprotein, das normalerweise die Energiewährung der Zelle über die mitochondriale Barriere austauscht. Mit einem spezifischen chemischen Hemmstoff und genetischen Werkzeugen zur Reduktion dieses Carriers zeigten sie, dass er für den Fettsäure-getriebenen Leak erforderlich ist: Das Blockieren des Carriers bewahrte die mitochondriale Spannung und verhinderte den Anstieg des Sauerstoffverbrauchs während des Fettabbaus, obwohl der Fettabbau selbst normal weiterlief. Das weist darauf hin, dass freie Fettsäuren gemeinsam mit dem Carrier einen kontrollierten Protonenleck über die mitochondriale Barriere erzeugen und so die entkoppelte Atmung einschalten.
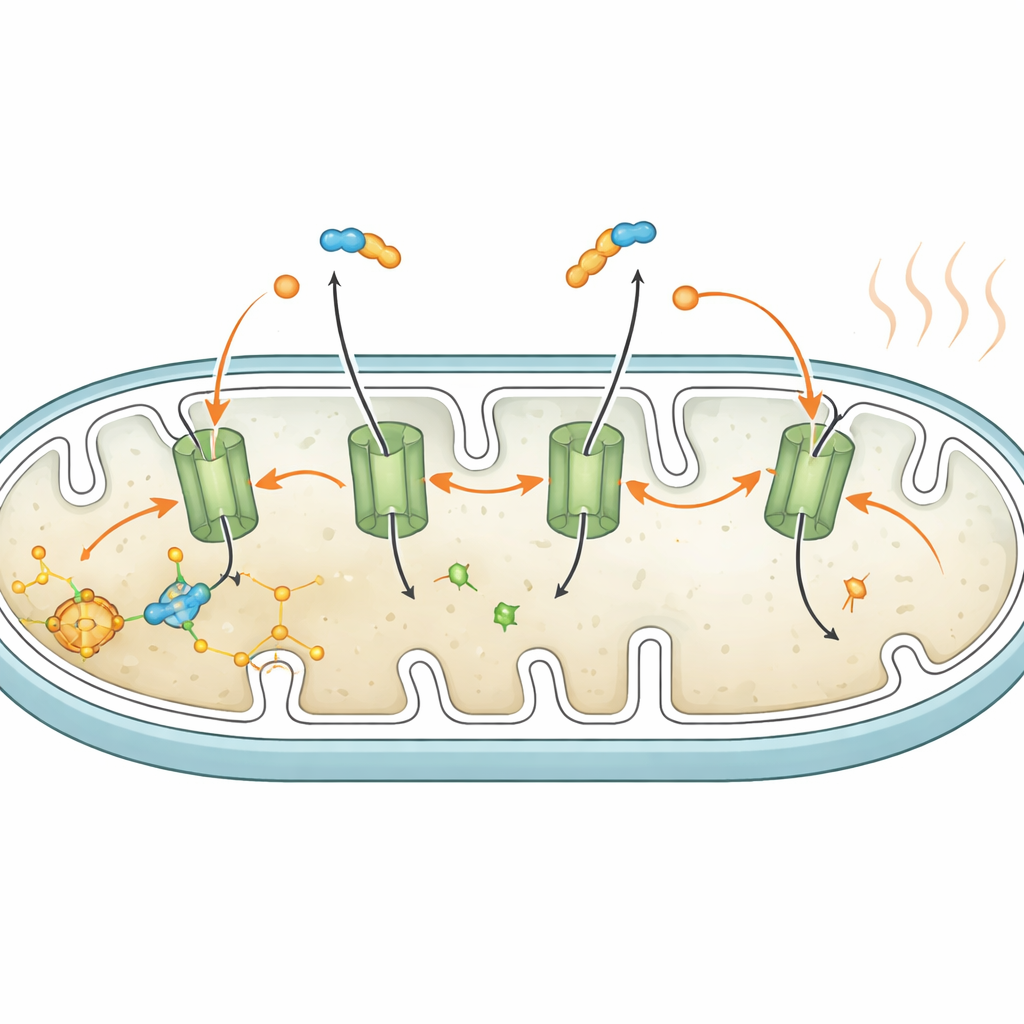
Von der Zellkultur zum lebenden Tier
Um zu prüfen, ob dieses Energieleck im ganzen Tier eine Rolle spielt, verwendeten die Forschenden Mäuse, bei denen ein Signalmolekül namens STAT3 spezifisch in Fettzellen entfernt worden war. Diese Tiere führen den Fettabbau normal durch, zeigen jedoch eine reduzierte Fettsäure-getriebene Atmung in ihrem weißen Fett. Unter üblichen Laborbedingungen, bei denen das braune Fett aktiv ist und den Großteil der Kälteschutzfunktion übernimmt, blieben diese Mäuse warm wie ihre normalen Wurfgeschwister. Wurden die Tiere jedoch fettleibig gemacht und bei einer Temperatur gehalten, bei der braunes Fett weitgehend inaktiv ist, wurden die Mäuse ohne STAT3 im Fett kälteempfindlich und zeigten einen schwächeren Anstieg des gesamten Sauerstoffverbrauchs bei Kälteeinwirkung oder durch Drogen ausgelösten Fettabbau. Wichtig ist, dass ähnliche Veränderungen nicht beobachtet wurden, wenn STAT3 nur im braunen Fett entfernt wurde, was auf eine spezifische Rolle des weißen Fettes hinweist.
Weißes Fett als verborgener Heizkörper
Die Studie kommt zu dem Schluss, dass in weißen Fettzellen freie Fettsäuren, die während aktiven Fettabbaus entstehen, an den ATP/ADP-Carrier in Mitochondrien binden und ein Energieleck auslösen können, das Wärme statt nutzbarer zellulärer Energie erzeugt. In fettleibigen Tieren, die warm gehalten werden, leistet diese entkoppelte Atmung im weißen Fett einen messbaren Beitrag zur Aufrechterhaltung der Körpertemperatur und zum gesamten Energieverbrauch, besonders wenn braunes Fett und Muskelzittern begrenzt sind. Da weißes Fett bei Erwachsenen, insbesondere bei Adipositas, reichlich vorhanden ist, könnte eine behutsame Verstärkung dieses Lecks einen neuen Weg bieten, den täglichen Kalorienverbrauch zu erhöhen und Gewichtsreduktionsstrategien zu unterstützen — vorausgesetzt, dies lässt sich sicher und ohne Schädigung anderer Gewebe durchführen.
Zitation: Ahmadian, M., Aksu, A.M., Dhillon, P. et al. Fatty acids promote uncoupled respiration via ATP/ADP carriers in white adipocytes. Nat Metab 8, 572–586 (2026). https://doi.org/10.1038/s42255-026-01467-2
Schlüsselwörter: weißes Fettgewebe, Fettsäuren, mitochondriale Entkopplung, Thermogenese, Fettleibigkeit