Clear Sky Science · de
Fehlplatzierte Expression von zytosolischem DHODH entkoppelt die de novo-Pyrimidin-Biosynthese von der mitochondrialen Elektronentransportkette
Warum das Durchtrennen einer verborgenen Verbindung in unseren Zellen wichtig ist
Jede Zelle Ihres Körpers muss ständig ihre DNA kopieren und reparieren — ein Vorgang, der eine gleichmäßige Versorgung mit chemischen „Buchstaben“ erfordert, den Pyrimidinen. Bei den meisten Tieren ist die Herstellung dieser Bausteine eng mit der Art und Weise verknüpft, wie Mitochondrien — die Kraftwerke der Zelle — Brennstoff unter Verbrauch von Sauerstoff verstoffwechseln. Diese Kopplung bedeutet, dass bei nachlassender mitochondrialer Atmung die Bausteine für DNA knapp werden und Zellen an Wachstum verlieren. Die hier zusammengefasste Studie zeigt, dass sich durch die Übernahme eines einzelnen Gens aus Bäckerhefe diese beiden Prozesse sauber entkoppeln lassen. Diese genetische Modifikation erlaubt es Säugerzellen, weiterhin Pyrimidine zu produzieren, selbst wenn ihre Mitochondrien beeinträchtigt sind, und eröffnet einen neuen Weg, Krankheiten mit gestörter Energiemetabolik zu untersuchen — und möglicherweise eines Tages zu behandeln.
Ein von der Hefe entliehenes Werkzeug
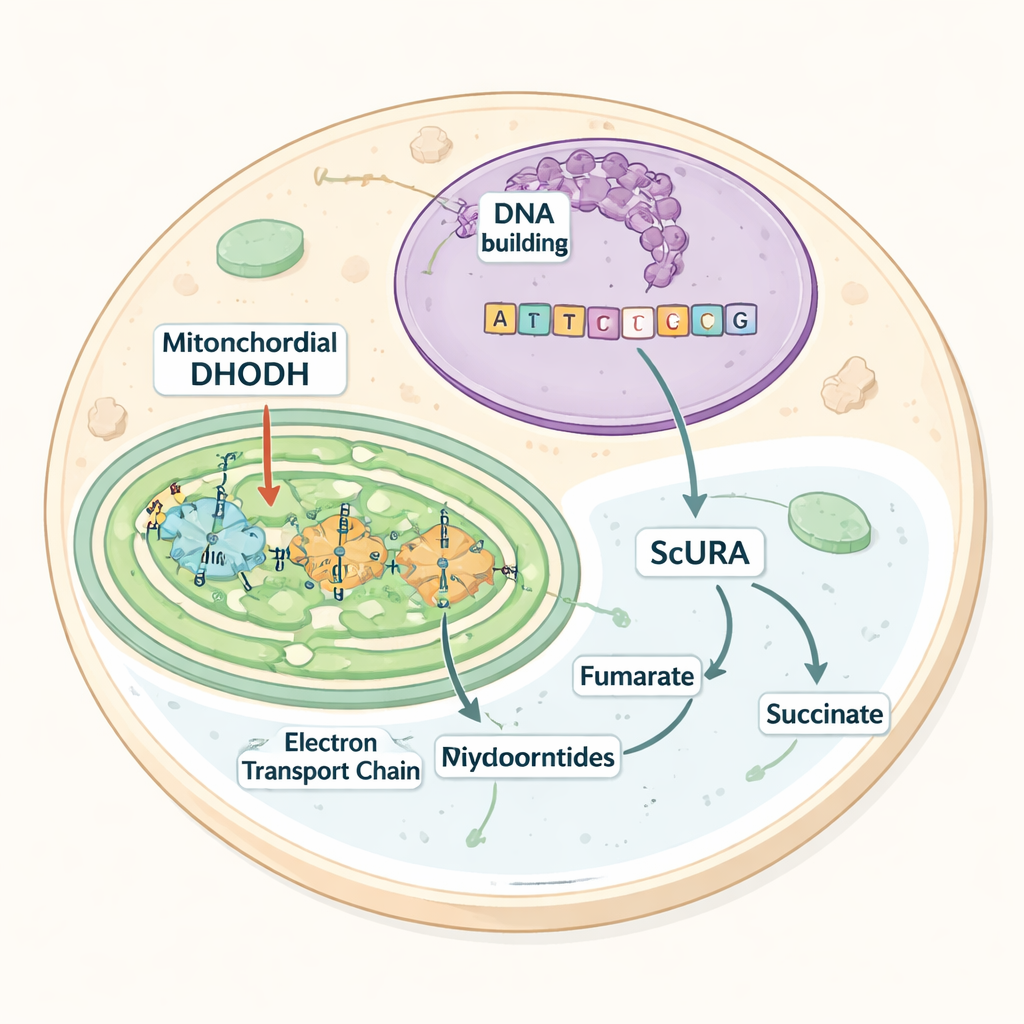
Im Mittelpunkt der Arbeit steht ein Enzym namens Dihydroorotat-Dehydrogenase (DHODH), das einen Schlüsselschritt im Aufbau der Pyrimidine katalysiert. Bei Säugetieren sitzt DHODH in der inneren Mitochondrienmembran und überträgt Elektronen auf ein Trägermolekül, das die Atmungskette speist. Wird dieser Elektronenfluss unterbrochen – etwa durch Wirkstoffinhibitoren oder genetische Defekte – stockt DHODH, die Pyrimidinproduktion bricht zusammen und Zellen werden auf zugeführtes Uridin angewiesen, einen fertiggestellten Baustein. Viele Mikroben, die ohne Sauerstoff gedeihen, umgehen diesen Engpass, indem sie alternative DHODH‑Varianten nutzen, die im Zytosol frei vorliegen und andere Elektronenakzeptoren verwenden. Die Autoren fragten, ob sich eine solche sauerstoffunabhängige Route in Säugerzellen installieren lässt.
Umschaltung, wie DNA‑Buchstaben hergestellt werden
Die Forschenden führten das URA1‑Gen aus der Hefe Saccharomyces cerevisiae in menschliche Zellen ein. URA1 codiert ein zytosolisches Enzym, bezeichnet als ScURA, das denselben chemischen Schritt wie die mitochondriale DHODH ausführt, jedoch Elektronen an Fumarat statt an den mitochondrialen Träger abgibt. Biochemische Tests zeigten, dass ScURA im Zytosol aktive Dimere bildet und eine neue, gegen Medikamente resistente DHODH‑Aktivität hinzufügte. Unter normalen Bedingungen beeinträchtigte die Zugabe von ScURA weder die mitochondriale Struktur noch die Atmung oder das Wachstum, was darauf hinweist, dass es eher als Backup‑Pfad denn als zusätzliche Last fungiert.
Zellen, die mitochondriale Hindernisse abschütteln
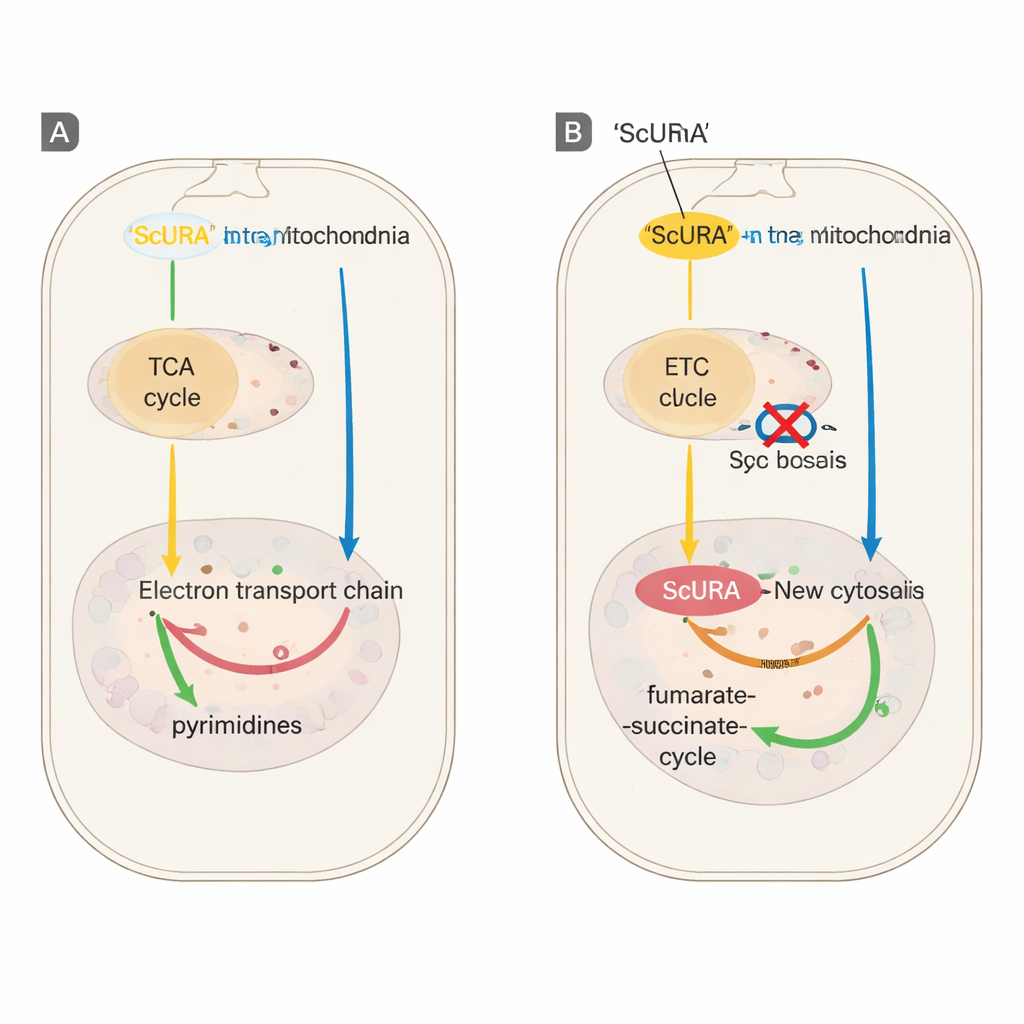
Um zu prüfen, ob dieser Backup‑Mechanismus das native System ersetzen kann, blockierte das Team chemisch entweder DHODH selbst oder die mitochondriale Elektronentransportkette — Behandlungen, die normalerweise die Zellteilung stoppen, sofern nicht Uridin zugeführt wird. Zellen, die ScURA exprimierten, proliferierten weiter ohne Unterstützung, selbst bei starker Hemmung des respiratorischen Komplexes III oder nach genetischer Deletion des endogenen DHODH‑Gens. Detaillierte Nachverfolgung von Stickstoff‑ und Kohlenstoffatomen aus markiertem Glutamin zeigte, dass ScURA‑expressierende Zellen trotz dieser Blockaden weiterhin Pyrimidin‑Nukleotide synthetisierten. Metabolitmessungen ergaben, dass sich ScURA‑Zellen statt in der Anhäufung toxischer Vorstufen an Fumarat banden, Elektronen an dieses weitergaben, Succinat produzierten und den Tricarbonsäure‑Zyklus (TCA) subtil umgestalteten, um einen Fumarat–Succinat‑Shuttle zwischen Zytosol und Mitochondrien zu unterstützen.
Rettung von Zellen mit beschädigten Kraftwerken
Die Autoren testeten ScURA dann in Zellmodellen für mitochondriale Erkrankungen. Zellen ohne mitochondriale DNA oder mit Mutationen, die die respiratorischen Komplexe III oder IV lahmlegen, sind üblicherweise auf zugeführtes Uridin angewiesen, um zu wachsen. Sobald sie so verändert waren, dass sie ScURA exprimierten, konnten diese unterschiedlichen Mutantenzellen ohne Uridin proliferieren, obwohl sie weiterhin Pyruvat benötigten, was auf einen verbleibenden Bedarf an gewisser mitochondrialer Aktivität hinweist. Auf Ebene der Genexpression verhinderte ScURA außerdem das Abschalten von ribosomalen Protein‑Genen, das normalerweise auftritt bei chronischer Hemmung der Elektronentransportkette, indem es die Versorgung mit Pyrimidin‑Bausteinen ausreichend hoch hielt, um die RNA‑Produktion aufrechtzuerhalten.
Was das für Gesundheit und Krankheit bedeutet
Indem ScURA die Pyrimidin‑Synthese sauber von der mitochondrialen Atmung trennt, bietet es Forschenden ein kraftvolles neues Werkzeug: Sie können jetzt in vielen Situationen klären, ob ein bestimmter Defekt oder Wirkstoffeffekt wirklich auf verloren gegangener Energiebereitstellung beruht oder vielmehr auf einem Mangel an DNA‑ und RNA‑Vorstufen. Langfristig könnten ähnliche Strategien bestehende Gentherapien für mitochondriale Erkrankungen ergänzen oder helfen zu erklären, warum manche Tumoren so stark darauf angewiesen sind, ihre mitochondriale Funktion wiederherzustellen. Obwohl die Übertragung eines Hefeenzym‑Konzepts in eine humantherapeutische Anwendung große Vorsicht erfordert, demonstriert diese Studie, dass ein einzelnes, gut gewähltes Gen eine grundlegende metabolische Verbindung umschreiben kann, die die Evolution lange Zeit eng verknüpft hielt.
Zitation: Curtabbi, A., Jaroszewicz, S.N., Sanz-Cortés, R. et al. Ectopic expression of cytosolic DHODH uncouples de novo pyrimidine biosynthesis from mitochondrial electron transport. Nat Metab 8, 454–466 (2026). https://doi.org/10.1038/s42255-026-01454-7
Schlüsselwörter: Pyrimidin-Stoffwechsel, mitochondriale Funktion, Elektronentransportkette, metabolische Umprogrammierung, mitochondriale Erkrankung