Clear Sky Science · de
Entschlüsselung der molekularen Mechanismen, die Typ‑2‑Diabetes in globalen Populationen und krankheitsrelevanten Geweben verursachen
Warum es wichtig ist, die Wurzeln von Diabetes zu verstehen
Typ‑2‑Diabetes betrifft weltweit Hunderte Millionen Menschen, doch wir wissen überraschend wenig darüber, welche molekularen Schalter im Körper die Krankheit tatsächlich verursachen und welche lediglich damit einhergehen. Diese Studie geht tief in unsere DNA und in mehrere Organe, um genau zu bestimmen, welche Gene und Proteine den Blutzucker wirklich in Richtung Diabetes treiben und welche ihn dagegen schützen. Indem die Forschenden Personen aus unterschiedlichen Abstammungen einbezogen und mehrere zentrale Gewebe untersuchten, rückt die Arbeit uns näher an präzisere Präventionsstrategien und Therapien, die für viele Populationen wirksam sind und nicht nur für Menschen europäischer Herkunft.
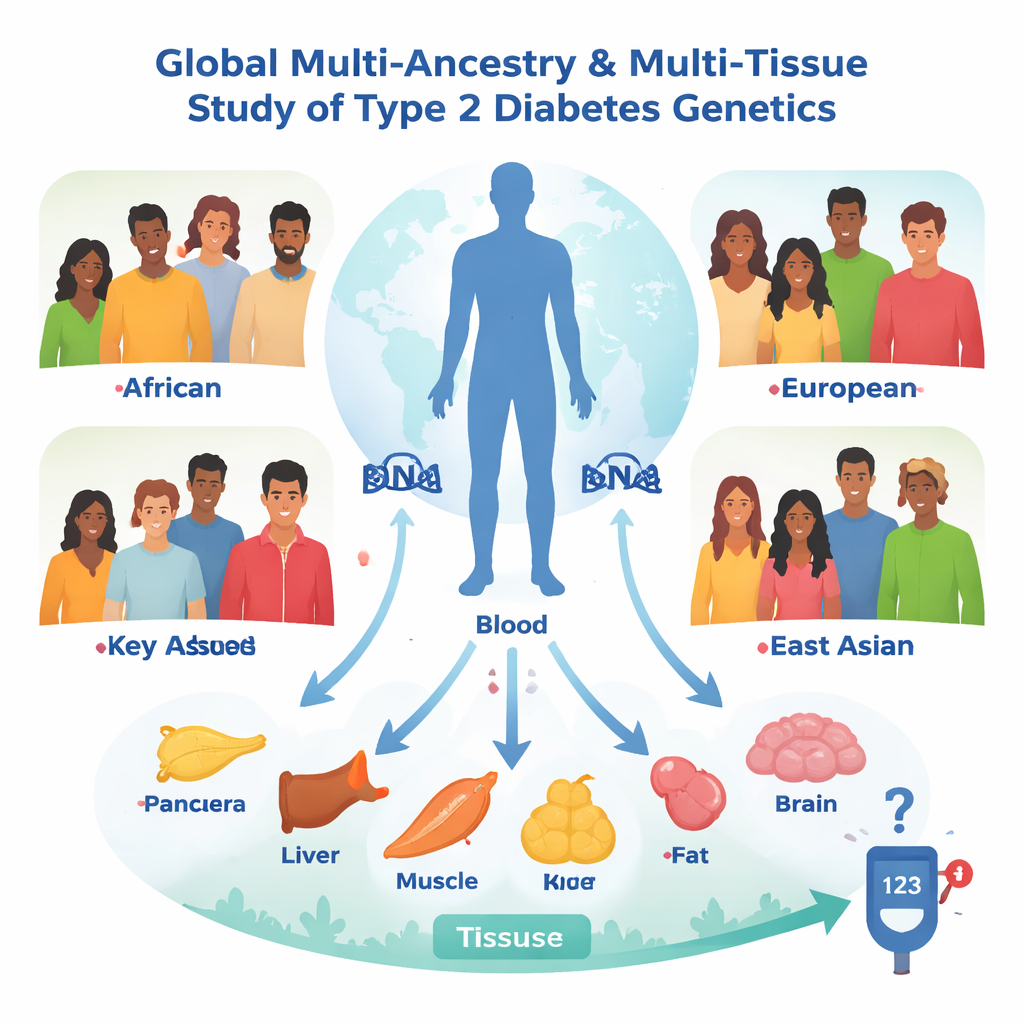
Weitreichende Untersuchungen: global und im Körperinneren
Das Team begann mit genetischen Daten von mehr als 2,5 Millionen Menschen, zusammengetragen von der Type 2 Diabetes Global Genomics Initiative. Statt nur zu fragen, welche DNA‑Varianten mit Diabetes assoziiert sind, stellten sie eine stärkere Frage: Welche Varianten verändern die Aktivität bestimmter Gene oder Proteine im Körper, und führen diese Veränderungen wiederum zu verändertem Diabetesrisiko? Dafür nutzten sie einen statistischen Ansatz namens Mendelsche Randomisierung, der natürliche genetische Unterschiede als eine Art eingebauten randomisierten Versuch behandelt. Sie analysierten über 20.000 Messungen der Genaktivität und mehr als 1.600 Blutproteine in Personen aus vier Abstammungsgruppen – europäischer, afrikanischer, admixed amerikanischer und ostasiatischer Herkunft – und wiederholten die Analysen in sieben Geweben, die zentral für die Blutzuckerregulation sind, darunter die Bauchspeicheldrüse, insulinproduzierende Inselzellen, Leber, Muskel und verschiedene Fettdepots.
Molekulare Hebel, die Risiko erhöhen oder senken
Indem sie diesen genetischen Pfaden folgten, identifizierten die Forschenden 335 Gene und 46 Blutproteine, deren genetisch vorhergesagte Spiegel eine kausale Auswirkung auf das Risiko für Typ‑2‑Diabetes haben, und bestätigten viele dieser Befunde in unabhängigen Kohorten. Einige der gefundenen molekularen Hebel waren bereits bekannte Verdächtige, wie MTNR1B, ein Gen, das an der Insulinfreisetzung aus Pankreas‑Inselzellen beteiligt ist, und BAK1, das den Zelltod in Bauchspeicheldrüse und Fettgewebe beeinflusst. Andere waren neue oder bislang weniger beachtete Akteure, darunter CPXM1, ein Protein, das mit Fettgewebeentwicklung und Insulinresistenz verknüpft ist, und HIBCH, ein Gen, das an der mitochondrialen Funktion beteiligt ist. Insgesamt katalogisierten sie 923 Gene und 46 Proteine mit Hinweisen darauf, dass eine Veränderung ihrer Aktivität in mindestens einem Gewebe die Wahrscheinlichkeit, Diabetes zu entwickeln, verändern kann.
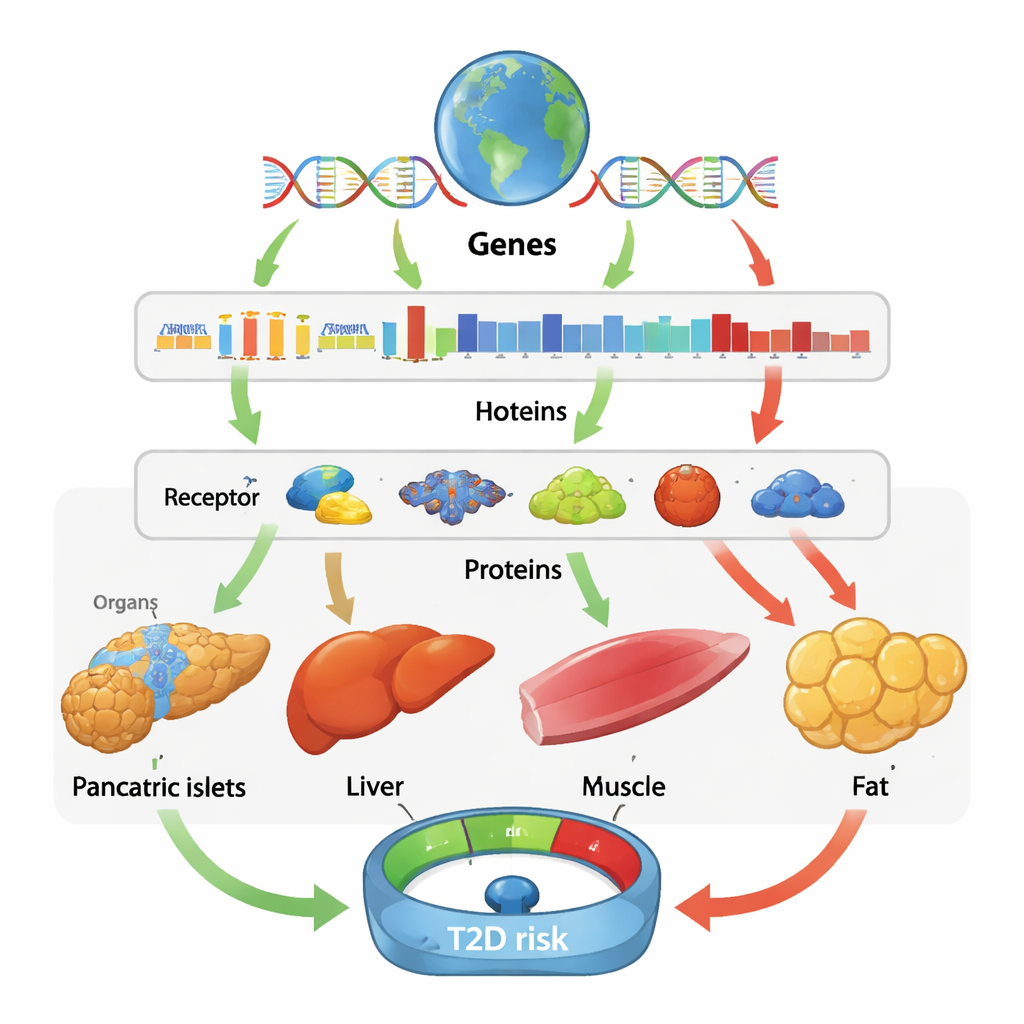
Gleiche Gene, unterschiedliche Geschichten in Geweben und Populationen
Eine auffällige Erkenntnis ist, dass die Wirkung eines Gens oft hochgradig gewebespezifisch ist. Beispielsweise scheint eine erhöhte BAK1‑Aktivität in der Bauchspeicheldrüse und in den Inselzellen das Diabetesrisiko zu steigern, vermutlich indem sie zum Verlust insulinproduzierender Zellen beiträgt, während höhere BAK1‑Spiegel in Fett und Muskel dagegen schützend wirken. HIBCH zeigte ein ähnlich gemischtes Muster: In einigen Geweben senkte erhöhte Aktivität das Risiko, in anderen erhöhte sie es. Diese Befunde zeigen, dass alleinige Blutuntersuchungen wichtige biologische Vorgänge in Organen übersehen können und dass dasselbe Molekül in einem Gewebe nützlich, in einem anderen aber schädlich sein kann. Im Gegensatz dazu zeigten Vergleiche der Ergebnisse über Abstammungen hinweg relativ geringe Unterschiede in den Effektgrößen, was darauf hindeutet, dass viele der zugrundeliegenden kausalen Mechanismen global geteilt werden, auch wenn bestimmte Signale – etwa spezifische schützende oder riskante Proteine in ostasiatischen oder afrikanischen Gruppen – nur dank nicht‑europäischer Daten erkennbar wurden.
Neue Befunde im Kontext bekannter Diabetes‑Biologie
Um zu prüfen, ob ihr Ansatz biologisch sinnvoll ist, verglichen die Autor:innen ihre kausalen Gene mit kuratierten Listen diabetes‑relevanter Gene aus Studien am Menschen und Experimenten an Mäusen. Gene mit der stärksten vorherigen Evidenz für eine Beteiligung an Diabetes zeigten in ihren Analysen deutlich häufiger kausale Effekte als zufällig ausgewählte Gene. Zudem stimmten die Gewebe, in denen diese kausalen Effekte auftraten, mit bekannten Krankheitsmechanismen überein: Gene, die mit Beta‑Zell‑Versagen in Verbindung stehen, waren vor allem in Pankreas‑Inselzellen relevant, während Gene, die mit dem metabolischen Syndrom assoziiert sind, ihre stärksten Effekte im viszeralen (tiefen Bauch‑)Fett zeigten. Diese Übereinstimmung stützt die Idee, dass die statistische Pipeline tatsächlich Mechanismen und nicht nur Korrelationen identifiziert.
Was das für zukünftige Therapie und Prävention bedeutet
Für Nicht‑Spezialisten lautet die zentrale Erkenntnis, dass diese Arbeit lange, anonyme Listen von DNA‑Varianten in eine klarere Karte spezifischer Gene, Proteine und Organe verwandelt, die Typ‑2‑Diabetes tatsächlich antreiben. Indem Ursache und Effekt unterschieden und aufgezeigt wird, wann dasselbe Molekül in verschiedenen Geweben gegensätzliche Rollen spielt, liefert sie Arzneimittelentwicklern präzisere Ziele und warnt davor, wo eine Einheitslösung nach hinten losgehen könnte. Wichtig ist auch, dass durch die bewusste Einbeziehung diverser Populationen die Studie dazu beiträgt, dass zukünftige Medikamente oder Risikovorhersagen, die auf diesen Einsichten basieren, mit höherer Wahrscheinlichkeit breit wirksam sind und nicht nur für Menschen europäischer Abstammung.
Zitation: Bocher, O., Arruda, A.L., Yoshiji, S. et al. Unravelling the molecular mechanisms causal to type 2 diabetes across global populations and disease-relevant tissues. Nat Metab 8, 506–520 (2026). https://doi.org/10.1038/s42255-025-01444-1
Schlüsselwörter: Typ‑2‑Diabetes, genetische Mechanismen, Multi‑Ancestry‑Genomik, gewebespezifische Genexpression, kausale Inferenz