Clear Sky Science · de
Lamin A/C‑regulierter Cystein‑Abbaufluss verändert das Schicksal von Stammzellen durch Epigenom‑Reprogrammierung
Wie das zelluläre Skelett mit dem Stoffwechsel spricht
Warum bleiben manche Zellen jugendlich und flexibel in dem, was sie werden können, während andere altern oder sich in die falsche Identität festlegen? Diese Studie offenbart ein überraschendes Gespräch in unseren Zellen zwischen dem nukleären „Gerüst“, das die DNA formt, und einer schwefelhaltigen Nährstoffverbindung, dem Cystein. Indem gezeigt wird, wie dieser Dialog Stammzellen zu gesunden Schicksalen – oder zu vorzeitiger Alterung – lenkt, legt die Arbeit nahe, dass das, was Zellen „essen“ und wie sie es verarbeiten, eines Tages so angepasst werden könnte, dass bestimmte genetische Krankheiten verhindert und möglicherweise Aspekte des Alterns verlangsamt werden.
Die verborgene Rolle der nukleären Hülle
Tief in jeder Zelle wird die DNA gegen ein Proteinnetz gepresst, die sogenannte nukleäre Lamina, die teilweise aus den Proteinen Lamin A und C aufgebaut ist. Diese Lamins geben dem Kern nicht nur seine Form; sie helfen auch zu entscheiden, welche Gene verschlossen bleiben und welche zugänglich sind. Die Autorinnen und Autoren untersuchten murine embryonale Stammzellen in ihrem flexibelsten, dem „naiven“, Zustand und fanden heraus, dass Lamin A/C normalerweise zwei Stoffwechselenzyme, CBS und CTH, dämpft, die am Aufbau und Abbau von Cystein beteiligt sind. Wenn Lamin A/C vorhanden und aktiv ist, werden diese Enzyme zurückgehalten und die Cysteinverarbeitung bleibt gering, was einen stabilen, jugendlichen Stammzellzustand unterstützt. 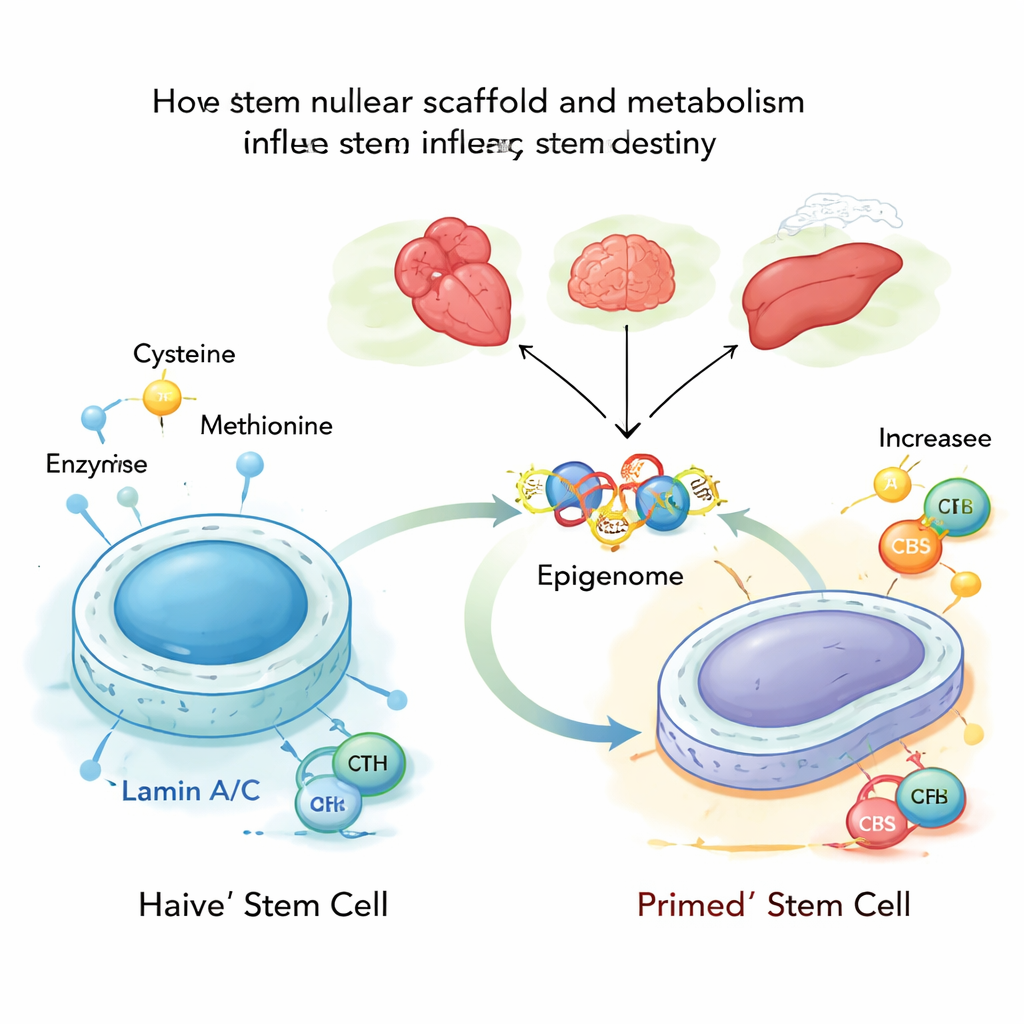
Wenn die Struktur versagt, beschleunigt sich der Stoffwechsel
Im nächsten Schritt entfernten die Forschenden Lamin A/C oder führten eine krankheitsverknüpfte Mutation ein, die eine menschliche vorzeitige Alterungskrankheit namens Hutchinson–Gilford‑Progerie nachahmt. Ohne normales Lamin A/C werden die CBS‑ und CTH‑Gene zugänglicher und stärker von einem Transkriptionsfaktor namens SP1 gebunden, wodurch sie aktiviert werden. Diese Veränderung lenkt mehr Cystein durch einen Stoffwechselweg, der in Acetyl‑CoA mündet – ein kleines Molekül, das Acetylgruppen transportiert, die verwendet werden, um die DNA‑Packung zu lockern. Wenn Cystein vermehrt in Acetyl‑CoA umgelenkt wird, werden Acetylgruppen bevorzugt an bestimmte Stellen auf Histonproteinen angehängt – insbesondere an zwei Positionen des Histons H3, bekannt als K9 und K27 – wodurch benachbarte Gene leichter aktiviert werden können.
Von chemischen Markern zu Entscheidungen über Zellschicksale
Diese Verschiebungen in den Histon‑„Marken“ wirken wie ein globales Umstimmen des Kontrollpults der Zelle. In naiven Stammzellen treibt die Erhöhung von CBS und CTH oder einfach die Zuführung von mehr Cystein die Zellen in einen fortgeschritteneren, „primed“ Zustand, der näher an der Bildung von echten Geweben liegt. Gene, die an der Herzentwicklung und anderen Linien beteiligt sind, werden aktiver, und die dreidimensionale Faltung der DNA ändert sich zugunsten dieser Programme. Umgekehrt hilft das Herunterregeln von CBS und CTH oder das Begrenzen von Cystein, eine naivere, jugendlichere Identität wiederherzustellen, selbst wenn die nukleäre Lamina beschädigt ist. In embryonalen Modellen führte diese metabolische Fehlsteuerung zu einer verzerrten Bildung der drei Keimblätter – den frühen Bausteinen aller Organe – und zu einer abnormalen Bevorzugung von Herzmuskelzellen, sofern CBS und CTH nicht wieder ins Gleichgewicht gebracht wurden. 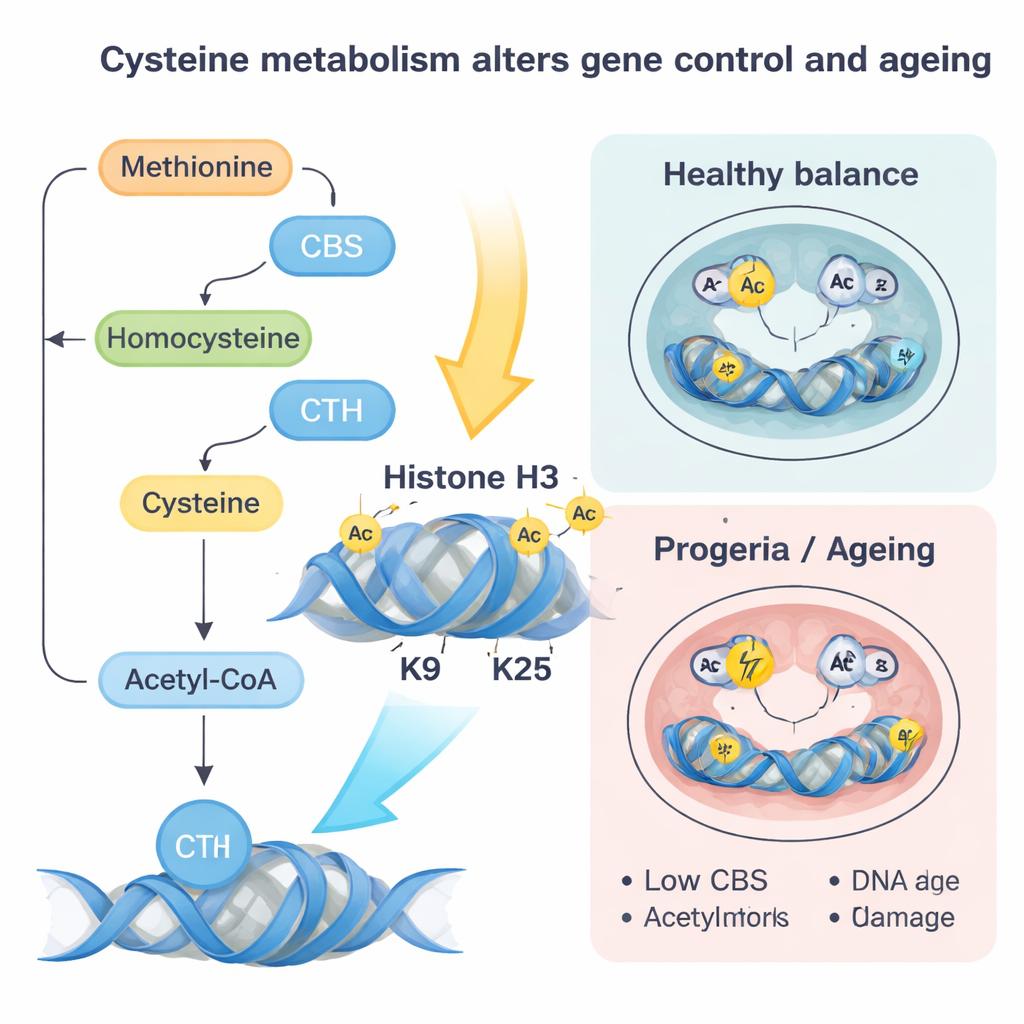
Stoffwechsel, DNA‑Marken und vorzeitige Alterung
Die progerieähnliche Lamin‑Mutation erzählte eine ergänzende Geschichte. Hier fallen CBS‑ und CTH‑Spiegel ab, wodurch der Cysteinfluss und das über diesen Weg erzeugte Acetyl‑CoA reduziert werden. Gleichzeitig wird Homocystein wieder in den Methioninzyklus zurückgeführt, was die SAM‑Spiegel erhöht – SAM ist der universelle Donor von Methylgruppen. Das begünstigt zusätzliche Methylmarken, insbesondere eine Marke namens H3K9me3, die vom Enzym SUV39H1 gesetzt wird, Chromatin verdichtet und mit eingeschränkter DNA‑Reparatur in Verbindung gebracht wird. Die Autorinnen und Autoren zeigten, dass eine behutsame Wiederherstellung von CBS oder die Einschränkung von Methionin SAM senkte, diese repressiven Methylmarken verringerte, die DNA‑Reparatur verbesserte, oxidativen Stress und Seneszenzmarker reduzierte und die Differenzierung von Herzzellen teilweise rettete. Ähnliche Abnahmen von CBS und Anstiege repressiver Marken wurden in normal gealterten Mäuseherzen und in Fibroblasten von älteren Menschen und Progerie‑Patienten beobachtet, was darauf hindeutet, dass dieser Regelkreis auch beim natürlichen Altern wirkt.
Was das für Gesundheit und Altern bedeutet
Für Nicht‑Spezialisten lautet die Botschaft, dass das strukturelle Gerüst der Zelle und ihr Stoffwechsel eng verknüpft sind: Wenn die nukleäre Hülle aus Lamin A/C gestört ist, ändert sich die Verwendung von Cystein, was wiederum die chemischen Markierungen an DNA‑verpackenden Proteinen umschreibt. Diese Markierungen entscheiden, welche Gene eingeschaltet werden, während Stammzellen den Körper aufbauen, und bestimmen mit, wie gut Zellen im Laufe des Lebens Schäden reparieren. Durch gezieltes Einstellen von Enzymen wie CBS und CTH – oder durch Anpassung der Zufuhr von Nährstoffen wie Methionin und Cystein – könnte es möglich sein, einige der Fehlmarkierungen bei lamin‑basierten Erkrankungen zu korrigieren und möglicherweise Aspekte vorzeitigen oder normalen Alterns zu mildern.
Zitation: Wang, Y., Shi, H., Wittig, J. et al. Lamin A/C-regulated cysteine catabolic flux modulates stem cell fate through epigenome reprogramming. Nat Metab 8, 431–453 (2026). https://doi.org/10.1038/s42255-025-01443-2
Schlüsselwörter: Stammzellen, nukleäre Lamina, Cystein‑Stoffwechsel, Epigenetik, Altern