Clear Sky Science · de
Struktur und Polydispersität einzelner Lipidvesikel mittels Kleinwinkel-Röntgenstreuung am European XFEL
Warum winzige Bläschen im Wasser wichtig sind
Lipidvesikel sind mikroskopische Bläschen aus denselben fettartigen Molekülen, aus denen unsere Zellmembranen bestehen. Sie spielen eine Schlüsselrolle bei der Wirkstoffabgabe, in Kosmetika und bei der Art und Weise, wie Zellen Hormone und Neurotransmitter transportieren. Da jedes Vesikel jedoch nur einige zehn Milliardstel Meter groß ist und sich in Wasser befindet, ist es überraschend schwierig, seine feine Struktur sichtbar zu machen. Diese Studie zeigt, wie man einzelne Vesikel nacheinander mit intensiven Röntgenblitzen untersucht und damit nicht nur ihre Durchschnittsstruktur, sondern auch ihre individuellen Unterschiede erfasst – Informationen, die sowohl für die Biologie als auch für die Nanotechnologie entscheidend sind.
Vom Verschwimmen zur Einzelpartikel-Klarheit
Jahrzehntelang haben Wissenschaftler die Methode der Kleinwinkel-Röntgenstreuung genutzt, um weiche Materialien wie Proteine, Nanopartikel und Lipidvesikel in Lösung zu untersuchen. Bei einem typischen Experiment durchdringt ein schmaler Röntgenstrahl eine Probe, die astronomisch viele Kopien des gleichen Partikels enthält. Der Strahl wird gestreut, und das entstehende Muster kodiert Größe und innere Struktur. Der Haken ist, dass diese Methode nur Mittelwerte über Billionen von Partikeln liefert, die in zufälligen Orientierungen und mit leicht unterschiedlichen Größen und Formen vorliegen. Viele der interessanten Details – etwa die Breite der Größenverteilung oder wie sehr einzelne Partikel von einer perfekten Kugel abweichen – gehen dadurch verloren.
Bewegung einfrieren mit ultrakurzen Röntgenpulsen
Um über Durchschnittswerte hinauszukommen, wenden sich die Autoren einem Röntgen-Freie-Elektronen-Laser (XFEL) am European XFEL zu. Dieses Gerät erzeugt ultrakurze, extrem helle Röntgenpulse, die nur wenige Billiardstel Sekunden dauern. In diesem Moment kann ein einzelnes Vesikel untersucht werden, bevor die intensive Strahlung es schädigt – ein Konzept, das als „diffract-before-destroy“ bekannt ist. Das Team verwendet einen Aerosolinjektor, um einzelne Vesikel aus dem Wasser in ein Vakuum zu sprühen, wo die Tröpfchen rasch abkühlen und vitrifizieren, sodass intakte Vesikel in einer dünnen Wasserschicht erhalten bleiben. Ein nanofokussierter Röntgenstrahl, nur wenige hundert Nanometer breit, trifft jeweils ein Vesikel, und ein großflächiger Detektor zeichnet das resultierende Beugungsmuster auf.
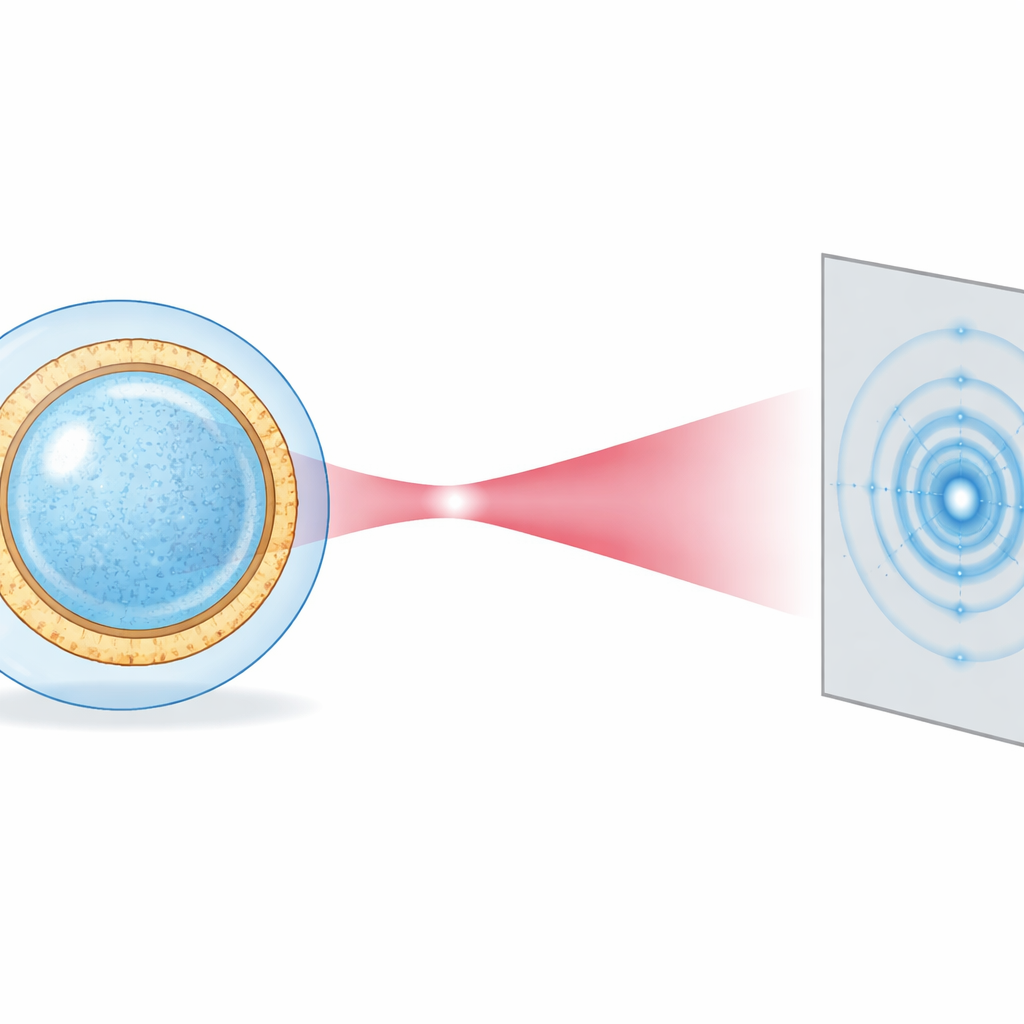
Vom Muster zur Form und Hülle
Jedes Vesikel erzeugt ein schwaches, ringförmiges Muster, das von seinem Radius, seiner Abweichung von einer perfekten Kugel und der detaillierten Schichtung elektronendichter Lipid-Kopfgruppen und diffuserer Fettschwänze in der Membran abhängt. Anstatt zu versuchen, ein vollwertiges Bild Pixel für Pixel zu rekonstruieren – ein Verfahren, das viele identische Kopien benötigt – passen die Forscher jedes Muster direkt mit einem physikalisch motivierten Modell an, das aus der konventionellen Streuung in Lösung entlehnt ist. Das Vesikel wird als leicht abgeplattete Kugel umgeben von einer glatten Wasserschale behandelt, und die Membran wird durch einfache, glockenförmige Dichteprofile beschrieben. Durch azimutales Mittel des Musters (Umwandlung in eine eindimensionale Kurve) und Durchführung von Kleinste-Quadrate-Anpassungen gewinnen sie für jedes Vesikel seinen Radius, seine Elliptizität (wie gestreckt oder abgeflacht es ist) und eine Schätzung des inneren Dichteprofils der Membran.
Die Variabilität der realen Welt abbilden
Da das Experiment mit hoher Wiederholrate läuft, sammelt das Team mehr als eine Million Bilder pro Messlauf. Automatisierte „Hit-Finding“-Routinen wählen jene aus, die tatsächlich ein einzelnes Vesikel enthalten, statt mehrere Partikel oder leere Aufnahmen. Aus Tausenden solcher Treffer erstellen die Forscher Histogramme von Vesikelradius und -form. Sie stellen fest, dass Vesikel, die kugelförmig vorbereitet wurden, während der Aerosolisierung oft leicht abgeflachte Ellipsoide werden, wahrscheinlich weil Wasser langsam aus dem Inneren entweicht, während die Membran außen hydratisiert bleibt. Die Daten zeigen außerdem, wie stark Variationen in der Größe die charakteristischen Welligkeiten der Streukurven verwischen und wie die Auswahl von Teilmengen mit ähnlichen Radien oder Formen – eine „in silico“-Reinigung – klarere strukturelle Signale der Doppelschichtmembran und ihrer dünnen umgebenden Wasserschicht wiederherstellt.
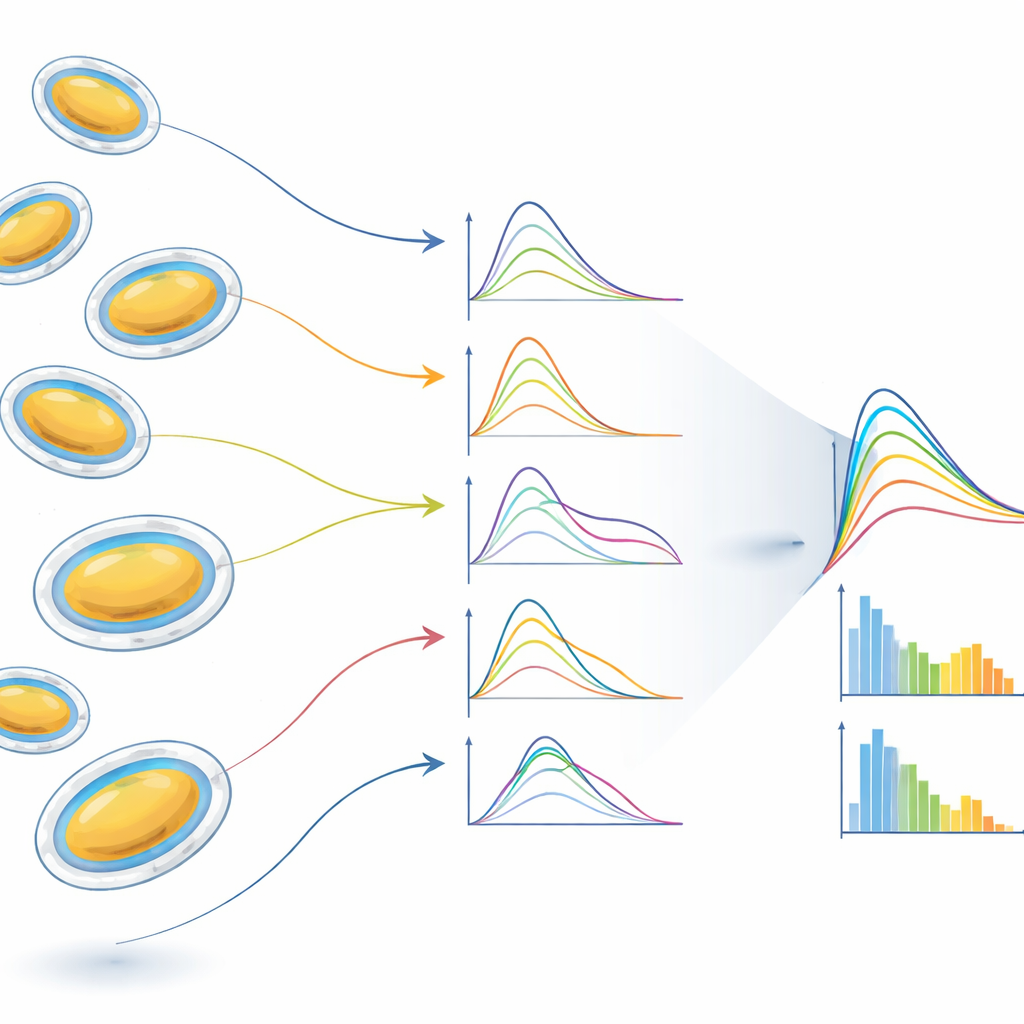
Ein neues Fenster für weiche Nanostrukturen
Durch die Kombination von XFEL-Pulsen, Einzelpartikelzufuhr und modellbasierter Analyse bringt diese Arbeit die traditionelle Kleinwinkel-Röntgenstreuung effektiv auf die Ebene einzelner Vesikel. Anstelle einer Mittelung über ein riesiges Ensemble können Forscher nun Strukturparameter für jedes Vesikel einzeln gewinnen und diese gezielt zu gut definierten Subpopulationen zusammenfassen. Dadurch lässt sich sowohl die durch Polydispersität verursachte Unschärfe reduzieren als auch diese Polydispersität selbst detailliert messen. Der Ansatz ist breit anwendbar auf empfindliche biologische und weichstoffliche Systeme, die von Natur aus heterogen sind – von wirkstofftragenden Liposomen und Proteo-Liposomen bis hin zu komplexeren zellulären Kompartimenten – und eröffnet nicht nur bessere statische Strukturmessungen, sondern perspektivisch auch Echtzeitfilme struktureller Veränderungen, die durch Licht oder andere Stimuli ausgelöst werden.
Zitation: Neuhaus, C., Stammer, M.L., Alfken, J. et al. Structure and polydispersity of single lipid vesicles by small-angle X-ray scattering at European XFEL. Commun Phys 9, 93 (2026). https://doi.org/10.1038/s42005-026-02551-5
Schlüsselwörter: Lipidvesikel, Röntgen-Freie-Elektronen-Laser, Kleinwinkel-Röntgenstreuung, Einzelpartikelbildgebung, NANOBIOTECHNOLOGIE