Clear Sky Science · de
ABEL‑FRET überbrückt die Zeitskala-Lücke in Einzelmolekülmessungen der strukturellen Dynamik am A2A‑Adenosinrezeptor
Winzige Schalter in der Zelle in Echtzeit beobachten
Viele der heutigen Medikamente wirken, indem sie molekulare „Schalter“ an Zelloberflächen — sogenannte Rezeptoren — umlegen. Diese Schalter verändern ständig ihre Form, während sie Signale ein‑ und ausschalten, doch die meisten Werkzeuge können nur die allerschnellsten oder die sehr langsamen Bewegungen erfassen, nicht beides. Diese Arbeit stellt eine Methode vor, mit der sich ein einzelner, für Medikamente relevanter Rezeptor in Lösung deutlich länger beobachten lässt als bisher, und zeigt, wie er in bestimmten, für die Wirkung von Arzneistoffen wichtigen Gestalten verharrt.
Warum diese formwechselnden Proteine wichtig sind
Die Studie konzentriert sich auf eine große Klasse von Zelloberflächenproteinen, die als G‑Protein‑gekoppelte Rezeptoren oder GPCRs bekannt sind. Diese Proteine steuern lebenswichtige Prozesse wie Sehen, Stimmung, Blutdruck und Immunantworten, und mehr als ein Drittel der zugelassenen Arzneimittel zielt auf sie ab. Ein gut untersuchtes Mitglied, der A2A‑Adenosinrezeptor, hilft bei der Regulation von Schlaf, Schmerz, Entzündung und neuronaler Signalübertragung und ist ein vielversprechendes Ziel für die Behandlung von Erkrankungen wie Parkinson und Krebs. GPCRs sind hochflexibel: Wenn verschiedene Moleküle binden, drängen sie den Rezeptor in unterschiedliche Formen, die bestimmte Signalwege begünstigen. Genau diese Flexibilität erschwert jedoch die Wirkstoffgestaltung auf Basis statischer Momentaufnahmen aus Röntgen‑ oder Kryo‑Elektronenmikroskopie.
Einen einzelnen Rezeptor verfolgen, ohne ihn festzupinnen
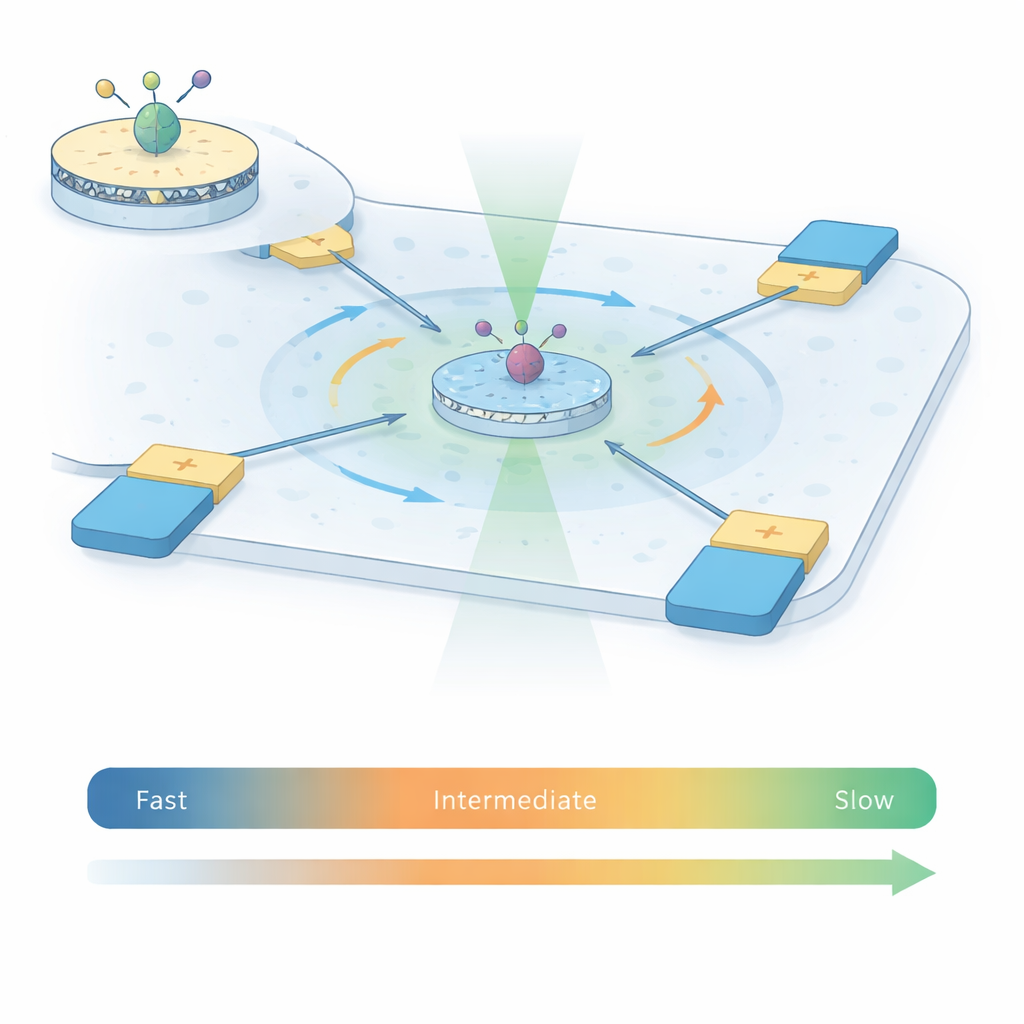
Um zu erfassen, wie sich A2A‑Rezeptoren bewegen, verbinden die Autoren zwei leistungsfähige Techniken zu dem, was sie ABEL‑FRET nennen. Zuerst rekonstituieren sie einzelne Rezeptoren in winzige Patches künstlicher Membran, sogenannte Nanodiscs, wodurch jedes Protein eine natürlicher wirkende Umgebung erhält als nur in Detergens. Sie koppeln ein Paar fluoreszierender Farbstoffe an zwei bewegliche Bereiche auf der Innenseite des Rezeptors. Mit der Formänderung ändern sich Abstand und relative Orientierung der Farbstoffe und damit die Energieübertragung zwischen ihnen — ein Phänomen, das als Förster‑Resonanzenergietransfer (FRET) bekannt ist. Zweitens verwenden sie statt eines Aufklebens auf einer Oberfläche eine Anti‑Brown’sche Elektrokinetische (ABEL) Falle: eine mikrofluidische Kammer mit Elektroden, die registrieren, wo sich ein fluoreszierendes Teilchen befindet, und es sanft zurück in die Mitte treiben, um die zufällige Brownsche Bewegung auszugleichen.
Die fehlende Zeitfenster‑Lücke schließen
Traditionelle Einzelmolekül‑FRET‑Experimente beobachten entweder frei diffundierende Rezeptoren nur für wenige Tausendstelsekunden oder auf einer Oberfläche immobilisierte Rezeptoren für Sekunden bis Minuten. Jede Methode deckt ein anderes Zeitfenster ab. Mit der ABEL‑Falle hält diese Arbeit einzelne A2A‑Rezeptoren ein bis zwei Sekunden im Blick, während sie frei in Lösung bleiben — etwa 100‑mal länger als in diffusionsbegrenzten Experimenten. Die verlängerte Beobachtungszeit erlaubt dem Team, zu messen, wie das FRET‑Signal innerhalb jedes gefangenen Ereignisses und über Tausende von Rezeptoren hinweg schwankt, in vier Zuständen: ohne Ligand, mit einem Antagonisten und mit zwei verschiedenen aktivierenden Molekülen (Agonisten). Statistische Werkzeuge aus der Signalanalyse — Varianz-, Korrelations‑ und Rekurrenzanalysen — erlauben es ihnen, zufälliges Photonenrauschen von echten, langsamen Strukturveränderungen des Rezeptors zu unterscheiden.
Verborgene, lang anhaltende Gestalten sichtbar gemacht
Die FRET‑Signale zeigen, dass Rezeptoren mehrere deutlich unterscheidbare Konformationen einnehmen, die sich während typischer Beobachtungszeiten von einigen Hundert Millisekunden nicht vollständig ineinander umwandeln. In allen Bedingungen ist die Verteilung der FRET‑Werte weit breiter als allein durch Rauschen zu erwarten wäre, was strukturelle Heterogenität offenbart: Verschiedene Moleküle verweilen in unterschiedlichen, lang anhaltenden Formen. Wenn aktivierende Moleküle binden, verschiebt sich das mittlere FRET‑Niveau nach oben, was darauf hindeutet, dass der Rezeptor mehr Zeit in einer „aktiv‑ähnlichen“ Anordnung seiner inneren Helices verbringt. Selbst dann zeigen die Korrelationsanalysen jedoch, dass ein Rezeptor, sobald er sich in einem hohen oder intermediären FRET‑Zustand befindet, eine hohe Wahrscheinlichkeit hat, dort mindestens mehrere Hundert Millisekunden zu verbleiben. Diese Ergebnisse revidieren frühere Schätzungen aus schnelleren Experimenten und verlängern die charakteristischen Verweilzeiten in lang‑lebigen Zuständen von nur Millisekunden auf deutlich über ein Zehntel Sekunde.
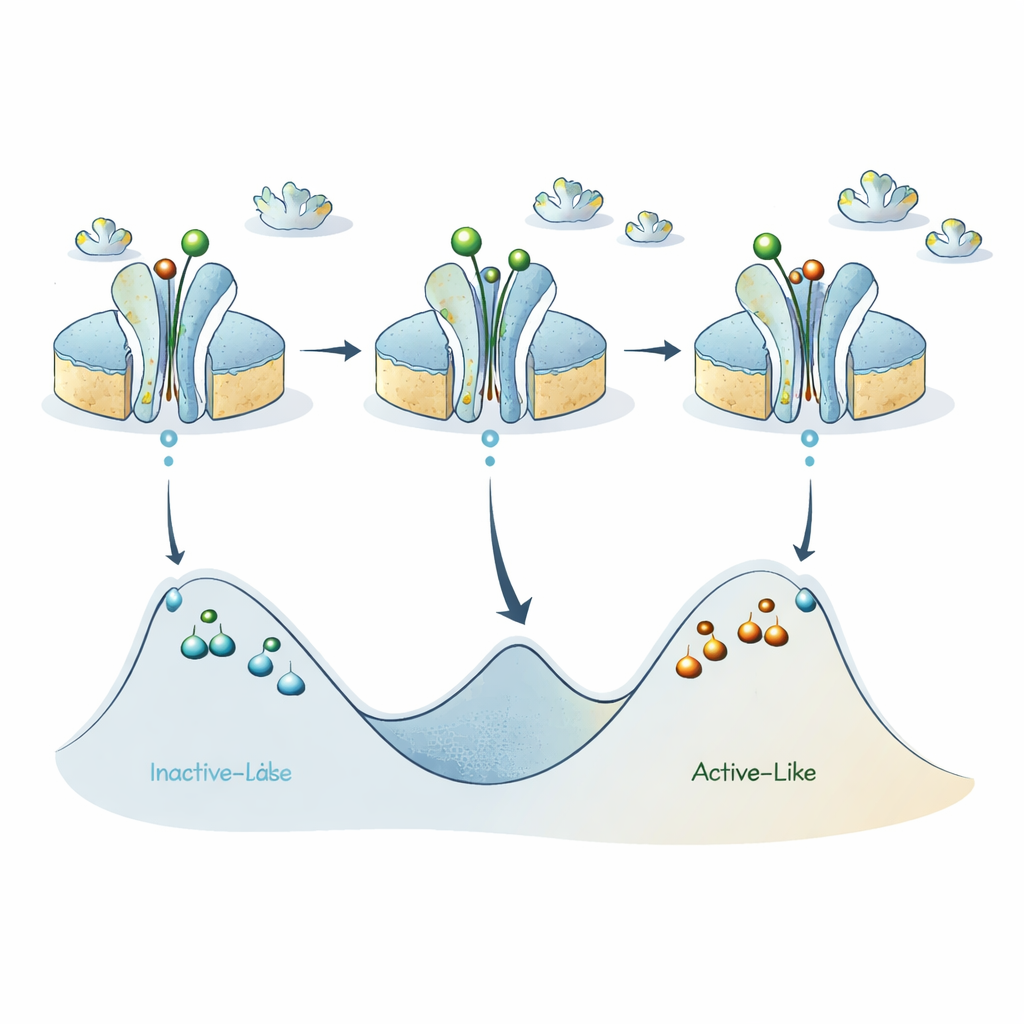
Eine neue Karte der Energielandschaft des Rezeptors
In der Zusammenführung dieser Befunde verfeinern die Autoren ein früheres Modell, wonach der A2A‑Rezeptor hauptsächlich zwischen einem inaktiv‑ähnlichen und einem aktiv‑ähnlichen Zustand umschaltet. Ihre neuen Daten legen nahe, dass jede dieser beiden groben Kategorien tatsächlich mehrere Unterzustände verbirgt, die durch beträchtliche Energiebarrieren getrennt sind, sodass einzelne Rezeptoren überraschend lange in einer bestimmten Ausprägung aktiv‑ähnlich oder inaktiv‑ähnlich „feststecken“ können. Aktivierende Liganden senken die Barriere zwischen den Hauptbecken des Inaktiv‑ und Aktiv‑ähnlichen Zustands und fördern schnelles Umschalten auf sub‑millisekundärer Skala, aber die inneren Barrieren innerhalb jedes Beckens bleiben hoch und erzeugen die langlebigen Unterzustände, die ABEL‑FRET detektiert.
Was das für zukünftige Medikamente bedeutet
Für Nicht‑Spezialisten lautet die Kernbotschaft: Ein Arzneistoffziel wie der A2A‑Rezeptor schaltet nicht einfach nur zwischen „aus“ und „an“. Stattdessen erkundet es eine zerklüftete Landschaft von Formen, von denen einige lange genug bestehen, um für die intrazelluläre Signalübertragung und die Wirkungsweise von Medikamenten über die Zeit relevant zu sein. Indem ABEL‑FRET die Beobachtungsdauer einzelner, natürlicher und ungebundener Rezeptoren verlängert, schließt die Methode eine entscheidende Lücke zwischen ultraschnellen und sehr langsamen Messungen. Dieser Ansatz lässt sich nun auf viele Membranproteine anwenden und bietet ein vollständigeres, zeitaufgelöstes Bild davon, wie potenzielle Arzneistoffziele atmen, sich verschieben und auf therapeutische Verbindungen reagieren.
Zitation: Maslov, I., Borshchevskiy, V., Pérez, I. et al. ABEL-FRET bridges the timescale gap in single-molecule measurements of the structural dynamics in the A2A adenosine receptor. Commun Chem 9, 114 (2026). https://doi.org/10.1038/s42004-026-01941-8
Schlüsselwörter: G‑Protein‑gekoppelte Rezeptoren, Einzelmolekül‑FRET, Adenosin A2A‑Rezeptor, Protein‑Konformationsdynamik, ABEL‑Trap