Clear Sky Science · de
Mechanistische Untersuchung der Sulfatmigration in Glykosaminoglykanen während der MS-Fragmentierung
Warum das Verschieben chemischer Markierungen an Zuckern wichtig ist
Unsere Zellen sind mit langen Zuckerketten überzogen, die Prozesse so unterschiedlicher Art wie Blutgerinnung, Immunabwehr und das Andocken von Viren an Zellen steuern. Viele dieser Ketten tragen winzige chemische Markierungen, sogenannte Sulfatgruppen, deren genaue Positionen entlang des Zuckergerüsts wie ein molekularer Barcode wirken und Proteinen anzeigen, wann und wo sie binden sollen. Wissenschaftler verlassen sich stark auf die Massenspektrometrie — eine mächtige Wägetechnik —, um diese Barcodes zu lesen. Diese Studie zeigt, dass sich Sulfatmarkierungen während solcher Messungen unbemerkt verschieben können und Forschende dadurch möglicherweise falsche Schlüsse über den wahren Aufbau dieser biologisch wichtigen Zuckerketten ziehen.
Komplexe Zuckerketten mit kritischen Markierungen
Glykosaminoglykane sind lange, lineare Zuckerketten, die oft an Proteine auf Zelloberflächen gebunden sind. Ihre Sulfatdekorationen sind nicht zufällig; bereits kleine Änderungen des Sulfatstandorts an einer bestimmten Zuckereinheit können das Zusammenwirken der Kette mit Wachstumsfaktoren, Gerinnungsproteinen oder Krankheitserregern radikal verändern. Deshalb versuchen Forschende nicht nur herauszufinden, wie viele Sulfate vorhanden sind, sondern genau, wo sie sitzen. Die Massenspektrometrie, häufig kombiniert mit kontrolliertem Aufbrechen der Zuckerkette, ist ein Hauptverfahren dafür. Frühere Hinweise deuteten jedoch bereits an, dass geladene Gruppen wie Sulfate sich während der Messung verschieben könnten, was das Auslesen des tatsächlichen Modifikationsmusters erschwert.
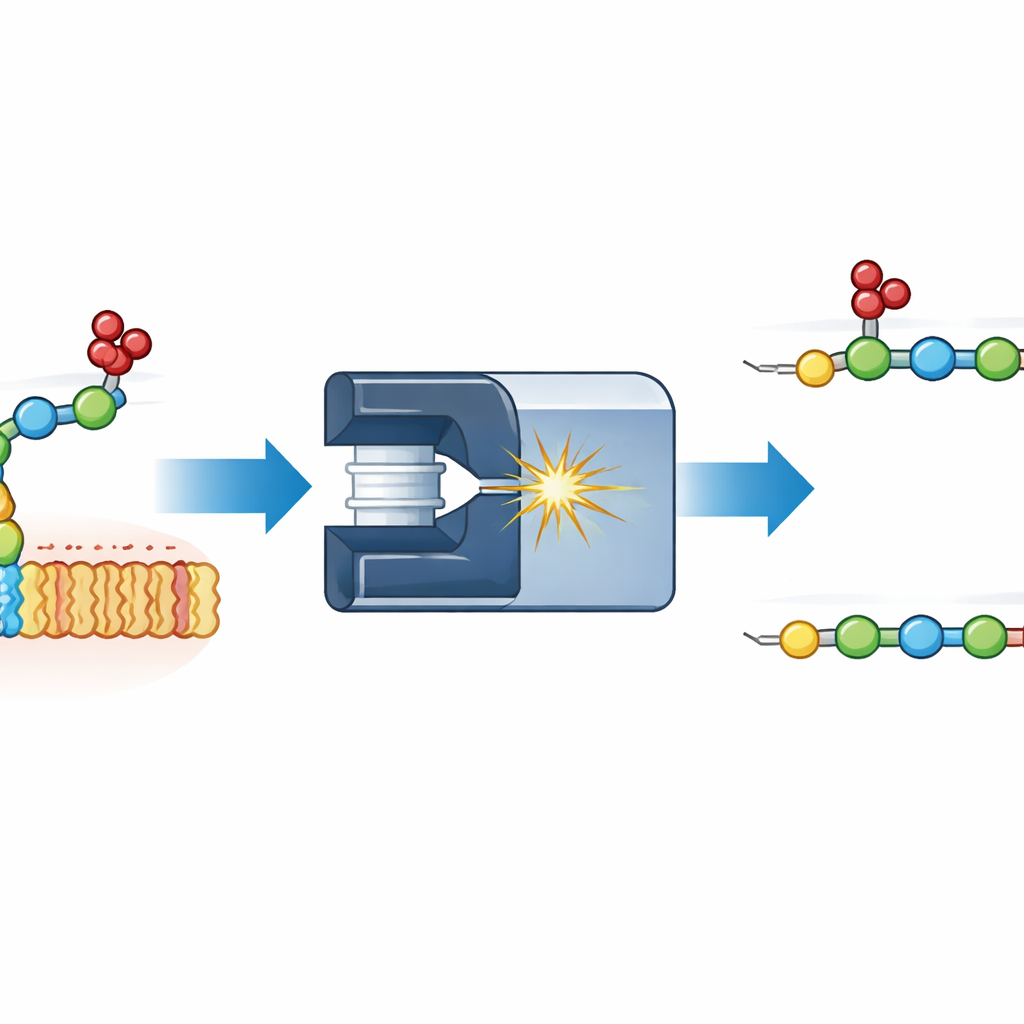
Zuschauen, wie Sulfate sich während der Messung bewegen
Die Autorinnen und Autoren konzentrierten sich auf ein einfaches Modell: ein Disaccharidfragment von Heparansulfat, einem der bekanntesten Glykosaminoglykane. Sie brachten unterschiedliche fluoreszierende Marker an einem Ende des Disaccharids an und fragmentierten es in einem Massenspektrometer. Indem sie maßen, wie die entstehenden Bruchstücke unter einem elektrischen Feld durch ein Gas drifteten — eine Technik namens Ionenmobilität — konnten sie Konformationen unterscheiden, die ansonsten dieselbe Masse hätten. Ein unerwartetes Fragment erschien, das genau um eine Sulfatgruppe schwerer war, jedoch an der falschen Stelle: Statt auf dem ersten Zucker zu verbleiben, war das Sulfat auf den zweiten gewandert. Vergleiche mit sorgfältig synthetisierten Referenzverbindungen zeigten, dass das gewanderte Sulfat an zwei unterschiedlichen Positionen des zweiten Zuckers landen konnte und so zwei verschiedene Formen erzeugte, die durch Ionenmobilität klar getrennt wurden.
Neue Zielpositionen präzisieren und Marker prüfen
Um besser zu verstehen, wo das Sulfat gelandet war und ob andere Positionen möglich sind, kombinierten die Forschenden ihre Messungen mit detaillierten Computersimulationen. Sie berechneten viele mögliche dreidimensionale Konformationen für die Kandidatenstrukturen und sagten voraus, wie sich jede im Gasphasenzustand verhalten sollte. Nur Sulfate an zwei spezifischen Stellen des zweiten Zuckers — in der Fachsprache als 6O- und 3O-Positionen bezeichnet — stimmten mit dem experimentellen Verhalten überein, während andere hypothetische Orte unwahrscheinlich erschienen. Die Forscher prüften anschließend, ob die angefügten Marker selbst die Umverteilung antreiben könnten, indem sie das ursprüngliche Label durch drei einfachere ersetzten. In jedem Fall hielt die Sulfatmigration an und erzeugte ähnliche Fragmenttypen, was darauf hindeutet, dass die Wahl des Markers wenig Einfluss darauf hat, ob Migration stattfindet, wenngleich sie subtil beeinflussen kann, wie leicht sich die verschiedenen Produkte auseinanderhalten lassen.
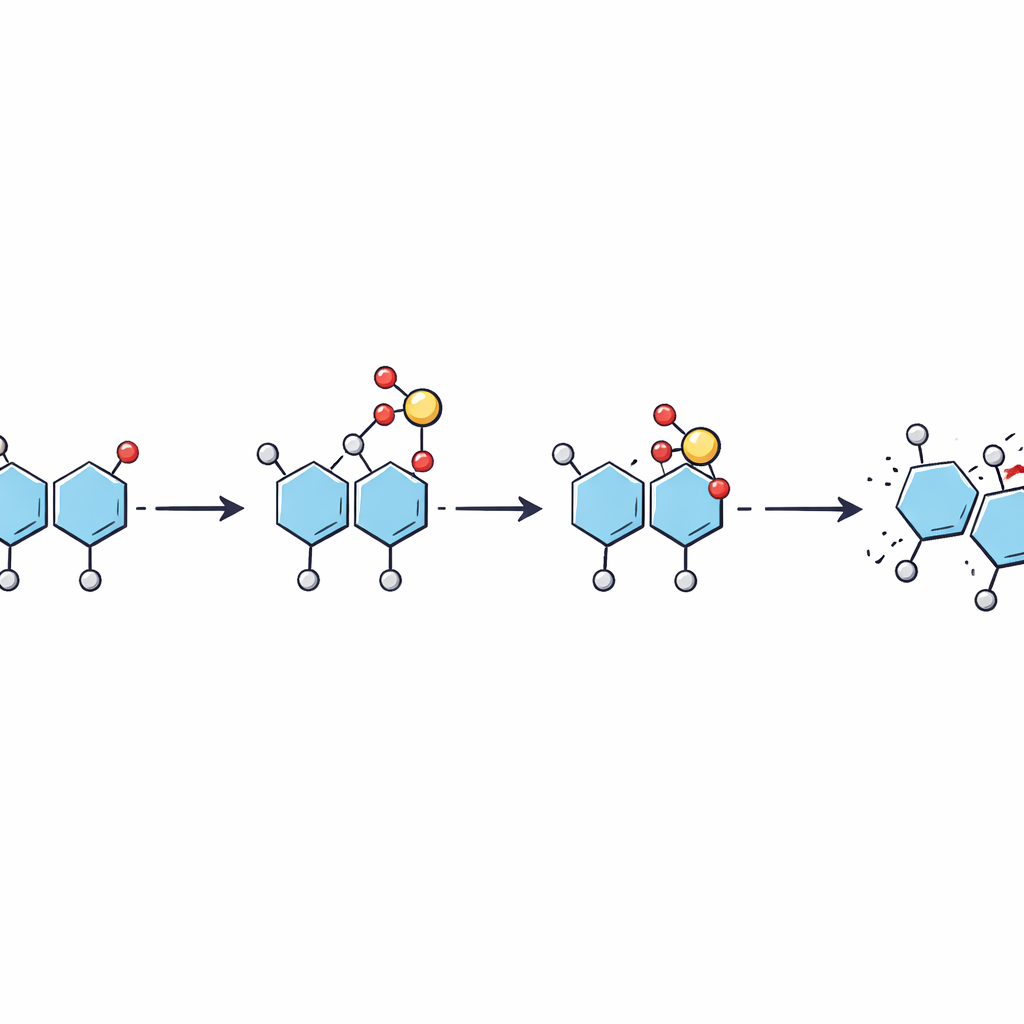
Stufenweises Hüpfen statt eines einzigen Sprungs
Mithilfe energieabgestimmter Fragmentierungsexperimente zusammen mit weiteren Simulationen setzten die Autorinnen und Autoren ein schrittweises Bild zusammen, wie das Sulfat wandert. Wenn das Ion im Massenspektrometer mit Energie versorgt wird, aktiviert zunächst ein mobiler Proton das Sulfat, das dann vom ursprünglichen Zucker auf eine bestimmte Stelle des benachbarten Zuckers hüpft, während die Bindung zwischen ihnen bricht. Dies führt zu einem Fragment, in dem das Sulfat eine Zwischenposition einnimmt. Bei weiterer Energiezufuhr kann das Sulfat entlang desselben Zuckers erneut zu einer stabileren Position wandern. Die Arbeit legt nahe, dass diese Umlagerungen bei geringeren Energien stattfinden können als jene, die nötig sind, um das Zuckerrückgrat zu brechen, sodass sie bei routinemäßigen Analysen unbemerkt im Hintergrund ablaufen können.
Folgen für das Entschlüsseln von Zuckerstrukturen
Für Nicht‑Spezialisten lautet die Kernbotschaft: Die chemischen Markierungen an wichtigen biologischen Zuckern sind während der Analyse nicht immer festgeschrieben; sie können sich entlang der Kette verschieben, während das Molekül durch das Massenspektrometer fliegt. Die Studie zeigt im Detail, dass zumindest für ein repräsentatives Heparansulfatfragment eine Sulfatgruppe von einer Zuckereinheit zur nächsten wandern und sich an neuen Positionen niederlassen kann, wobei Fragmente entstehen, die echte strukturelle Merkmale vortäuschen. Das bedeutet, dass einige frühere und künftige Messungen den Sulfat‑Code falsch interpretieren könnten, sofern nicht zusätzliche Techniken wie Ionenmobilität und fortgeschrittene Modellierung eingesetzt werden, um diese verborgenen Bewegungen aufzudecken. Die Arbeit fordert systematischere Studien, um zu klären, wie verbreitet solche Sulfatmigrationen sind, damit Forschende Zuckermuster auf Zelloberflächen verlässlicher mit Gesundheit und Krankheit in Verbindung bringen können.
Zitation: Polewski, L., Yaman, M., Tokić, M. et al. Mechanistic study on the sulfate migration in glycosaminoglycans during MS fragmentation. Commun Chem 9, 130 (2026). https://doi.org/10.1038/s42004-026-01939-2
Schlüsselwörter: Heparansulfat, Glykosaminoglykane, Massenspektrometrie, Sulfatmigration, Ionenmobilität