Clear Sky Science · de
Bindungstiefen-Modulation beeinflusst die Wirksamkeit photoschaltbarer Liganden am 5-HT2A-Rezeptor
Licht auf schaltbare Hirnmedikamente
Stellen Sie sich ein Medikament vor, das Sie mit einem Lichtblitz an- und ausschalten können, das gezielt Rezeptoren im Gehirn steuert und Nebenwirkungen vermeidet. Diese Studie untersucht genau diese Idee für einen wichtigen Serotoninrezeptor, der mit Stimmung, Wahrnehmung und psychedelischen Wirkstoffen verknüpft ist. Die Forschenden gingen der Frage nach, warum zwei nahezu identische lichtempfindliche Moleküle so unterschiedlich reagieren – eines funktioniert nahezu als perfekter Ein/Aus-Schalter, das andere weigert sich hartnäckig, wirklich auszuschalten. Ihre Antwort beruht auf einem überraschend einfachen Faktor: wie tief das Molekül im Rezeptor sitzt.
Lichtgesteuerte Wirkstoffe im Gehirn
Lichtaktivierte Medikamente, auch photopharmakologische Werkzeuge genannt, sind so gestaltet, dass ein Lichtstrahl einen Teil des Moleküls zwischen zwei Formen umschaltet, etwa einer gebogenen und einer gestreckten Version. Diese Formen können ändern, wie stark das Medikament sein Ziel bindet. In dieser Arbeit ist das Ziel der menschliche 5-HT2A-Rezeptor, ein Protein auf Gehirnzellen, das auf Serotonin reagiert und sowohl bei antipsychotischen wie auch bei psychedelischen Effekten eine zentrale Rolle spielt. Die untersuchten Moleküle sind Derivate von N,N-Dimethyltryptamin (DMT), mit einer lichtempfindlichen Azobenzol-Einheit modifiziert. Zwei Varianten unterscheiden sich nur darin, wo eine winzige Methoxygruppe an einem Ring sitzt – entweder in para- oder meta-Position – doch ihr biologisches Verhalten unter Licht ist dramatisch verschieden.
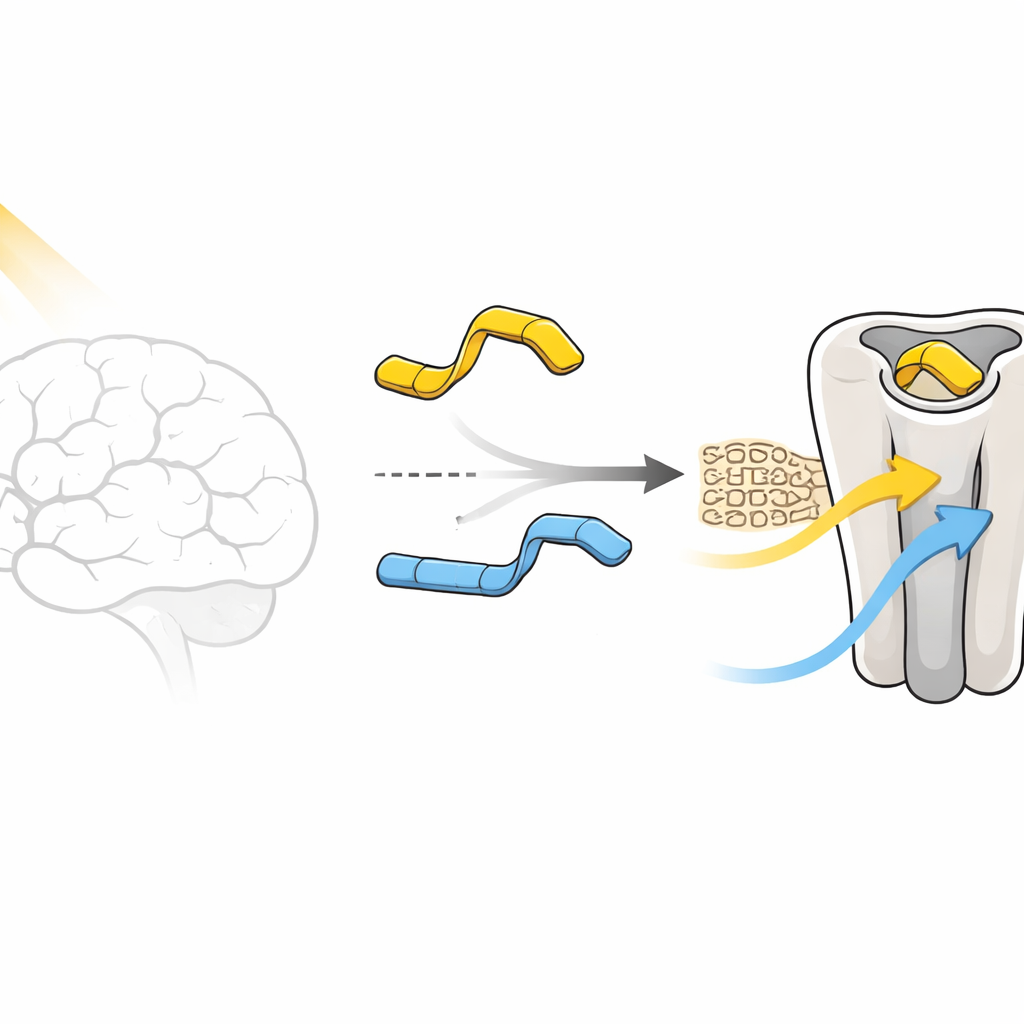
Zwei fast identische Moleküle, sehr unterschiedliche Schalter
In Zelltests verhält sich die para-Variante, genannt Verbindung 1, fast wie ein digitaler Schalter. Im Dunkeln aktiviert ihre „trans“-Form den Rezeptor kaum und blockiert ihn sogar leicht, wirkt also wie ein schwacher Antagonist. Wenn Licht sie in die „cis“-Form bringt, wird dasselbe Molekül zu einem moderaten Aktivator und schaltet den Rezeptor teilweise ein. Die meta-Variante, Verbindung 2, kooperiert nicht auf diese Weise: Sowohl ihre Licht- als auch Dunkel-Formen halten den Rezeptor relativ aktiv und liefern nie einen echten „Aus“-Zustand. Das zentrale Rätsel dieser Arbeit ist, warum eine so minimale chemische Änderung – nur das Verschieben einer kleinen Gruppe am Ring – die Rezeptorantwort so stark verändert.
Ein Blick hinein mit atomgenauen Filmen
Um das zu klären, nutzte das Team umfangreiche All-Atom-Molekulardynamik-Simulationen und drehte praktisch detailreiche Filme jedes Atoms im Rezeptor, der umgebenden Membran, dem Wasser und jedem Liganden über insgesamt etwa 80 Mikrosekunden. Sie simulierten beide Moleküle in beiden lichtgesteuerten Formen sowie in inaktiven und aktiven Formen des 5-HT2A-Rezeptors. Durch Verfolgen bekannter struktureller „Mikroschalter“ im Protein – etwa eines Schlüssel-Tryptophans, das umklappt, einer Salzbrücke, die bricht, und der Bewegung von Natrium und Wasser tief im Kern – konnten sie erkennen, ob der Rezeptor eher in Richtung Aus- oder Ein-Zustand tendierte. Sie verglichen außerdem, wie eng die neuen Moleküle die Bindungsposition von LSD, einem gut untersuchten partiellen Aktivator, nachahmten, wobei die Überlappung ihrer Ringsysteme als Orientierung diente.
Tiefe zählt mehr als nur Form
Die Kernbotschaft ist, dass die Wirksamkeit der Moleküle vor allem davon abhängt, wie tief sie in die Bindetasche des Rezeptors eindringen. Im inaktiven Rezeptor bildet die trans-Form der para-Verbindung spezielle Wasserstoffbrücken, die sie ungewöhnlich tief hineinziehen, unterhalb der Region, in der typische aktivierende Kontakte stattfinden. Dieses „Über-Einströmen“ verhindert, dass sie Schlüsselpolarreste berührt, die den Rezeptor einschalten, sodass es den Aus-Zustand stabilisiert. Die trans-Form der meta-Verbindung kann dieselben Verankerungskontakte nicht eingehen und sitzt stattdessen höher in einer eher LSD-ähnlichen Pose, die mit Aktivierung vereinbar ist, was ihre Restaktivität erklärt. Wenn Licht beide Moleküle in ihre cis-Formen umlässt, wandern sie allgemein in flachere, aktivatorähnlichere Positionen. Doch selbst hier spielt Geometrie eine Rolle: Im aktiven Rezeptor kann cis-Verbindung 2 tiefer in einen hydrophoben Tunnel zwischen zwei Helices hineingleiten und eine beständige Wasserstoffbrücke bilden, die ihr starkes Agonistenverhalten verstärkt, während cis-Verbindung 1 sterisch daran gehindert wird.
Feine Kontrolle über internes Wasser und Ionen
Die Simulationen zeigen außerdem, dass die Bindungstiefe fein die innere Natriumtasche und den Wasserweg abstimmt, die bekanntlich die Rezeptoraktivierung beeinflussen. Tiefe, starre Bindung durch die para-Verbindung in ihrer trans-Form hält ein Natriumion eng eingefangen und die umgebende Region relativ trocken – Merkmale, die mit einem Aus-Zustand assoziiert sind. Im Gegensatz dazu erlaubt die beweglichere Bindung der meta-Verbindung oder die cis-Formen mehr Wasserzugang und lockert die Natriumumgebung, was den Rezeptor für Aktivierung vorbereitet. Ein aromatischer „Toggle-Switch“-Rest kann seine Orientierung leichter umklappen, wenn Liganden flexibel und nicht überverankert sind, und schiebt den Rezeptor weiter in Richtung eines Ein-Zustands, besonders bei cis-Verbindung 2.
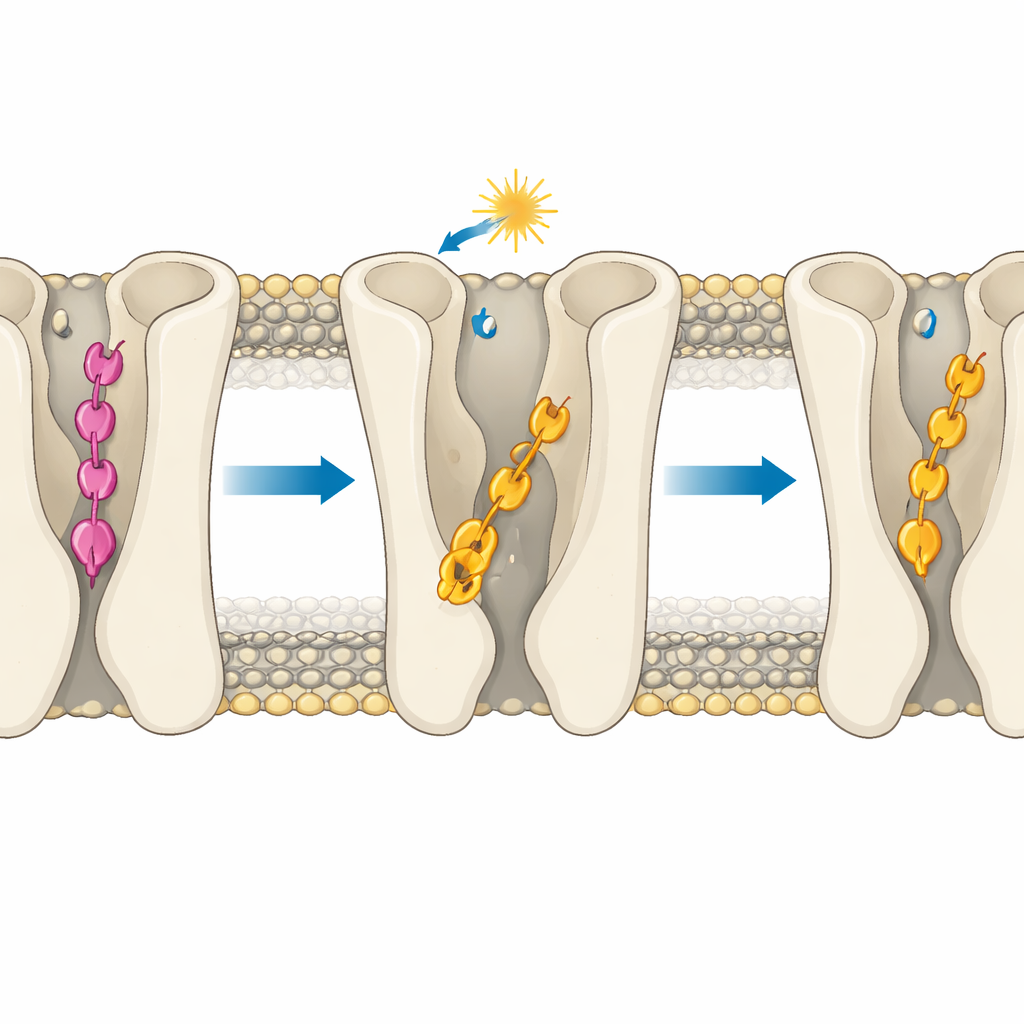
Designregeln für künftige lichtgesteuerte Medikamente
Für Nicht-Spezialisten lautet die Botschaft: Die exakte Tiefe, in der ein Wirkstoff in seiner Rezeptortasche sitzt, kann den Unterschied zwischen Aus, teilweise Ein und starkem Ein ausmachen – selbst wenn die chemische Veränderung auf dem Papier winzig wirkt. Indem die Studie zeigt, wie ein photoschaltbarer Ligand übermäßig tief eindringen und den Rezeptor ausschalten kann, während ein nah verwandter weiterhin in einer aktivierungsfreundlichen Tiefe bleibt, bietet sie eine klare Designregel: Kontrollieren Sie die Eindringtiefe genauso sorgfältig wie die lichtinduzierten Formänderungen. Diese Erkenntnisse könnten die Entwicklung der nächsten Generation lichtsensitiver Verbindungen leiten, die Hirnerkrankungen mit bislang unerreichter Präzision behandeln, Signalwege kontrolliert und reversibel hoch- oder runterregeln und dabei Nebenwirkungen minimieren.
Zitation: Weber, V., Salvadori, G., Natale, F. et al. Binding pose depth modulates photoswitchable ligands’ efficacy at the 5-HT2A receptor. Commun Chem 9, 121 (2026). https://doi.org/10.1038/s42004-026-01936-5
Schlüsselwörter: Photopharmakologie, Serotonin-5-HT2A-Rezeptor, photoschaltbare Liganden, GPCR-Aktivierung, molekulare Dynamik-Simulationen