Clear Sky Science · de
Untersuchung der Stabilität von BOx auf verschiedenen anorganischen Trägern
Sauberere Kraftstoffe aus einem alltäglichen Element
Die Umwandlung von gewöhnlichem Propan – dem Gas aus Grillflaschen – in wertvollere Bausteine für Kunststoffe erfordert meist heiße, energieintensive Prozesse, die zudem viel Kohlendioxid erzeugen. Diese Studie untersucht, wie Verbindungen des vergleichsweise häufigen Elements Bor auf schonendere und sauberere Weise bei dieser Umwandlung helfen können. Indem die Autoren aufdecken, wie Bor sich bei hohen Temperaturen auf verschiedenen festen Oberflächen verhält, zeigen sie neue Ansätze zur Gestaltung von Katalysatoren auf, die nützliche Chemikalien mit weniger Abfall und geringerem Energieverbrauch herstellen.
Warum die Propan-zu-Kunststoff-Chemie wichtig ist
Die moderne Welt ist stark abhängig von leichten Olefinen wie Propen und Ethen, die zentrale Bausteine für Kunststoffe, Fasern und zahllose Alltagsprodukte sind. Heute werden die meisten dieser Verbindungen aus Erdöl oder Erdgas über energiefressende Verfahren hergestellt, die große Mengen CO₂ freisetzen. Ein alternatives Verfahren, die oxidative Dehydrierung von Propan, kann prinzipiell diese Olefine bei niedrigeren Temperaturen und mit weniger unerwünschten Nebenprodukten erzeugen. Borbasierte Materialien sind kürzlich als vielversprechende Katalysatoren für diese Reaktion hervorgetreten, weil sie sehr selektiv sind: Sie begünstigen die Umwandlung von Propan zu Olefinen, anstatt es vollständig zu CO₂ zu verbrennen. Dennoch ist noch nicht vollständig verstanden, wie die „aktiven“ Borspezies aussehen oder wo genau die Reaktion stattfindet – auf der Katalysatoroberfläche, in der Gasphase oder beides.
Überraschende Mobilität von Bor in heißen Reaktoren
Die Autoren konzentrierten sich auf Boroxid, eine einfache Bor-Sauerstoff-Verbindung, oft als BOx bezeichnet, die auf drei gängigen anorganischen Materialien aufgebracht wurde: reinem Siliciumdioxid (Silica), reinem Aluminiumoxid (Alumina) und einem gemischten Silica–Alumina. Mithilfe einer Kombination von Techniken, die Gase verfolgen, die beim Erhitzen von der Oberfläche entweichen, sowie Methoden, die die lokale Atomstruktur in Feststoffen untersuchen, zeigten sie, dass Bor nicht immer am Ort bleibt. Auf Silica neigt Boroxid dazu, lose gebundene Cluster zu bilden, die verdampfen und flüchtige borspezifische Arten in den Gasstrom abgeben können. Auf alumina-reichen Trägern bindet Bor hingegen stärker an aluminiumverknüpfte Sauerstoffatome und bildet ein stabileres, glasartiges Netzwerk, das sich dem Auswaschen in die Gasphase widersetzt. Einfache Waschtests untermauerten dieses Bild: Das meiste Bor ließ sich von Silica-unterstützten Proben abspülen, jedoch deutlich weniger von alumina-basierten.
Verknüpfung der Bor-Stabilität mit katalytischem Verhalten
Diese Unterschiede in der Bor-Mobilität korrelierten eng mit dem katalytischen Verhalten in der Propanreaktion. Auf Silica unterstütztes Boroxid begann bei etwa 80 °C niedrigeren Temperaturen, Propan in Olefine umzuwandeln, als Katalysatoren mit Alumina, obwohl alle drei Systeme letztlich sehr ähnliche Beziehungen zwischen Propanumsetzung und Olefinselektivität zeigten. Beim Erhitzen der Proben unter gleichzeitiger Überwachung borhaltiger Fragmente in der Gasphase wurde deutlich, dass Silica bei Reaktionstemperaturen viel mehr Boroxid und verwandte Spezies freisetzte als Alumina. Das deutet darauf hin, dass Träger, die Bor leichter entweichen lassen, die Reaktion früher auslösen können, weil reaktivere borspezifische Zwischenstoffe in die Gasphase gelangen und dort Kettenreaktionen anstoßen, die Propan umwandeln.
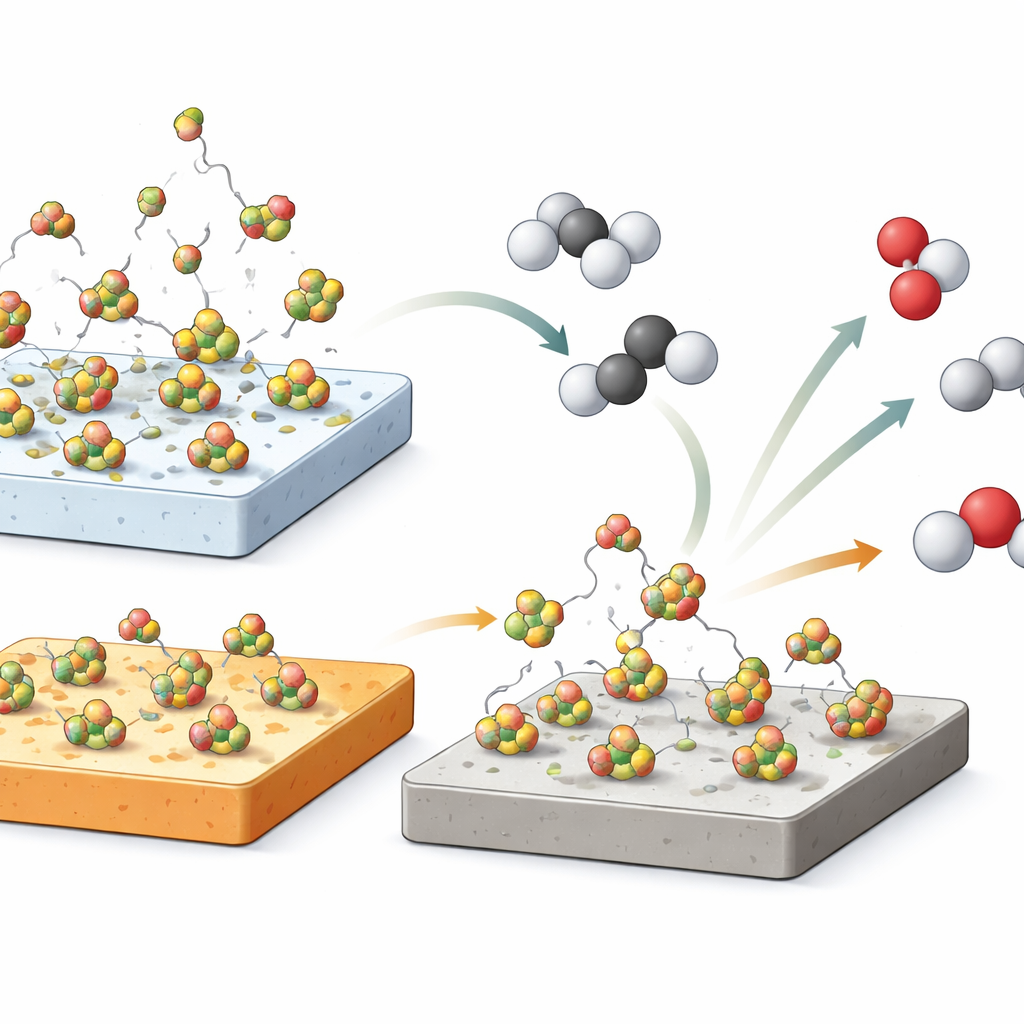
Gasförmiges Bor als unsichtbarer Helfer
Um zu prüfen, ob gasförmiges Bor allein die Chemie antreiben kann, führten die Forscher ein aufsehenerregendes Experiment durch: Sie entfernten den festen Katalysator vollständig und injizierten stattdessen einen winzigen Impuls einer Borsäurelösung – in etwa ein Siebzigstel der Bormenge, die normalerweise auf einem Katalysator vorhanden ist – direkt in einen heißen, leeren Reaktor. Als die Lösung bei 500 °C schnell zu Boroxid zersetzte, stieg die Propanumsetzung um ungefähr 20 %, bei einer Olefinselektivität, die der über den Festkatalysatoren ähnelt. Ein Kontrollversuch mit reinem Wasser erzeugte nur einen kleinen, kurzlebigen Effekt. Zusammen mit den Desorptionsmessungen deutet dieses Ergebnis stark darauf hin, dass flüchtige borspezifische Arten in der Gasphase eine wichtige Rolle spielen, wahrscheinlich indem sie radikalische Ketten initiieren, die Propan in Propen und Ethen umwandeln.
Was das für künftige Katalysatoren bedeutet
Für Nichtfachleute ist die wichtigste Erkenntnis, dass der feste Träger unter einem borbasierten Katalysator nicht nur ein inert wirkendes Gerüst ist – er steuert aktiv, wie viel Bor in die Gasphase entweichen kann und damit, wie leicht die Reaktion beginnt. Träger wie Silica, die Bor leichter freisetzen, führen zu einer Aktivierung des Propans bei niedrigeren Temperaturen, während alumina-reiche Träger Bor stärker festhalten und höhere Temperaturen erfordern, obwohl am Ende bei laufender Reaktion alle ähnliche Produktselektivitäten erreichen. Diese Einsicht legt nahe, dass das gezielte Abstimmen der Bindungsstärke von Bor an seinen Träger Chemikern ermöglichen könnte, Katalysatoren zu entwickeln, die Stabilität und Aktivität ausbalancieren und so sauberere, energieeffizientere Wege von einfachen Brennstoffen wie Propan zu den Molekülen eröffnen, die moderne Materialien begründen.
Zitation: Johánek, V., Wróbel, M., Knotková, K. et al. Exploring the stability of BOx at various inorganic supports. Commun Chem 9, 116 (2026). https://doi.org/10.1038/s42004-026-01926-7
Schlüsselwörter: Boroxid-Katalysatoren, oxidative Dehydrierung von Propan, radikalische Gasphasen-Chemie, Silica- und Alumina-Träger, Olefinsynthese