Clear Sky Science · de
Kristallisation ausgelöst durch Massendiffusion bei niedrigerer lokaler Übersättigung
Warum das über das Labor hinaus wichtig ist
Salzkristalle wirken vielleicht alltäglich, doch ihre Entstehung hat weitreichende Folgen — von der Arzneimittelherstellung bis zur Rückgewinnung von Ressourcen aus salzhaltigen Abwässern. Diese Studie zeigt, dass Kristalle früher und an anderen Orten zu wachsen beginnen können, wenn die Flüssigkeit durch Temperatur- und Konzentrationsgradienten sanft aus dem Gleichgewicht gedrängt wird. Das Verständnis dieses feinen Verhaltens kann helfen, sauberere und günstigere Verfahren zur Behandlung von Brüden zu entwerfen, bessere Materialien zu erzeugen und unerwünschte Ablagerungen in Rohren und Anlagen zu kontrollieren.

Wie Kristalle normalerweise entstehen
Kristallisation tritt auf, wenn ein gelöster Stoff, etwa Kaliumchlorid (KCl) in Wasser, über die Menge hinausgeht, die bequem gelöst bleiben kann. Dieser Zustand heißt Übersättigung. Klassische Theorien besagen, dass Kristalle nur dann erscheinen, wenn die Übersättigung hoch genug ist, um eine Energiebarriere zu überwinden, und dass die Keimbildung dort beginnen sollte, wo die Lösung am stärksten übersättigt ist. In der Industrie treibt man Lösungen üblicherweise durch Abkühlung, Verdampfen des Lösungsmittels oder Zugabe eines „Antilösungsmittels“ in diesen Zustand. Unter diesen konventionellen, weitgehend gleichförmigen Bedingungen haben Forschende eine metastabile Zone kartiert — ein Fenster, in dem die Flüssigkeit übersättigt ist, aber noch keine sichtbaren Kristalle gebildet hat.
Drei verschiedene Wege, dasselbe Salz kristallisieren zu lassen
Die Autorinnen und Autoren untersuchten, wie KCl-Kristalle unter drei sorgfältig kontrollierten Szenarien in einer eigens konstruierten, flachen Zelle mit separater Temperatursteuerung oben und unten auftreten. Zuerst führten sie Standard-Abkühlungsexperimente durch, senkten die Temperatur gleichmäßig von 20 °C und beobachteten, wann die ersten Kristalle erschienen. Das ergab eine Referenzgrenze in der Konzentrations–Temperatur-Karte: unterhalb einer bestimmten Temperatur bildeten sich stets Kristalle; oberhalb blieb die Lösung stundenlang frei von Kristallen. Diese Referenz verglichen sie anschließend mit zwei komplexeren Situationen, in denen die Lösung eine gerichtete Massenströmung erlebte statt einer einfachen, gleichförmigen Abkühlung.
Wenn Wärme Salz bewegen lässt
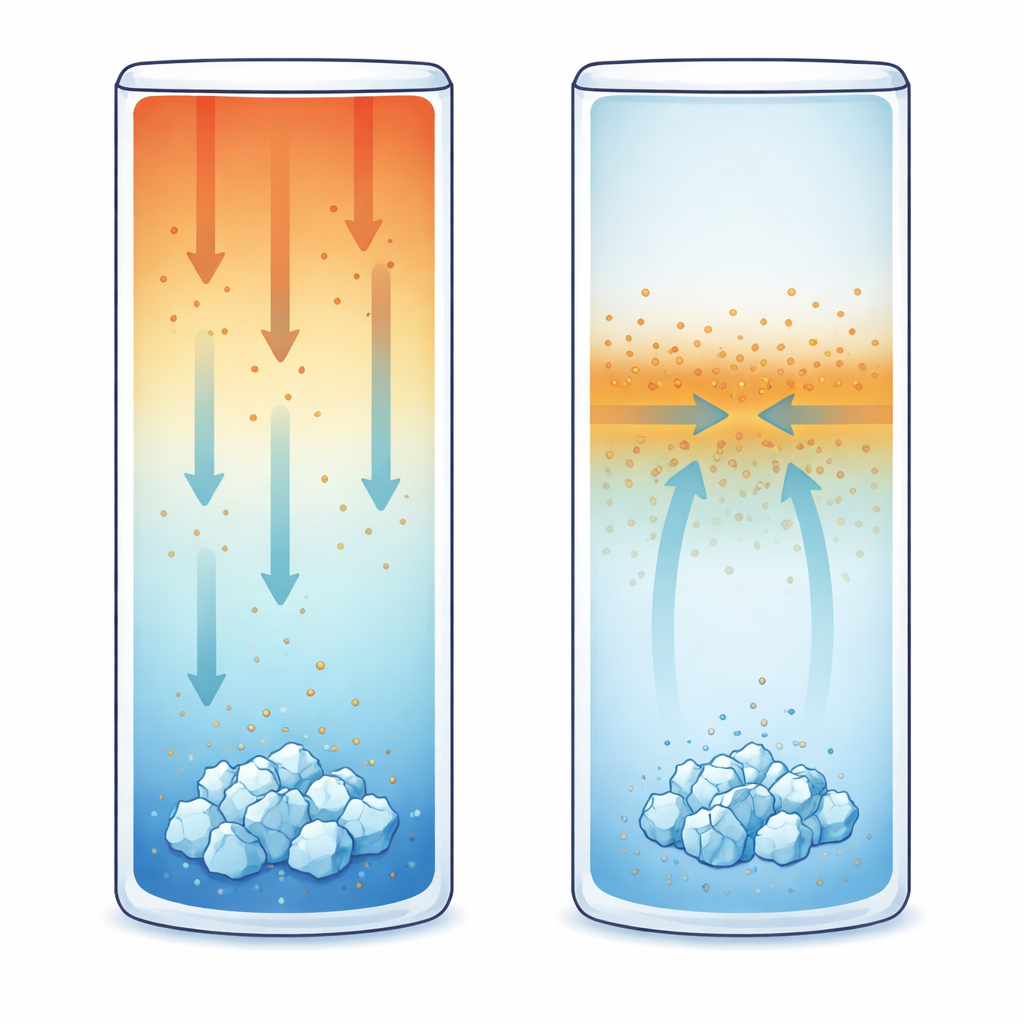
Im zweiten Versuchsblock begann die Lösung mit derselben Zusammensetzung, wurde aber so gehalten, dass oben 20 °C und unten 15 °C herrschten. Dieser vertikale Temperaturgradient verursacht Thermodiffusion, das heißt gelöste Ionen drifteten als Reaktion auf Temperatur und nicht nur auf Konzentration. Für KCl im getesteten Bereich ist das Verhalten thermophob: Ionen neigen dazu, sich in Richtung der kälteren Region zu bewegen und sich so vermehrt am Boden anzureichern. Mit einer empfindlichen optischen Methode, der phasenverschobenen Interferometrie, verfolgten die Forschenden winzige Änderungen des Brechungsindexes, die zeigen, wie sich Konzentration und Temperatur entwickeln. Sie fanden heraus, dass sich Kristalle konsequent an der kalten unteren Wand bildeten — in Bereichen, in denen der Konzentrationsgradient am steilsten war — obwohl die lokale Übersättigung dort leicht niedriger war als im Fall der gleichmäßigen Abkühlung. Anders gesagt ermöglichte der anhaltende Massenfluss die frühere Ausbildung von Kristallen als erwartet.
Wenn Salz bei vollkommen einheitlicher Temperatur diffundiert
Das dritte Szenario beseitigte Temperaturunterschiede vollständig. Die gesamte Zelle wurde konstant bei 17 °C gehalten und zunächst mit der Referenzlösung gefüllt. Dann wurde aus einer oberen Ecke eine kleinere Menge einer verdünnten KCl-Lösung sanft injiziert, wodurch ein scharfer Konzentrationskontrast entstand, aber kaum Strömung aufkam. Die Diffusion glättete diesen Kontrast, während Ionen vom konzentrierteren in den verdünnten Bereich wanderten. Auch hier zeigte die Interferometrie, wie sich das Konzentrationsfeld im Laufe der Zeit entwickelte. Überraschenderweise erschienen die ersten sichtbaren Kristalle nicht dort, wo die Lösung am stärksten übersättigt war. Stattdessen bildeten sie sich etwa auf halber Höhe der Zelle, nahe der Grenzfläche, an der der Konzentrationsgradient — und damit der diffusive Massenfluss — am stärksten war.
Was das für Theorie und Technik bedeutet
Bei allen drei Methoden — Abkühlung, Thermodiffusion und isotherme Diffusion — sahen die ersten auftauchenden Kristalle sehr ähnlich aus: überwiegend kubische KCl-Kristalle mit bekannten Wachstumsformen. Verändert hat sich nicht die Kristallstruktur, sondern die Bedingungen, die ihre Keimbildung auslösten. Unter aufgezwungenen Massenflüssen traten Kristalle bei niedrigerer lokaler Übersättigung und an Orten auf, die von Gradienten statt von Konzentrationsmaxima bestimmt wurden. Das deutet darauf hin, dass gerichteter molekularer Verkehr in der Flüssigkeit Ionen zu dichten Bereichen ordnen kann, die als frühe Keime fungieren und die metastabile Zone effektiv verengen. Während die klassische Keimungstheorie dieses Verhalten nicht vollständig erklärt, stimmen neuere Mehrschritt-Keimbildungsmodelle mit den Beobachtungen überein. Praktisch weist die Arbeit auf eine intelligentere Steuerung der Kristallisation in Prozessen wie der Null-Flüssig-Ableitung (zero-liquid-discharge) in der Entsalzung hin, bei der die Nutzung von Thermodiffusion helfen könnte, Abfallbrühen mit weniger Energie und Chemikalien in feste Salze zu verwandeln.
Zitation: Xu, S., Torres, J.F. Crystallisation triggered by mass diffusion at a lower local supersaturation. Commun Chem 9, 125 (2026). https://doi.org/10.1038/s42004-026-01925-8
Schlüsselwörter: Kristallisation, Thermodiffusion, Übersättigung, Entsalzung, Massenfluss