Clear Sky Science · de
Synergistische Kationen‑Facetten‑Effekte beschleunigen die alkalische Wasserstoffbildungs‑Kinetik auf gestuften Pt‑Oberflächen
Warum das für saubere Energie wichtig ist
Die Erzeugung von sauberem Wasserstoff aus Wasser ist ein zentraler Baustein vieler Netto‑Null‑Energiepläne. Dennoch verschwenden die derzeit praktischsten Geräte Energie, weil die Reaktion, die Wasserstoffblasen erzeugt, in alkalischen (basischen) Lösungen überraschend langsam sein kann. Diese Studie geht bis auf die Ebene einzelner Atome und Wassermoleküle, um zu erklären, warum manche Platinoberflächen besser funktionieren als andere und wie häufige gelöste Ionen in der Lösung mit der Metalloberfläche zusammenwirken können, um die Wasserstoffproduktion zu beschleunigen.
Metalloberflächen formen, um Wasser zu lenken
Die Forschenden konzentrieren sich auf Platin, das Referenzmaterial zur Wasserspaltung, und vergleichen zwei Arten atomarer Landschaften auf seiner Oberfläche. Die eine ist flach, wie eine glatte Terrasse (genannt Pt(111)); die andere ist gestuft, wie eine winzige Treppe (Pt(311)). Mit fortgeschrittenen quantenmechanischen Simulationen, die sowohl Elektronen als auch bewegte Wassermoleküle einbeziehen, modellieren sie das Verhalten dieser unterschiedlichen Oberflächen unter realistischen Betriebs‑Spannungen in einem alkalischen Elektrolyseur. Ziel ist es, zu sehen, wie die lokale Umgebung direkt neben dem Metall — dort, wo Wasser, Ionen und Elektronen zusammentreffen — die Geschwindigkeit des ersten Schritts der Wasserstoffbildung steuert.
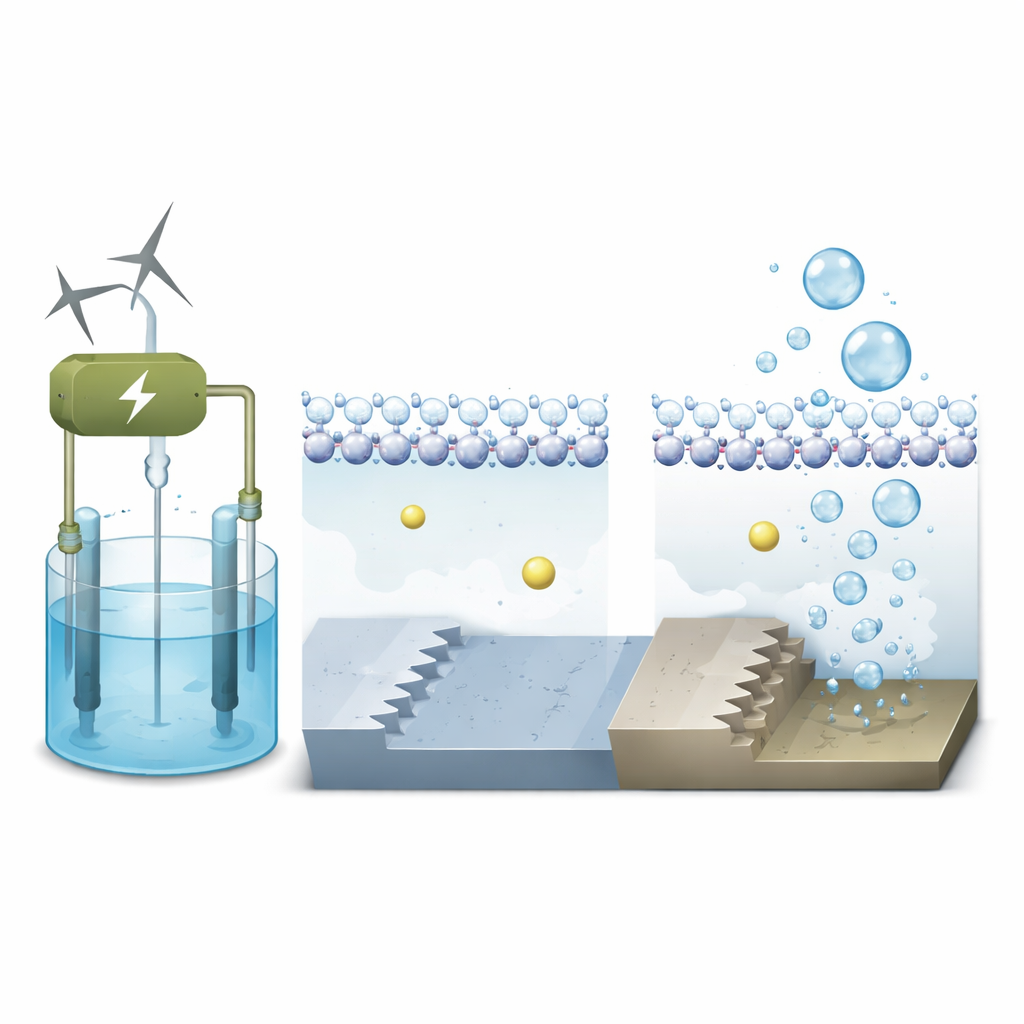
Salzionen als versteckte Helfer
In alkalischen Elektrolyseuren enthält die Flüssigkeit Alkalimetallionen wie Natrium. Diese positiv geladenen Ionen treiben nicht nur ziellos umher; sie können sich in der Nähe der Elektrode anhäufen und das elektrische Feld an der Grenzfläche subtil umgestalten. Die Simulationen zeigen, dass auf der flachen Platinterrasse Wasser eine dichte, geordnete Schicht bildet, wobei die Wasserstoffatome nach unten zur negativ geladenen Oberfläche zeigen. Natriumionen verbleiben weiter entfernt, durch diese Wasserschicht vom Metall getrennt, sodass ihr Einfluss auf die Reaktion eher moderat ist. Auf der gestuften Oberfläche hingegen binden die unterkoordinieren Atome an der Stufenkante Wasser stärker und erzeugen eine rauere, unordentlichere lokale Wasserstruktur.
Ein spezieller Nahflächen‑Cluster, der Ionen näher zieht
An diesen Stufenkanten entdeckt das Team ein wiederkehrendes Strukturmotiv: ein Wassermolekül, das direkt an die Platinstufe gebunden ist und seinerseits ein nahe gelegenes Natriumion zusammen mit weiteren Wassermolekülen hält. Dieser kompakte Platin–Wasser–Natrium‑Cluster zieht das Ion effektiv um etwa 2,3 Å näher an das Metall heran als auf der flachen Oberfläche. Die größere Nähe verstärkt das lokale elektrische Feld in dieser winzigen Region erheblich und polarisiert benachbarte Wassermoleküle stark. Die Simulationen zeigen, dass eine O–H‑Bindung in diesen Wassermolekülen stärker gedehnt ist als üblich, was darauf hinweist, dass sie bereits teilweise zu brechen beginnt, noch bevor die Reaktion formal abläuft.
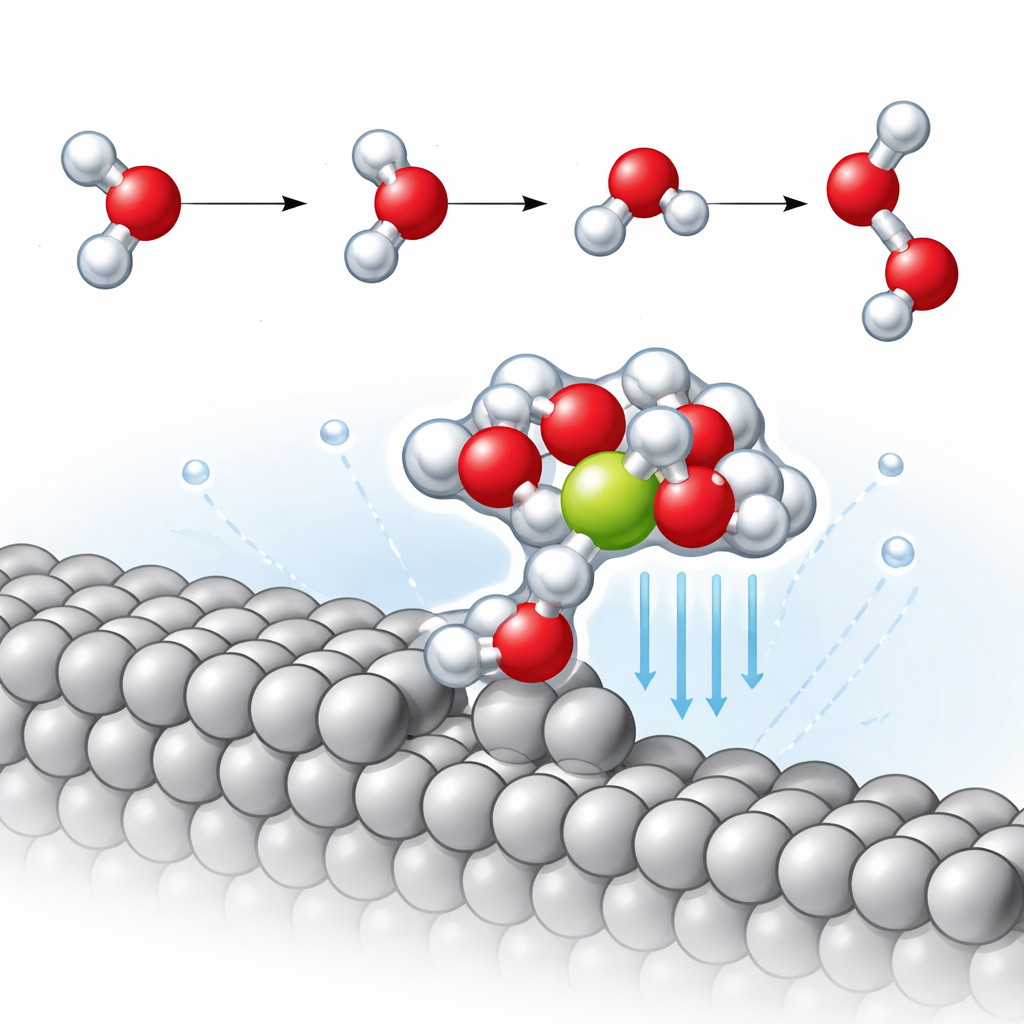
Verringerung der Barriere für Wasserstoffbildung
Der entscheidende langsame Schritt der alkalischen Wasserstoffentwicklung ist als Volmer‑Schritt bekannt: Dabei spaltet ein Wassermolekül, Wasserstoff bindet an das Metall, während das verbleibende Hydroxid in die Flüssigkeit abdriftet. Indem sie den energieärmsten Reaktionsweg verfolgen, finden die Autorinnen und Autoren heraus, dass Natrium auf der flachen Platinoberfläche nur einen geringen Einfluss auf die Aktivierungsenergie dieses Schritts hat. Im Gegensatz dazu senkt auf der gestuften Oberfläche der in der Nähe stabilisierte Natrium‑Cluster die Aktivierungsenergie um etwa 0,14 Elektronenvolt — ungefähr das Dreifache der Verbesserung, die auf der flachen Facette beobachtet wird. Eine detaillierte Analyse der Schwingungsbewegungen zeigt, dass die zum Metall gerichtete O–H‑Bindung in Anwesenheit des nahen Ions deutlich geschwächt wird, wodurch sie leichter bricht und so die Wasserstoffbildung beschleunigt.
Eine Gestaltungsregel für bessere Wasserstoffkatalysatoren
Insgesamt kommt die Studie zu dem Schluss, dass die beste Leistung bei der alkalischen Wasserstoffproduktion nicht allein von der Metalloberfläche oder dem Elektrolyten abhängt, sondern von ihrem Zusammenspiel. Gestufte Platinstellen, die spezielle Wasser‑Ionen‑Cluster verankern können, ziehen Alkalikationen nahe heran, verstärken das lokale elektrische Feld, brechen Wasserbindungen teilweise vor und beschleunigen so den entscheidenden ersten Schritt der Wasserstoffentwicklung stark. Für eine nicht‑fachliche Leserschaft lautet die Quintessenz: Durch sorgfältiges Formen der mikroskopischen Gestalt von Katalysatoroberflächen und die Auswahl von Elektrolyten, die die richtigen Ionen an die richtigen Stellen bringen, können Ingenieurinnen und Ingenieure einige der grundlegenden Verlangsamungen alkalischer Geräte überwinden und energieeffizientere Systeme zur Erzeugung von sauberem Wasserstoff entwerfen.
Zitation: Zhang, Q., Sun, P., Li, H. et al. Synergistic cation-facet effects boost alkaline hydrogen evolution kinetics on stepped Pt surfaces. Commun Chem 9, 113 (2026). https://doi.org/10.1038/s42004-026-01924-9
Schlüsselwörter: Wasserstoffentwicklung, alkalische Elektrolyse, Platinkatalysator, Grenzflächenwasser, Alkalimetallkationen