Clear Sky Science · de
Strukturelle Grundlage der Filamentbildung von menschlichem RegIIIα
Wie unser Darm Keime bekämpft
Unsere Darme sind ständig Milliarden von Bakterien ausgesetzt, von denen viele harmlos oder sogar nützlich sind. Erscheinen jedoch gefährliche Mikroben, benötigt der Körper schnelle, präzise Wege, sie zu bekämpfen, ohne eigenes Gewebe zu schädigen. Diese Studie betrachtet eines dieser natürlichen Abwehrproteine, genannt RegIIIα, und zeigt, wie es seine Gestalt verändert, um Bakterien zu töten, und sich anschließend in eine sicherere, weniger schädliche Form umschaltet. Das Verständnis dieses Formwechsels könnte Forschern helfen, besser nachzuvollziehen, wie wir das Gleichgewicht der Darmmikrobiota erhalten und was bei Krankheiten schiefgeht.
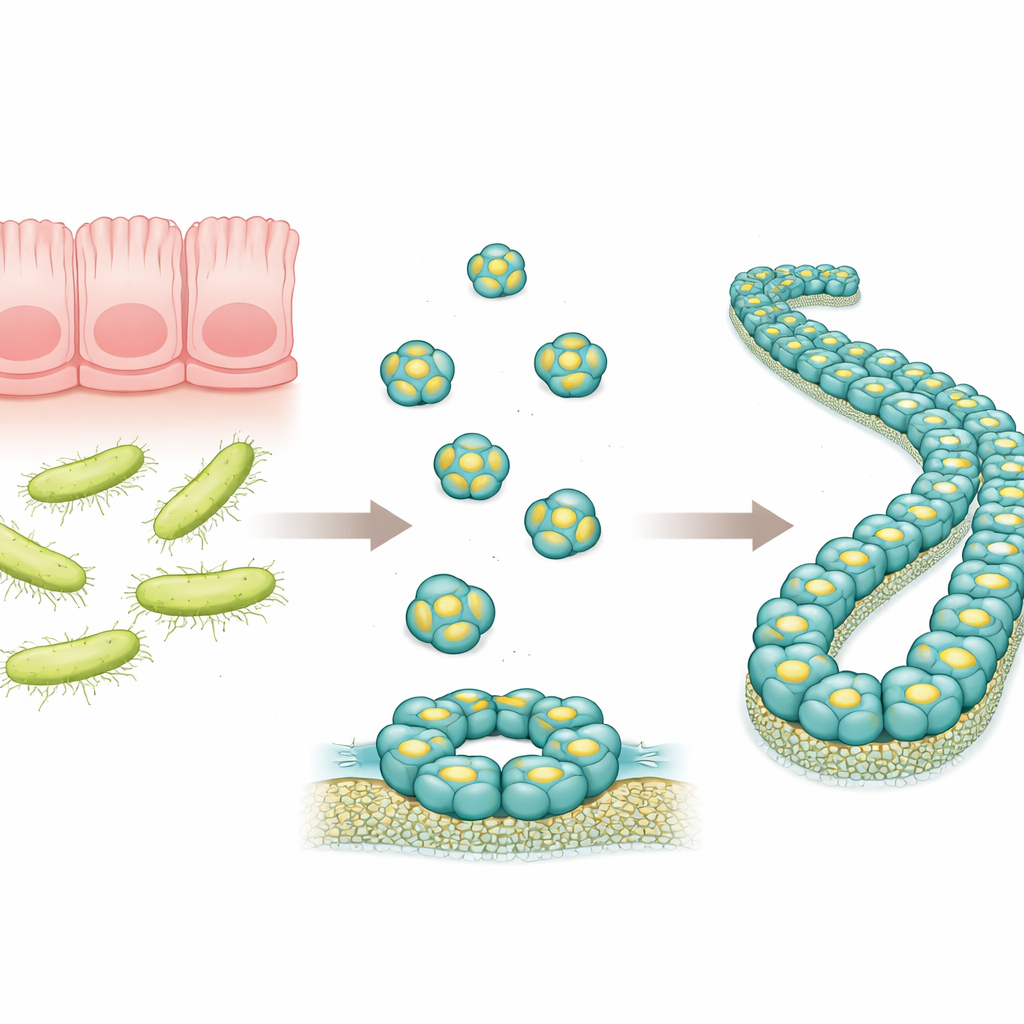
Ein winziger Verteidiger im Darm
RegIIIα ist ein im Verdauungstrakt produziertes Protein, das bestimmte Bakterien ins Visier nimmt, insbesondere solche mit dicken Außenwänden, den sogenannten Gram-positiven Bakterien. Frühere Arbeiten legten nahe, dass RegIIIα Löcher in bakterielle Membranen schlagen kann, indem es ringförmige Strukturen bildet, durch die der Inhalt des Mikroben ausläuft und zum Tod führt. Forschende beobachteten außerdem, dass sich diese Ringstrukturen mit der Zeit zu langen Filamenten aufstapeln, die scheinbar die tödliche Wirkung des Proteins verringern. Die genaue Anordnung der RegIIIα-Moleküle in diesen größeren Assemblierungen war jedoch nicht im Detail bekannt, was das Verständnis seiner Funktion und der Kontrolle seiner Aktivität erschwerte.
Das Filament in atomarem Detail sehen
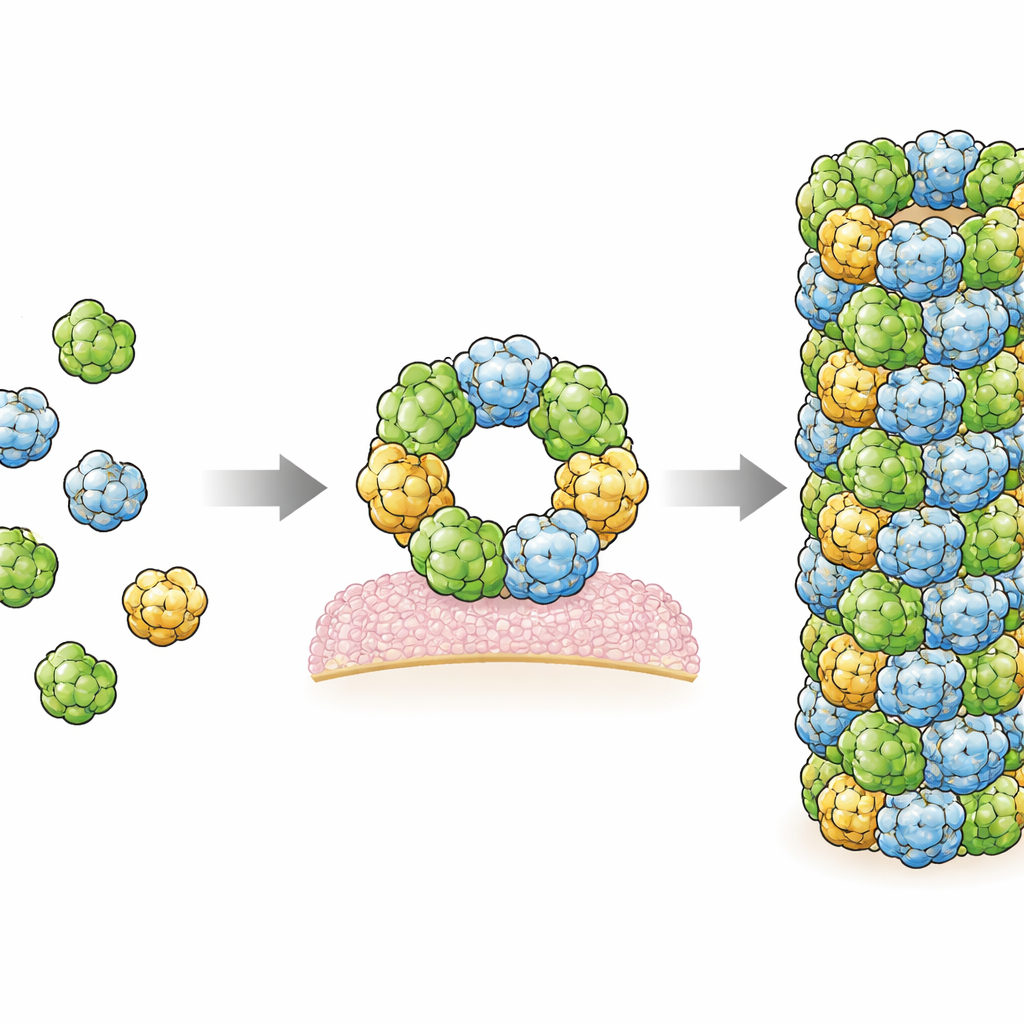
In dieser Studie stellten die Autorinnen und Autoren menschliches RegIIIα in Bakterien her und lösten dann seine Assemblierung zu Filamenten unter kontrollierten Bedingungen aus. Sie nutzten eine leistungsfähige Bildgebungsmethode, die Kryo-Elektronenmikroskopie, die biologische Moleküle in einer dünnen Eisschicht mit nahezu atomarer Auflösung sichtbar machen kann. Sie fanden heraus, dass sich die Filamente aus sich wiederholenden Dreiergruppen identischer RegIIIα-Einheiten, sogenannten Trimern, zusammensetzen, die in einem regelmäßigen Helixmuster aufeinandergestapelt sind. Jedes einzelne RegIIIα-Molekül ähnelt stark dem, was zuvor in Kristallstrukturen beobachtet wurde, doch ihre Orientierung innerhalb des Filaments unterscheidet sich von einem früheren, niedrigauflösenderen Modell. Diese korrigierte Orientierung verändert, wie Wissenschaftler*innen denken, dass das Protein mit bakteriellen Membranen und mit seinem eigenen regulatorischen Segment interagiert.
Wie Proteine sich verbinden und warum Lipide wichtig sind
Durch genaue Betrachtung der Struktur identifizierten die Forschenden zwei Hauptkontaktregionen, oder Schnittstellen, an denen benachbarte RegIIIα-Moleküle aneinanderstoßen und das Filament zusammenhalten. Sie veränderten daraufhin spezifische Aminosäuren an diesen Schnittstellen und zeigten, dass diese Veränderungen die Filamentbildung verhinderten, was bestätigte, dass diese Kontaktstellen unerlässlich sind. Interessanterweise zeigten die Kryo-EM-Karten in beiden Schnittstellen zusätzliche unscharfe Bereiche, die wahrscheinlich kleine, längliche Moleküle darstellen, die zwischen Proteinoberflächen eingeklemmt sind. Ihre Form und die chemische Umgebung deuten darauf hin, dass es sich um Lipide handeln könnte, dieselben öligen Moleküle, aus denen Zellmembranen bestehen. Das stützt frühere Hinweise, dass Lipide die RegIIIα-Assemblierung fördern, möglicherweise indem sie wie molekularer Klebstoff die Verbindungen zwischen Untereinheiten stabilisieren.
Der Ein-/Aus-Schalter: pH und ein verborgenes Segment
Das Team untersuchte auch, was steuert, wann RegIIIα sich zusammenlagern kann. Bevor es aktiv wird, trägt das Protein ein kurzes „Pro-Segment“, das von Verdauungsenzymen abgeschnitten werden muss. In ihrer hochauflösenden Filamentstruktur ist im Zentrum der Assemblierung kein Platz für dieses zusätzliche Stück, was impliziert, dass das Pro-Segment die Fähigkeit von RegIIIα blockiert, die porenbildenden Ringe und Filamente überhaupt zu bilden. Sie stellten fest, dass die Neigung zur Filamentbildung auch von der Säure abhängt: Filamente bilden sich leicht bei einem pH-Wert, der dem des Dünndarms ähnelt, aber schlecht bei saurerem pH. Eine einzelne Aminosäure, Histidin 50, scheint als pH-empfindlicher Schalter zu fungieren; wenn sie durch eine andere Restgruppe ersetzt wird, verliert die Filamentbildung weitgehend ihre pH-Empfindlichkeit. Zusammen schaffen diese Merkmale – Enzymabschnitt, Lipidbindung und pH – ein gestuftes Kontrollsystem, das steuert, wann und wo RegIIIα aktiv ist.
Welche Bedeutung das für die Darmgesundheit hat
Insgesamt liefert diese Arbeit die bisher detaillierteste Darstellung davon, wie RegIIIα-Moleküle zu größeren Strukturen zusammengesetzt werden, die sowohl mit ihrer antibakteriellen Wirkung als auch mit ihrem selbstbegrenzenden Verhalten zusammenhängen. Dieselben Schnittstellen, die die Filamente bilden, bauen auch die hexameren Ringe auf, von denen angenommen wird, dass sie Poren in bakteriellen Membranen bilden, was auf ein empfindliches Gleichgewicht zwischen einer potenten, tödlichen Form und einem sichereren, gedämpften Zustand hinweist. Die Zuordnung krankheitsassoziierter Mutationen auf diese Struktur zeigt, dass viele von ihnen an wichtigen Kontaktpunkten liegen, was nahelegt, dass Störungen in der Assemblierung bestimmten Darmerkrankungen oder Pankreasstörungen zugrunde liegen könnten. Indem die Studie klärt, wie dieses natürliche Antibiotikum aktiviert wird, von Lipiden geführt wird und durch den lokalen pH-Wert geformt wird, legt sie die Grundlage für künftige Bestrebungen, unsere angeborene Abwehr gezielt zu verstärken — entweder um Infektionen besser zu bekämpfen oder um sie zu beruhigen, wenn sie fehlreguliert ist.
Zitation: Han, J., Cao, Q. Structural basis for human RegⅢα filament formation. Commun Chem 9, 117 (2026). https://doi.org/10.1038/s42004-026-01921-y
Schlüsselwörter: RegIIIα, Darm-Immunität, Cryo-Elektronenmikroskopie, Proteinfilamente, antibakterielle Peptide