Clear Sky Science · de
Azobenzol-gebundene ionisierbare amphiphile Janus-Glykoside für lichtgesteuerte, einkomponentige und organ-modulierbare pDNA-Lieferung
Mit Licht zu intelligenterer Genübertragung
Gentherapien versprechen, Krankheiten an ihrer Wurzel zu behandeln, indem sie Teile genetischer Information direkt in unsere Zellen bringen. Doch dieses fragile Gepäck sicher durch den Blutkreislauf, in die richtigen Organe und in Zielzellen zu lotsen, bleibt eine große Herausforderung. Diese Studie stellt eine neue Klasse winziger, zuckerbasierter Partikel vor, deren Verhalten sich mithilfe von Licht umschalten lässt, noch bevor sie in den Körper gelangen. So können Forschende steuern, wohin ein therapeutisches Gen gelangt und wie stark es exprimiert wird — und das bei weitgehend erhaltener Zellverträglichkeit. 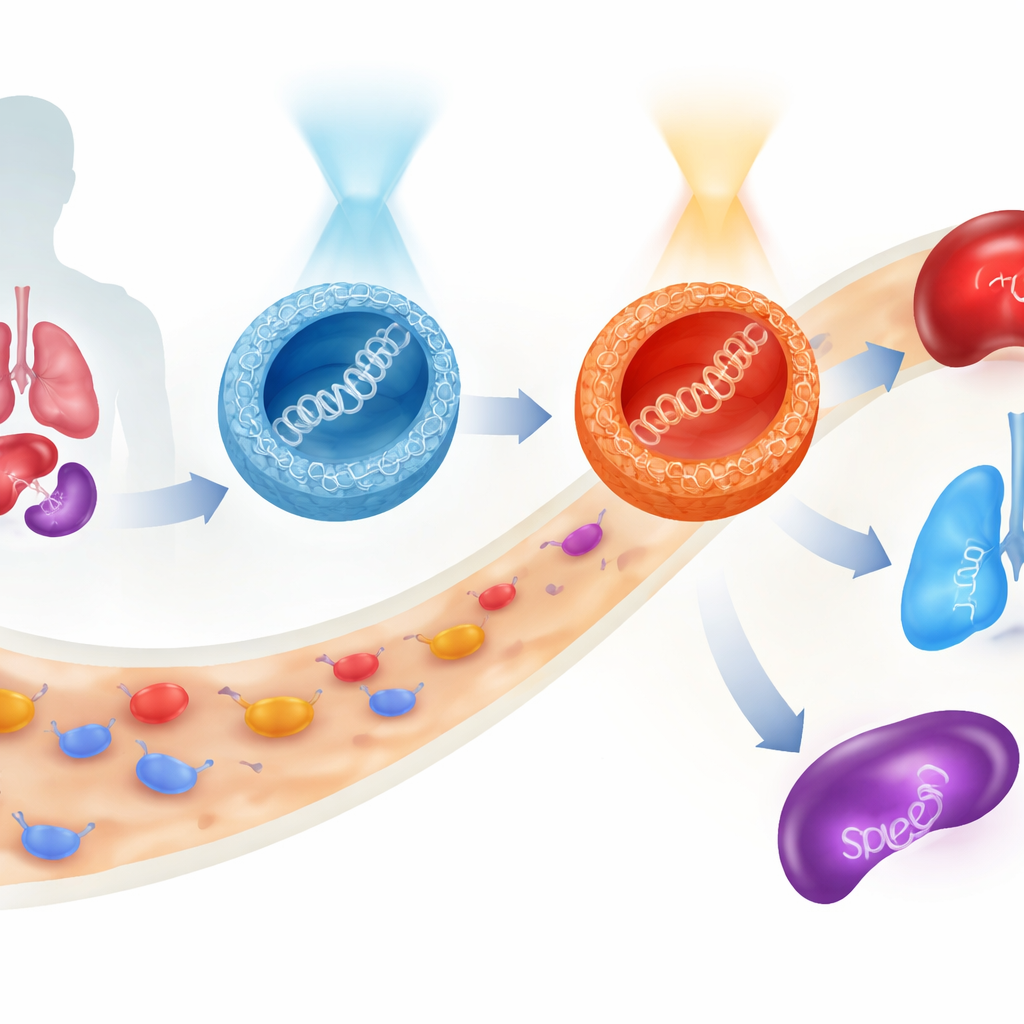
Der Bedarf an präzisen genetischen Kurieren
Die derzeit erfolgreichsten Vehikel zur Genlieferung sind Lipidnanopartikel, die die mRNA-COVID-19-Impfstoffe ermöglichten. Diese mehrkomponentigen Tröpfchen umschließen und schützen Nukleinsäuren, sammeln sich jedoch meist überwiegend in der Leber an und setzen nur einen kleinen Bruchteil ihrer Fracht innerhalb der Zellen frei. Durch Anpassung ihrer Zusammensetzung lässt sich zwar beeinflussen, welche Organe bevorzugt werden, doch die Gemische sind komplex und schwer präzise zu steuern. Das Team dieser Arbeit verfolgte stattdessen das Ziel, einzelne, wohldefinierte Moleküle zu entwerfen, die sich zu Nanopartikeln mit vorhersehbaren Formen und Eigenschaften zusammensetzen — und die von außen aktiv durch einen einfachen Lichtimpuls eingestellt werden können.
Eine molekulare Wippe, gesteuert durch Licht
Im Zentrum des neuen Systems stehen doppelte „Janus“-Glykoside: aus zwei Glukoseeinheiten aufgebaute Moleküle mit wasserliebenden, geladenen Köpfen und fettliebenden Schwänzen, die über ein zentrales Azobenzol-„Scharnier“ verbunden sind. Azobenzol kann unter Belichtung mit unterschiedlichen Lichtfarben zwischen zwei spiegelbildlichen Formen, genannt E und Z, umschalten. In wässriger Lösung mit DNA versammeln sich viele Kopien dieser Moleküle spontan zu weichen, geschichteten Partikeln, die sich um Stränge von Plasmid-DNA legen. Die Forschenden bereiterten zwei Varianten vor — eine mit Sauerstoffbrücken und eine mit Schwefelbrücken zwischen Zucker und Scharnier — um Stabilität und biologisches Verhalten fein abzustimmen. Durch Vorbestrahlung der Lösungen ließen sich entweder die E- oder die Z-Form anreichern, um zu untersuchen, wie jeder Zustand die entstehenden Genlieferpartikel prägt.
Wie gestaltwandelnde Partikel sich verhalten
Messungen von Partikelgröße, Oberflächenladung und innerer Struktur zeigten, dass das lichtinduzierte Umschalten zwischen E- und Z-Zustand klare physikalische Folgen hat. Allgemein erzeugte die Z-Form kleinere, gleichmäßigere Nanopartikel mit einem geordneteren, geschichteten Inneren als die E-Form. Mikroskopische Aufnahmen zeigten, dass diese inneren Anordnungen wechselnde Schichten aus lipidähnlichem Material und DNA ähneln. Wichtig ist, dass beide Zustände die DNA vor enzymatischem Abbau schützten. In kultivierten Zellen aus Niere, Leber und immunem Gewebe führten die verschiedenen Isomerzustände zu auffällig unterschiedlichen Genexpressionsniveaus, obwohl die zugrunde liegende DNA identisch war. Mehrfache Lichtimpulse, die nach dem Eindringen der Partikel in die Zellen appliziert wurden, steigerten die Genexpression um ein Mehrfaches. Das deutet darauf hin, dass der mechanische Ruck durch das Umschalten den Partikeln hilft, sich zu lockern und ihre Fracht freizusetzen, und möglicherweise auch ihr Entkommen aus intrazellulären Kompartimenten erleichtert. 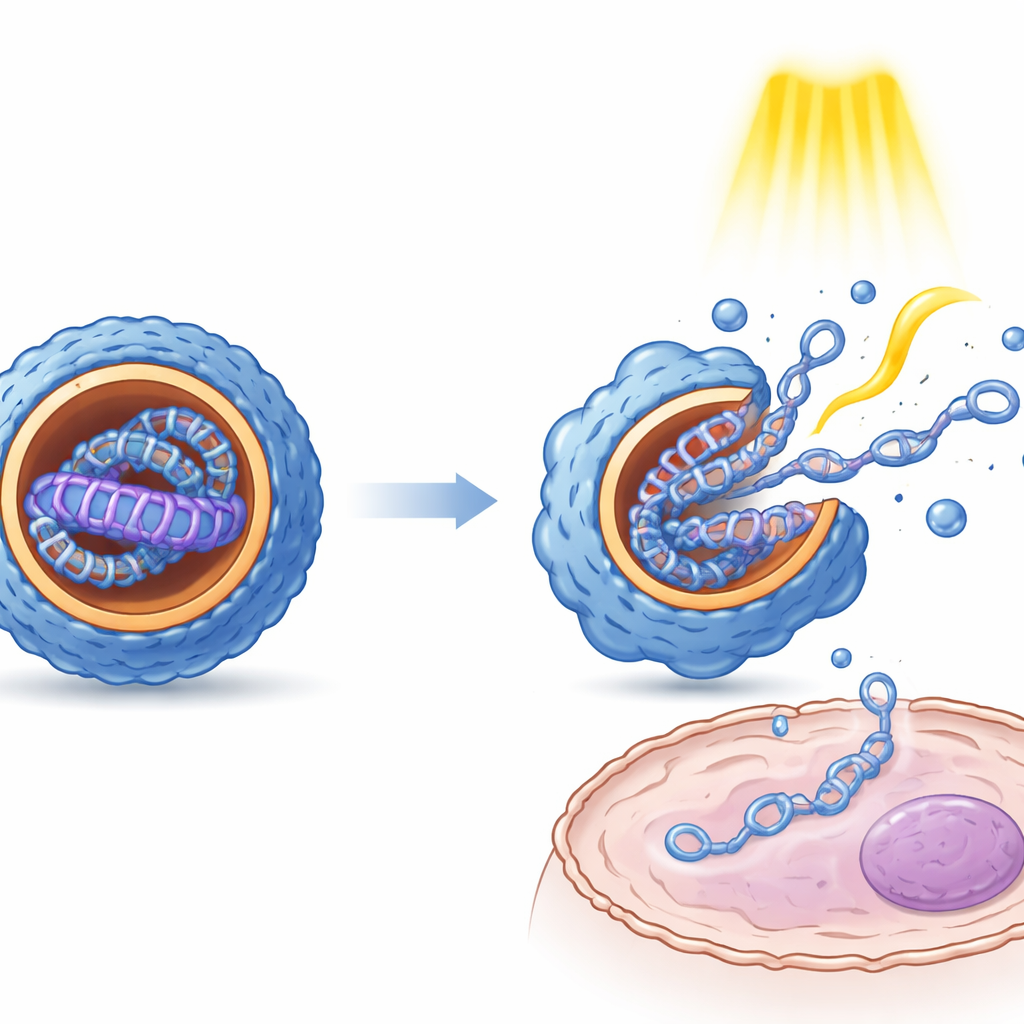
Gene zu bestimmten Organen leiten
Das überraschendste Verhalten zeigte sich in Mäusen. Wurden die sauerstoffgebundenen Partikel in ihrer E-reichen Form verabreicht, trat die Expression eines Marker-Gens überwiegend in der Leber und teilweise in der Lunge auf. Ein Vorumschalten auf die Z-Form vor der Injektion steigerte nicht nur die Gesamtexpression, sondern verschob auch die Verteilung zugunsten der Lunge. Die schwefelgebundenen Partikel erzählten eine andere Geschichte: Ihre Z-Form bevorzugte die Milz, ein zentrales Immunorgan. Somit konnten die Forschenden mit demselben grundlegenden molekularen Gerüst — und ohne die DNA-Fracht zu verändern — die Genaktivität überwiegend an Leber, Lunge oder Milz richten, allein durch Wahl der Verbindung (Sauerstoff oder Schwefel) und der lichtaktivierten Form (E oder Z) des Trägers. Während dieser Tests blieb die Zellvitalität hoch, was darauf hindeutet, dass das System vergleichsweise schonend ist.
Ein lichtstimulierbarer Weg zu künftigen Gentherapeutika
Alltagssprachlich hat das Team einen winzigen, lichtschaltbaren DNA-Shuttle gebaut. Vor der Injektion „programmiert“ eine kurze Lichtbehandlung die Shuttles in eine von zwei Formen. Jede Form setzt sich zu Nanopartikeln mit charakteristischer Größe und Oberflächencharakter zusammen, was wiederum bestimmt, wie stark sie an verschiedene Zelltypen haften und wo sie im Körper landen. Da dasselbe chemische Gerüst auf viele kleine Weisen modifiziert werden kann und weil das Umschalten reversibel ist und die DNA selbst nicht verändert, bietet diese Plattform eine flexible Methode, um Ort und Wirkungsweise von Gentherapien fein abzustimmen. Obwohl vor einer klinischen Anwendung noch viel Arbeit nötig ist, zeigt die Studie, dass sorgfältig entworfene, einkomponentige Träger, die sich mit Licht steuern lassen, zu mächtigen Werkzeugen für sicherere und präzisere Gentherapien werden könnten.
Zitation: Wang, Z., Rivero-Barbarroja, G., Benito, J.M. et al. Azobenzene-bridged ionizable amphiphilic Janus glycosides for light-controlled, single-component and organ-modulable pDNA delivery. Commun Chem 9, 118 (2026). https://doi.org/10.1038/s42004-026-01920-z
Schlüsselwörter: Genlieferung, lichtempfindliche Nanopartikel, Azobenzol-Schalter, zielgerichtete DNA-Therapie, Nanomedizin