Clear Sky Science · de
S9-Protease WprP2 katalysiert gleichmäßige Spaltung am Vorläuferpeptid in der RiPP-Biosynthese
Warum winzige Schneidwerkzeuge in Zellen wichtig sind
In Bakterien schneiden spezialisierte molekulare Scheren lange Aminosäureketten in kleinere, aktive Fragmente, die häufig zu Antibiotika oder anderen nützlichen Naturstoffen werden. Diese Studie entdeckt ein zuvor unbekanntes Schneidwerkzeug — eine Protease namens WprP2 — die ihr Zielpeptid mit ungewöhnlicher Präzision zuschneidet. Zu verstehen, wie dieses Enzym funktioniert, könnte Forschern helfen, neuartige bioaktive Peptide und Antibiotika der nächsten Generation zu entwickeln.
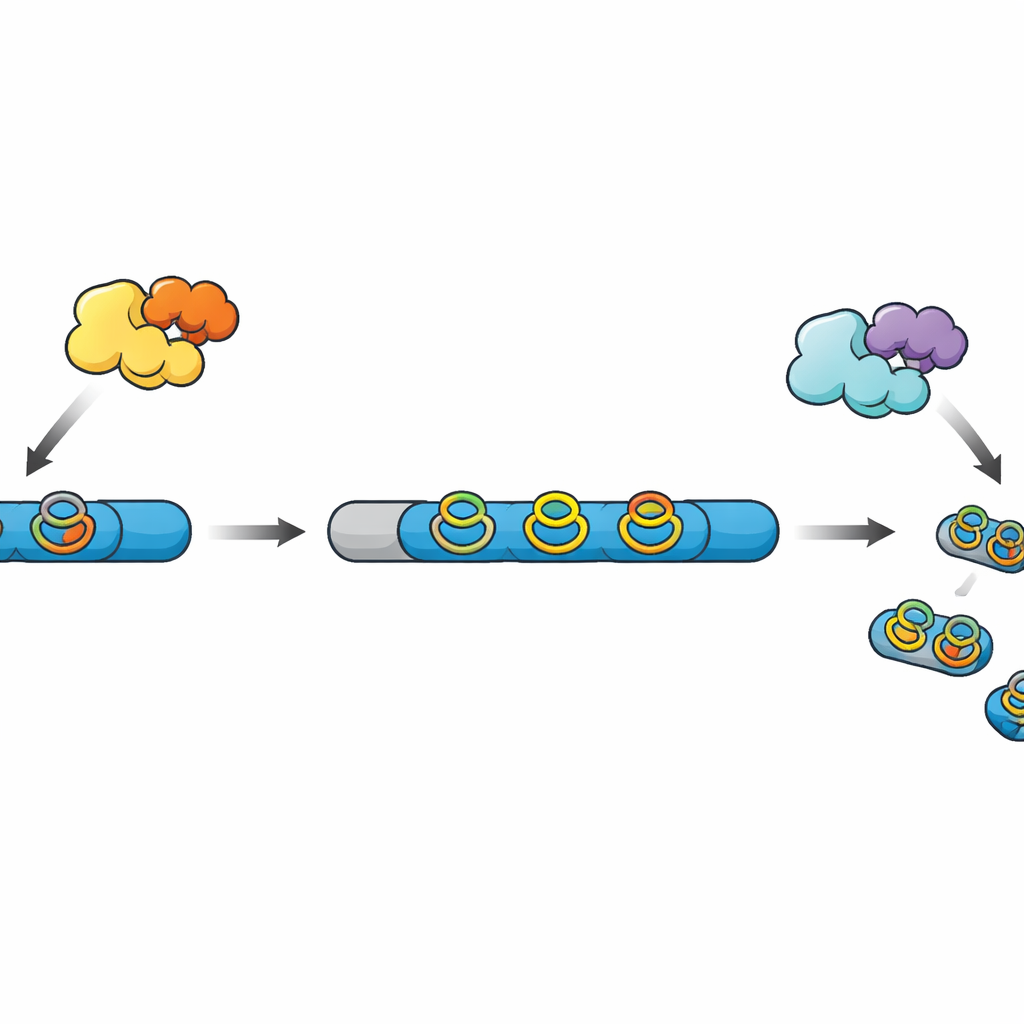
Von rohen Ketten zu fertigen Mini‑Medikamenten
Viele moderne peptidbasierte Naturstoffe, zusammengefasst als RiPPs, beginnen als einfache Ketten, die am Ribosom synthetisiert werden. Diese Ketten enthalten eine Leader-Region, die als Griff fungiert, und eine Core-Region, die nach einer Reihe chemischer Modifikationen zum Endprodukt wird. Andere Enzyme fügen Querbindungen und Ringe hinzu, die das Peptid stabiler und aktiver machen; schließlich entfernt eine Protease den Leader und setzt das reife Molekül frei. In einer neu entdeckten Familie von RiPPs bauen radikal-SAM-Enzyme kompakte „Cyclophan“-Ringe aus aromatischen Aminosäuren, aber in den meisten bekannten Biosynthese-Clustern fehlt die zugehörige Protease, sodass die letzten Verarbeitungsschritte rätselhaft bleiben.
Auf der Spur eines fehlenden Partnerenzyms
Die Autoren hatten zuvor ein Radikal-SAM-Enzym namens WprB1 untersucht, das identische Querbindungen in drei sich wiederholenden WPR-Segmenten eines Vorläuferpeptids erzeugte. In der neuen Arbeit durchsuchten sie bakterielle Genome nach Verwandten dieses Enzyms und suchten in der Nähe nach Genen, die eine Protease kodieren könnten. In Streptomyces venezuelae fanden sie einen vielversprechenden Cluster, der ein ähnliches Querbindungsenzym, ein Hilfsprotein, ein passendes Vorläuferpeptid mit drei WPR-Wiederholungen und eine Kandidaten-Serinprotease der S9-Familie enthielt, die sie WprP2 nannten. Das machte das System zu einem idealen Versuchsobjekt, um herauszufinden, wie das Peptid schließlich geschnitten wird, um die aktiven Fragmente freizusetzen.
Beobachtung des Peptids beim Zerschneiden
Um WprP2 zu untersuchen, stellten die Forscher das Vorläuferpeptid in Bakterien her, sowohl mit als auch ohne das Querbindungsenzym, reinigten es und mischten es dann in kontrollierten in-vitro-Reaktionen mit der Protease. Massenspektrometrie zeigte, dass WprP2 zunächst die Kette jeweils unmittelbar nach jedem WPR-Segment durchtrennt und anschließend einen zweiten Schnitt in einem festen Abstand vor einer bestimmten Prolin‑Restposition weiter entlang der Sequenz ausführt. Diese beiden Schritte erzeugen eine Serie kleinerer, gleichförmiger Fragmente. Erstaunlicherweise führte WprP2 dieses Schnittmuster aus, unabhängig davon, ob das Querbindungsenzym zuvor die Cyclophan-Ringe eingebaut hatte, was zeigt, dass die Ringe für die Erkennung nicht erforderlich sind. Im Vergleich mit kommerziellem Trypsin, das an bestimmten quervernetzten Stellen nicht schneiden kann, funktionierte WprP2 weiterhin und unterstreicht so seine ungewöhnliche Robustheit.
Entschlüsselung dessen, was das Enzym erkennt
Die Forscher fragten anschließend, welche Merkmale des Peptids WprP2 tatsächlich liest. Durch systematisches Verändern einzelner Aminosäuren rund um die Schnittstellen stellten sie fest, dass viele benachbarte Reste wenig Einfluss hatten, aber die Änderung eines Schlüssel‑Arginins innerhalb des WPR-Segments oder der Glutamin‑ bzw. Prolin‑Reste an der zweiten Schnittstelle diesen jeweiligen Schritt blockieren konnte. Experimente mit einem verwandten Vorläuferpeptid, das andere flankierende Reste trug, zeigten, dass die Protease weiterhin nach WPR-Wiederholungen schnitt, den zweiten Schnitt jedoch nur ausführte, wenn ein Glutamin‑Prolin‑Paar vorhanden war. Computergenerierte Strukturmodelle mit AlphaFold3 stützten dieses Bild: in den vorhergesagten Komplexen reihen sich die WPR-basierten und die Glutamin‑Prolin‑Stellen der Reihe nach am katalytischen Zentrum des Enzyms aus, was zu einem sequentiellen Zwei‑Schritt‑Mechanismus passt.
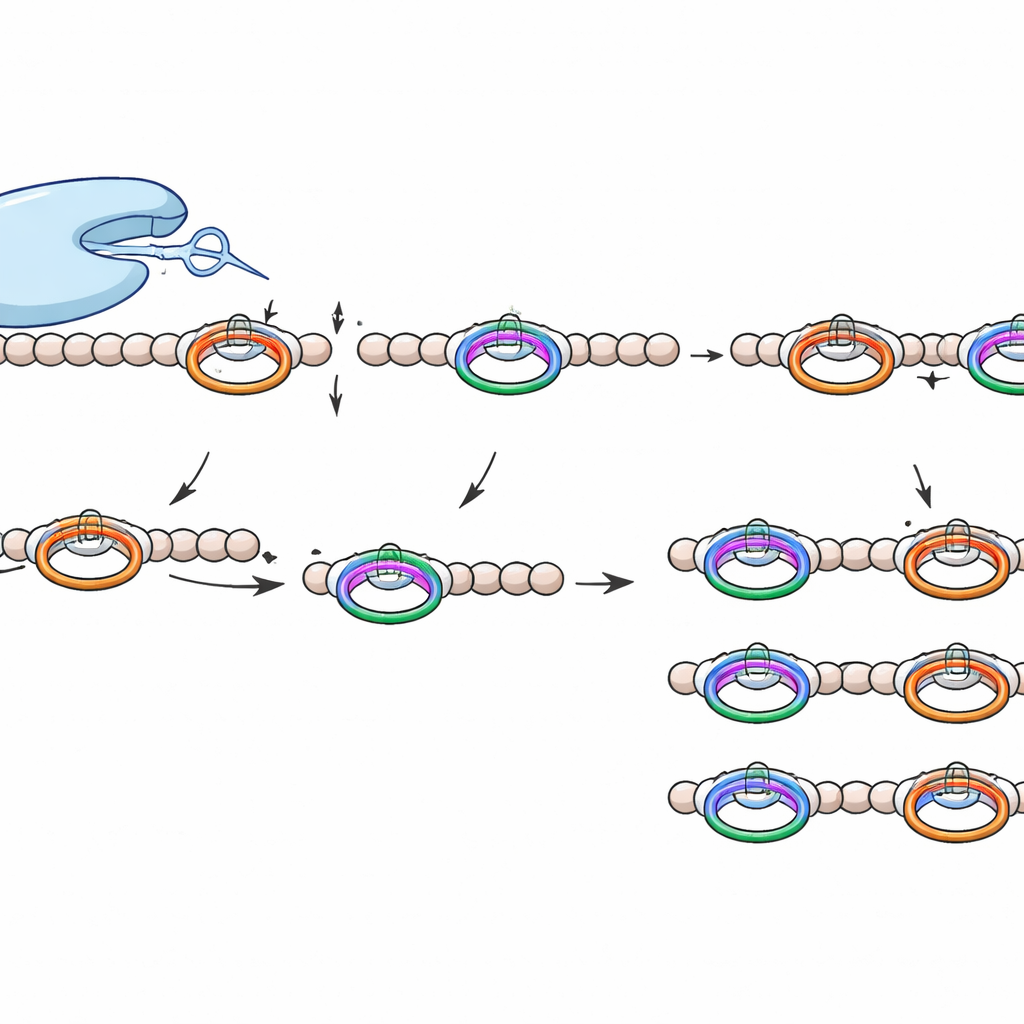
Was dieses Schneidwerkzeug besonders macht
WprP2 gehört zur größeren S9-Familie von Proteasen, zu der bereits medizinisch relevante Enzyme zählen, unterscheidet sich aber in mehreren Punkten. Es schneidet auf der N‑terminalen Seite einer Prolin‑Rest statt danach, es wirkt auf ein sich wiederholendes Motiv, um über die gesamte Vorläuferkette gleich große Fragmente zu erzeugen, und es zeigt eine breite Toleranz gegenüber den Aminosäuren, die zwischen seinen beiden Erkennungsstellen liegen. Diese Kombination aus Präzision und Flexibilität wurde bisher bei RiPP‑assoziierten Proteasen nicht beobachtet.
Wie diese Entdeckung genutzt werden könnte
Indem sie eine Protease aufgedeckt haben, die einfache Sequenzhinweise erkennt und gleichmäßige, wiederholte Schnitte ausführt, erweitert diese Arbeit das wachsende Werkzeugset für Peptid-Engineering um ein leistungsfähiges neues Instrument. Praktisch könnte WprP2 dazu genutzt werden, Designerpeptide freizusetzen oder umzubauen, einschließlich solcher mit komplexen Querbindungen, die gegenüber Standardenzymen wie Trypsin resistent sind. Für Nicht‑Spezialisten lautet die zentrale Erkenntnis: Wissenschaftler haben eine neue Art molekularer Scheren entdeckt, die lange Peptidketten in präzise, gleich große Stücke zerschneidet und so den Weg für eine kontrolliertere Produktion potenzieller Antibiotika und anderer bioaktiver Moleküle öffnet.
Zitation: Haedar, J.R., Khan, A.H., Ma, S. et al. S9 protease WprP2 catalyzes uniform cleavage on the precursor peptide in RiPP biosynthesis. Commun Chem 9, 108 (2026). https://doi.org/10.1038/s42004-026-01915-w
Schlüsselwörter: RiPP-Peptide, Serinprotease, WprP2, Cyclophan-Naturstoffe, Peptid-Engineering