Clear Sky Science · de
Sterische Einschluss-induzierte Emissionssonde zur Überwachung von Proteinkonformationen in lebenden Zellen
Formwandelnde Proteine in Echtzeit beobachten
In jeder lebenden Zelle verändern Proteine ständig ihre Gestalt, während sie Signale weiterleiten, ihre Umgebung wahrnehmen und lebenswichtige Aufgaben erfüllen. Viele Krankheiten entstehen, wenn diese Formänderungen fehlgeleitet werden, doch war es überraschend schwierig, solche Bewegungen direkt in lebenden Zellen zu beobachten – insbesondere über sehr schnelle und sehr langsame Zeitskalen hinweg. Diese Arbeit stellt eine neue lichtemittierende Sonde vor, genannt BIOSCE, die winzige Proteinbewegungen in sichtbare Aufhellungen verwandelt und es Forschern ermöglicht, einzelne Proteine beim Biegen, Drehen und Interagieren in Echtzeit innerhalb lebender Zellen zu verfolgen. 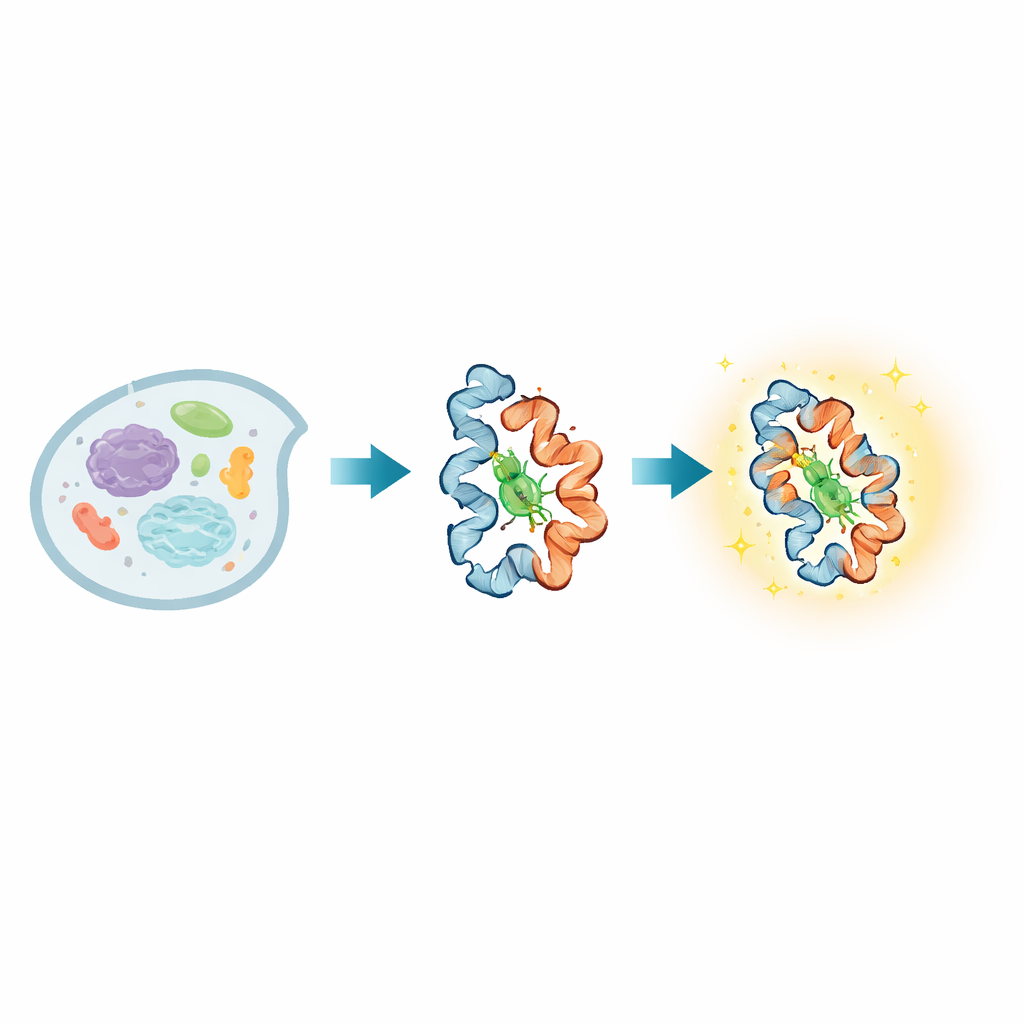
Ein neuer Lichtschalter für bewegte Proteine
Im Kern von BIOSCE steht ein kleiner Farbstoff, MTPABP‑Cl, der heller wird, wenn er zusammengedrückt wird. Die Forscher koppeln diesen Farbstoff an einen weit verbreiteten Protein‑Tag namens HaloTag, der genetisch an nahezu jedes Zielprotein fusioniert werden kann. Wenn das markierte Protein seine Form ändert oder dichter mit Nachbarproteinen zusammenpackt, verändert sich der „Raum“, den der Farbstoff zum Schwingen hat. In einer lockeren Umgebung können sich die inneren Teile des Farbstoffs frei drehen und ein Großteil des absorbierten Lichts geht durch Bewegung verloren; in einer engeren Tasche werden diese Bewegungen blockiert und der Farbstoff setzt stattdessen mehr dieser Energie als Licht frei. Diese „sterische Einschluss‑induzierte Emission“ verwandelt subtile Verschiebungen in der lokalen Dichte um ein einzelnes Protein in eine gleichmäßige Helligkeitsänderung statt in ein einfaches An‑/Aus‑Signal und macht die Sonde sehr empfindlich für kleine Konformationsänderungen.
Entwicklung und Prüfung des druckempfindlichen Farbstoffs
Das Team entwickelte und synthetisierte MTPABP‑Cl so, dass er in Lösung schwach leuchtet, aber heller wird, wenn er durch HaloTag oder durch eine kompaktere Fusionsproteine gehalten wird. Sorgfältige Messungen zeigten, dass der Farbstoff blaues Licht absorbiert und fernrotes Licht emittiert, was vorteilhaft für die Bildgebung in tieferen Zellschichten und für langzeitige Beobachtungen ist. Wenn er nur an HaloTag gebunden war, stieg die Lichtausbeute; wenn HaloTag an ein Partnerprotein fusioniert war, das sich um den Farbstoff faltete, nahm die Helligkeit noch weiter zu. Computersimulationen bestätigten, dass der Farbstoff in kompakteren Proteinanordnungen stärkere Dichte, eine kleinere exponierte Oberfläche und mehr stabilisierende Kontakte erfährt – alles Faktoren, die Bewegungen einschränken und die Emission verstärken. Der Farbstoff bindet außerdem schnell und spezifisch an HaloTag, zeigt sehr geringes Hintergrundsignal in Zellen ohne Tag und bleibt in den verwendeten Konzentrationen nicht toxisch, was seine Verwendung in Lebendzellversuchen unterstützt. 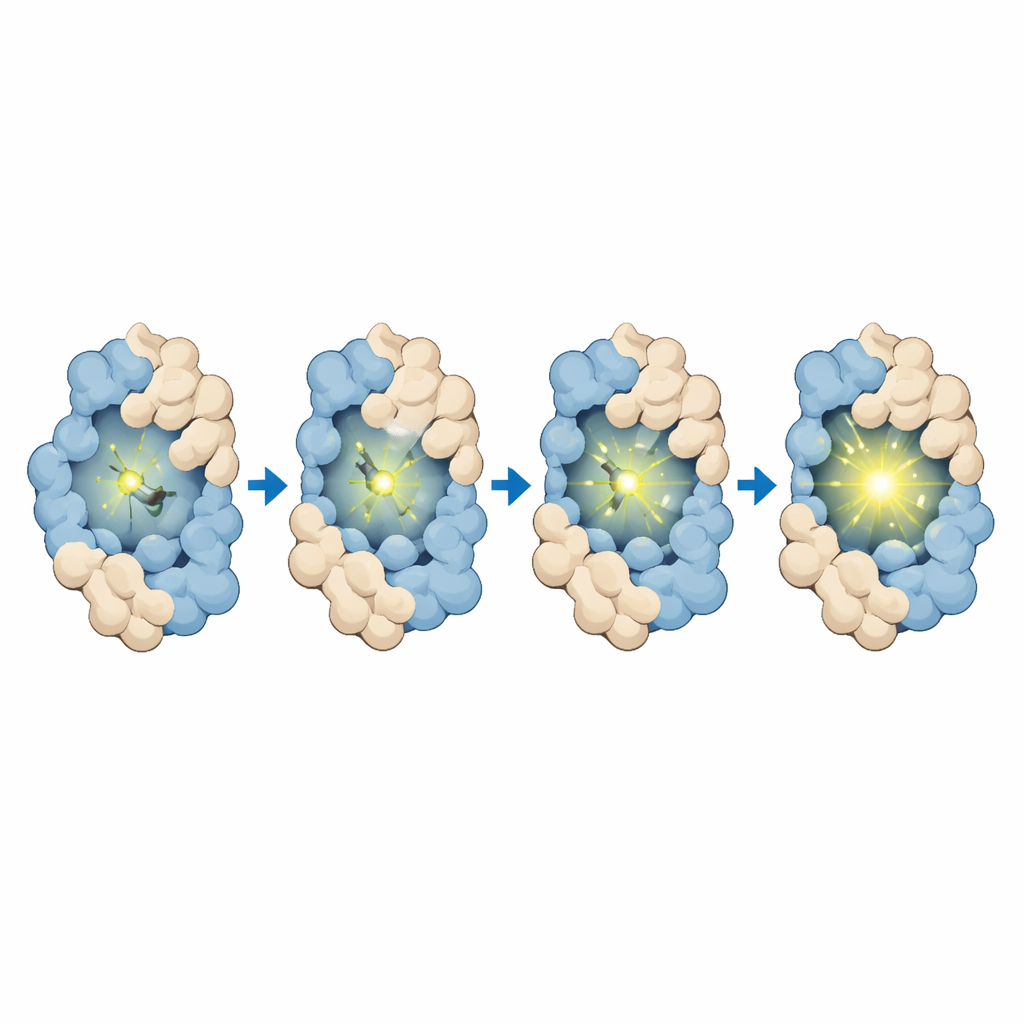
Schnellen Signalen und Proteinbegegnungen folgen
Um zu demonstrieren, was BIOSCE leisten kann, wendeten die Autoren es auf mehrere bekannte zelluläre Prozesse an. Zunächst passten sie einen Calcium‑Sensor auf der Basis von Calmodulin an, ein Protein, das seine Form ändert, wenn es Calciumionen bindet – zentrale Botenstoffe bei neuronaler Aktivität und vielen anderen Zellereignissen. Durch Fusion von Calmodulin mit HaloTag und Markierung mit MTPABP‑Cl erzeugten sie einen chemigenetischen Indikator namens SCECaMP. In humanen Zellen und neuronähnlichen Zellen wurde dieser Indikator mit Calcium‑Spitzen, ausgelöst durch Kaliumstimulation, heller und dunkler, mit Reaktionsgeschwindigkeiten, die mit den weit verbreiteten GCaMP‑Fluoreszenzproteinen vergleichbar sind. Da das BIOSCE‑Signal direkt von der lokalen Dichte um den Farbstoff abhängt, kann es Calmodulins strukturelle Änderungen getreu wiedergeben und gleichzeitig stabile, langlebige Fluoreszenz für ausgedehnte Bildgebung liefern.
Medikamentenvermittelte Interaktionen und Toxin‑Schäden sichtbar machen
Die Forscher prüften anschließend, ob BIOSCE verfolgen kann, wenn zwei Proteine durch ein Medikament zusammengebracht werden. Sie nutzten ein klassisches System, in dem Rapamycin zwei Partner, FKBP und FRB, in einem wichtigen Wachstumsregulationsweg zusammenführt. Durch Anbringen von HaloTag an FKBP oder FRB und Markierung mit MTPABP‑Cl beobachteten sie schnelle, millisekunden‑skalige Anstiege der Fluoreszenz, als Rapamycin diese Proteine näher zusammenbrachte und umordnete. Der Helligkeitsanstieg spiegelte eine dichtere Mikroumgebung um den Farbstoff wider, als die Partner in enge Nähe traten. In einem komplexeren Test untersuchten sie SNAP25, ein für die Neurotransmitterfreisetzung essentielles Protein der Nerventerminale und das Hauptziel von Botulinum‑Neurotoxin A. Indem sie HaloTag auf beiden Seiten der Schnittstelle des Toxins platzierten und mit dem Farbstoff markierten, konnten sie die Bewegungen des N‑terminalen und C‑terminalen Fragmentes nach der Spaltung getrennt verfolgen. Einzelpartikelverfolgung zeigte, dass ein Fragment in der Nähe der Zellmembran verankert blieb, während das andere freier durch das Zytoplasma diffundierte, wobei das genaue Muster davon abhing, ob die Markierung vor oder nach der Toxinexposition erfolgte. Die Sonde meldete sogar schnelle, zinkinduzierte Konformationsänderungen in SNAP25 während dieses Prozesses.
Bedeutung für Biologie und Medizin
Zusammen zeigen diese Ergebnisse, dass BIOSCE eine vielseitige neue Methode ist, um zu visualisieren, wie einzelne Proteine in lebenden Zellen über ein breites Spektrum an Zeitskalen hinweg bewegen, falten und interagieren. Da die Methode auf einer allgemeinen HaloTag‑Fusion und einem einzigen kleinmolekularen Farbstoff beruht, kann sie prinzipiell auf viele verschiedene Proteine angewendet werden, ohne den gesamten Sensor für jedes Ziel neu zu entwerfen. Die kontinuierliche, einschlussabhängige Helligkeitsänderung erlaubt es Forschern, subtile strukturelle Verschiebungen zu detektieren statt nur große, binäre Ereignisse. Für die Zukunft planen die Autoren, die Sonde‑Zufuhr und die Eindringtiefe der Bildgebung zu verbessern, damit BIOSCE in Geweben und ganzen Organismen eingesetzt werden kann. Gelingt dies, könnte dieser Ansatz zu einem mächtigen Werkzeug werden, um Ort, Bewegung und Funktion von Proteinen in Gesundheit und Krankheit zu verknüpfen und möglicherweise in detaillierte Computermodelle zellulären Verhaltens einfließen.
Zitation: Jia, H., Yang, L., Yang, Y. et al. Steric confinement-induced emission probe for monitoring protein conformations in live cells. Commun Chem 9, 109 (2026). https://doi.org/10.1038/s42004-026-01914-x
Schlüsselwörter: dynamik von Proteinkonformationen, Lebendzell‑Bildgebung, fluoreszierende Biosensoren, HaloTag‑Sonden, Botulinum‑Neurotoxin