Clear Sky Science · de
Minimierter Probenverbrauch für zeitaufgelöste serielle Kristallographie angewandt auf den Redoxzyklus des menschlichen NQO1
Enzyme in Aktion beobachten mit weniger kostbaren Proben
Die moderne Biologie nutzt zunehmend leistungsstarke Röntgenlaser, um zu sehen, wie sich biomolekulare Strukturen bewegen und verformen. Solche Experimente verbrauchen jedoch normalerweise enorme Mengen an mühsam hergestelltem Protein. Diese Studie stellt eine neue Methode vor, um winzige Proteinkristalle bei der Zuführung in einen Röntgen-Freie-Elektronen-Laser wesentlich effizienter zu verwenden und den benötigten Materialaufwand um bis zu 97 % zu reduzieren. Gleichzeitig zeigt sie, dass diese sparsamere Methode dennoch frühe Schritte im Wirkungszyklus eines medizinisch relevanten menschlichen Enzyms erfassen kann und damit den Weg für häufiger durchgeführte „Filme“ von Proteinen bei der Arbeit ebnet. 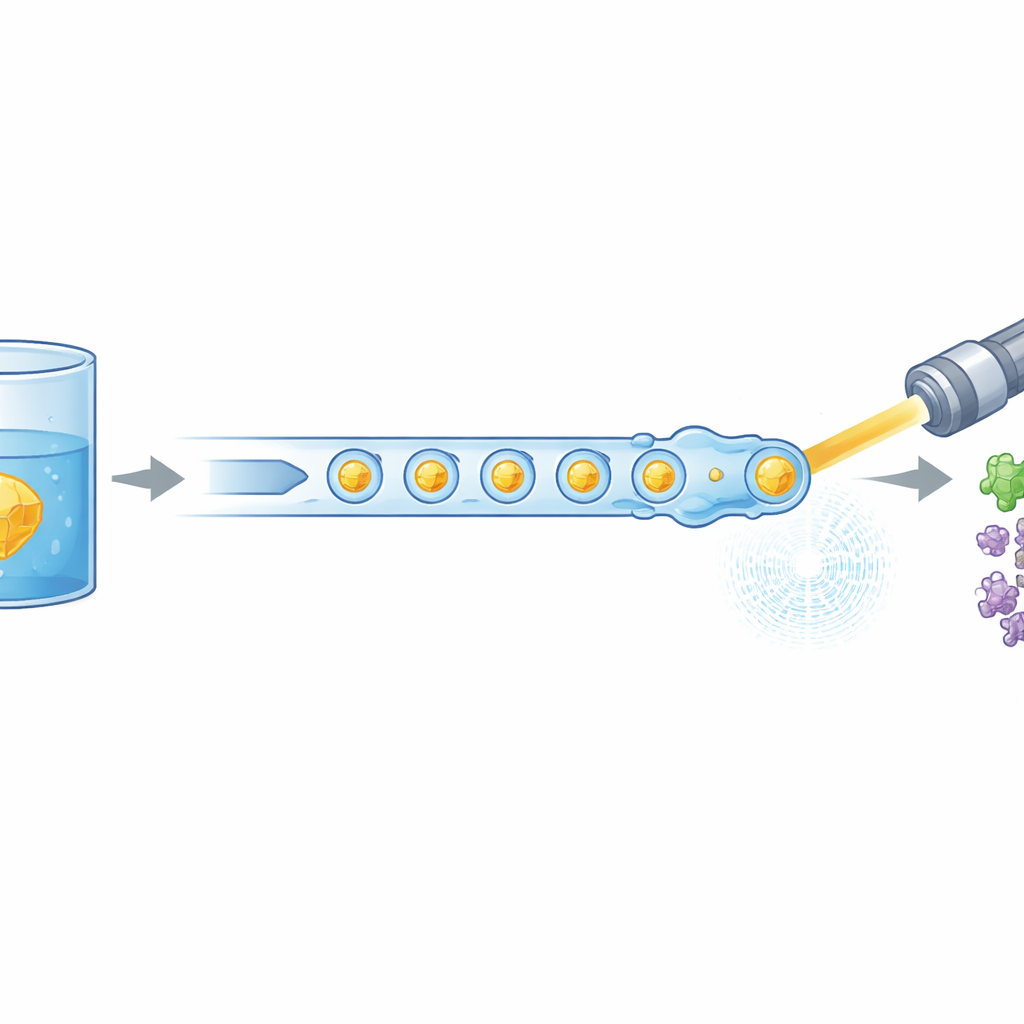
Warum molekulare Filme so teuer sind
Um zu verstehen, wie Proteine ihre Aufgaben tatsächlich erfüllen, wenden sich Forschende zunehmend von statischen Schnappschüssen zu zeitaufgelösten „Filmen“, die Reaktionen in Echtzeit verfolgen. Ein führender Ansatz, die zeitaufgelöste serielle Kristallographie, sprüht Millionen mikroskopischer Proteinkristalle durch einen extrem hellen Röntgenstrahl. Jeder Kristall wird nur einmal getroffen und liefert so eine schädigungsfreie Momentaufnahme; tausende solcher Bilder werden zu einem vollständigen Bild zusammengesetzt. Der Haken ist, dass für jeden Zeitpunkt einer Reaktion — Zehntelsekunden, ganze Sekunden usw. — eine neue Charge Kristalle benötigt wird. Da die Proteinsynthese und -aufbereitung langsam und teuer sein kann, ist der Probenverbrauch zu einem wichtigen Engpass geworden, insbesondere an Spitzeneinrichtungen wie dem European XFEL, wo Röntgenpulse in schnellen Zügen mit Megahertz-Frequenz eintreffen.
Eine neue Art, winzige Tropfen auf Abruf zu liefern
Die Forschenden gingen das Problem an, indem sie die Zuführung der Kristalle in den Röntgenstrahl neu gestalteten. Statt eines kontinuierlichen Flüssigkeitsstroms erzeugen sie eine sorgfältig getaktete Abfolge mikroskopischer Tropfen, die jeweils Proteinkristalle enthalten und durch eine Ölphase getrennt sind. Ein winziges 3D-gedrucktes Bauteil kombiniert zwei Ströme — Proteinkristalle und einen gelösten Reaktionspartner — zu kleinen gemischten Volumina, die dann in Tropfen abgetrennt werden. Diese Tropfen werden durch eine gasfokussierte Düse geführt, die einen schmalen Jet bildet, der mit dem Vakuum und den Geschwindigkeitsanforderungen des XFEL kompatibel ist. Entscheidend ist, dass die Tropfenproduktion elektrisch mit dem Timing der Röntgenpulz-Züge synchronisiert wird, sodass nahezu jeder nützliche Puls einen Tropfen trifft statt leere Flüssigkeit. 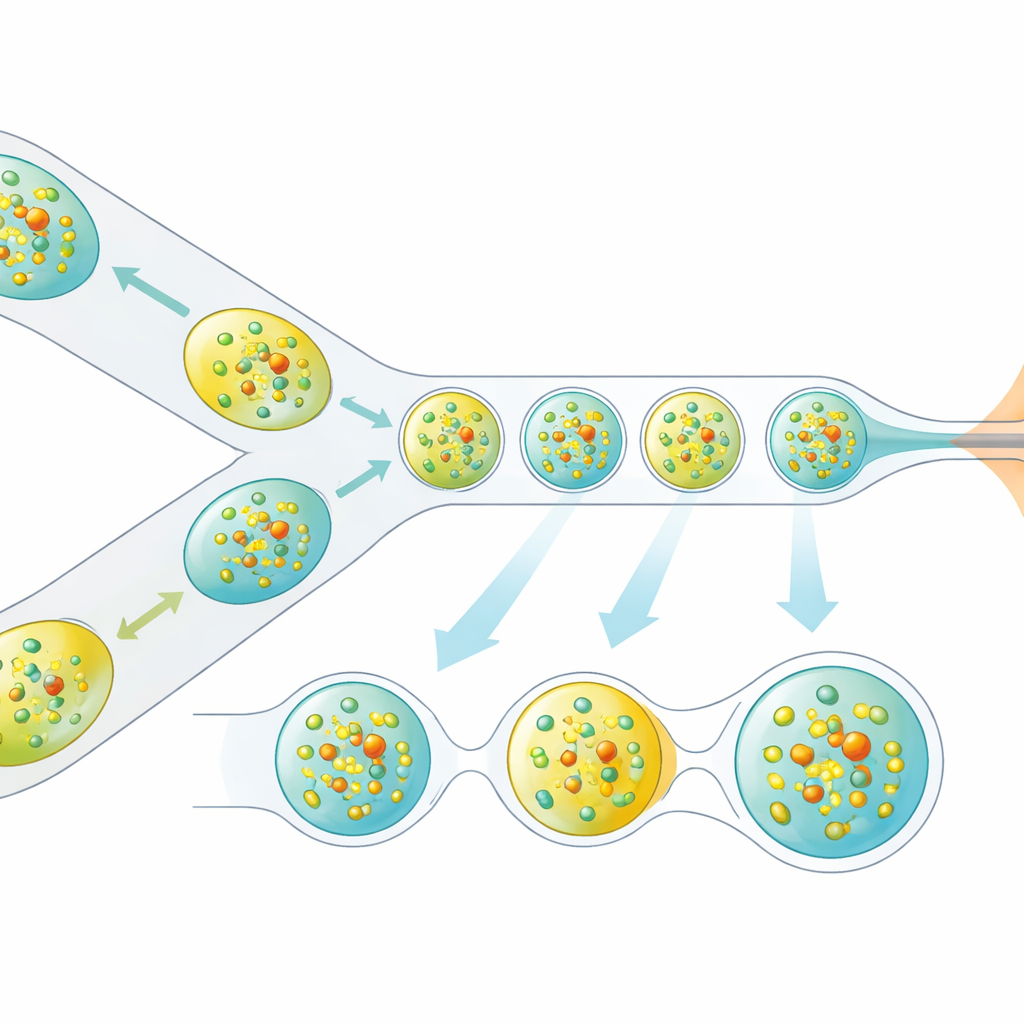
Erprobung der Methode an einem menschlichen Enzym
Um zu zeigen, dass der tropfenbasierte Ansatz für reale biologische Fragestellungen taugt, untersuchte das Team NAD(P)H:chinon-Oxidoreduktase 1 (NQO1), ein menschliches Enzym, das am zellulären Redoxgleichgewicht beteiligt ist und mit Erkrankungen in Verbindung gebracht wird. Sie mischten Mikrokristalle von NQO1 mit dessen natürlichem Cofaktor NADH und untersuchten das System an zwei frühen Zeitpunkten: 0,3 Sekunden und 1,2 Sekunden nach dem Mischen. Anhand der resultierenden Röntgenbeugungsmuster rekonstruierten sie dreidimensionale Strukturen des Enzyms für jede Verzögerung. Trotz deutlich geringerem Proteinverbrauch im Vergleich zu herkömmlichen kontinuierlichen Durchfluss-Experimenten war die Datenqualität ausreichend, um feine Elektronendichte-Merkmale in den aktiven Zentren des Enzyms zu erkennen, konsistent mit NADH-Molekülen, die mit geringer Besetzung zu binden beginnen.
Was die frühen Strukturaufnahmen zeigen
Die Strukturen zeigen, dass kurz nach dem Mischen nicht alle aktiven Zentren im Kristall gleich reagieren. Bei 0,3 Sekunden sind Hinweise auf NADH deutlich in drei von vier aktiven Zentren der Einheitszelle sichtbar und treten oft in mehr als einer Konformation auf, was darauf hindeutet, dass der Cofaktor mehrere Positionen erkundet, bevor er sich festlegt. Nach 1,2 Sekunden haben sich einige dieser Merkmale zu einer dominanten Bindungsweise geschärft, doch bleibt das Gesamtbild flexibel und nur partiell besetzt. Dieses ungleichmäßige, sich verändernde Verhalten stimmt mit früheren biochemischen Befunden überein, dass die beiden Untereinheiten eines NQO1-Dimers nicht völlig synchron agieren, sondern eine „half-of-the-sites“-Aktivität zeigen, bei der eine Seite zuerst reagiert, während die andere nachhinkt. Die zeitaufgelösten Daten liefern damit einen frühen strukturellen Einblick, wie sich diese Asymmetrie im Raum ausprägt.
Proben sparen bei erhaltenem wissenschaftlichem Gehalt
Praktisch betrachtet reduzierte die segmentierte Tropfenmethode den Proteinverbrauch für die Messungen bei 0,3 Sekunden um etwa das Sechsfache und für die Experimente bei 1,2 Sekunden um bis zu 97 % gegenüber traditionellen kontinuierlichen Jets unter ähnlichen Bedingungen. Dennoch lieferte sie verlässliche Strukturinformationen bei Raumtemperatur und war mit der anspruchsvollen Pulsstruktur des European XFEL kompatibel. Für Nicht-Spezialisten lautet die Schlussfolgerung: Forschende können nun beobachten, wie Enzyme wie NQO1 ihre Arbeit nahezu in Echtzeit beginnen, während sie pro Zeitpunkt nur Milligramm kostbarer Probe verwenden. Dadurch wird es viel realistischer, viele Reaktionszeiten und viele verschiedene Proteine zu untersuchen und so letztlich zu verstehen, wie medizinisch wichtige Enzyme sich bewegen, biegen und zusammenarbeiten, während sie die Chemie des Lebens ausführen.
Zitation: Doppler, D., Grieco, A., Koh, D. et al. Minimized sample consumption for time-resolved serial crystallography applied to the redox cycle of human NQO1. Commun Chem 9, 107 (2026). https://doi.org/10.1038/s42004-026-01908-9
Schlüsselwörter: serielle Kristallographie, Röntgen-Freie-Elektronen-Laser, Tropfenmikrofluidik, Enzymdynamik, NQO1